Les politiques publiques de lutte contre l’antibiorésistance dans le secteur animal au cours des dix dernières années en France (plans Ecoantibio) ont porté leur principal angle d’action sur la meilleure maîtrise de l’usage vétérinaire des antibiotiques [1]. Des résultats très importants ont été obtenus, dont une réduction d’environ 50 % de l’exposition des animaux aux antibiotiques (tous antibiotiques confondus), et d’environ 90 % si l’on ne considère que les antibiotiques dits « d’importance critique » (AIC) pour l’Homme (céphalosporines de 3e et 4e générations et fluoroquinolones) (Figure 1). Cet objectif de maîtrise de l’usage vétérinaire des antibiotiques s’est appuyé sur des dispositions incitatives mais également réglementaires, contraignant les vétérinaires à la réalisation d’un antibiogramme avant toute prescription d’un AIC et leur interdisant strictement l’emploi d’une longue liste d’autres antibiotiques utilisés en médecine humaine, tels que la vancomycine, le linézolide ou les carbapénèmes.
Evolution de l’exposition des animaux (toutes espèces confondues) aux antibiotiques d’importance critique pour l’Homme au cours des plans Ecoantibio.
Pour autant, plusieurs situations de terrain montrent que la résistance à un antibiotique chez un animal ne résulte pas nécessairement de son exposition au dit antibiotique. Des phénomènes de co-sélection peuvent d’une part être observés, qui relèvent en fait de l’administration d’un autre antibiotique. Dans le cadre de la surveillance de l’antibiorésistance chez les animaux malades en France, le réseau Résapath [2] analyse les niveaux de multi-résistance des souches bactériennes isolées lors d’infections (Figure 2). Si l’on analyse ces données en détail, il apparaît par exemple que certaines bactéries, notamment les Escherichia coli producteurs de bêta-lactamases à spectre étendu (BLSE), sont souvent résistants à plusieurs classes différentes d’antibiotiques. Une telle bactérie pourra persister chez un animal suite à l’usage d’un seul de ces antibiotiques, tout en étant résistante aux autres, même en l’absence de sélection directe par ceux-ci.
Evolution entre 2011 et 2021 des proportions de souches de E. coli multi-résistantes aux antibiotiques (données du Résapath).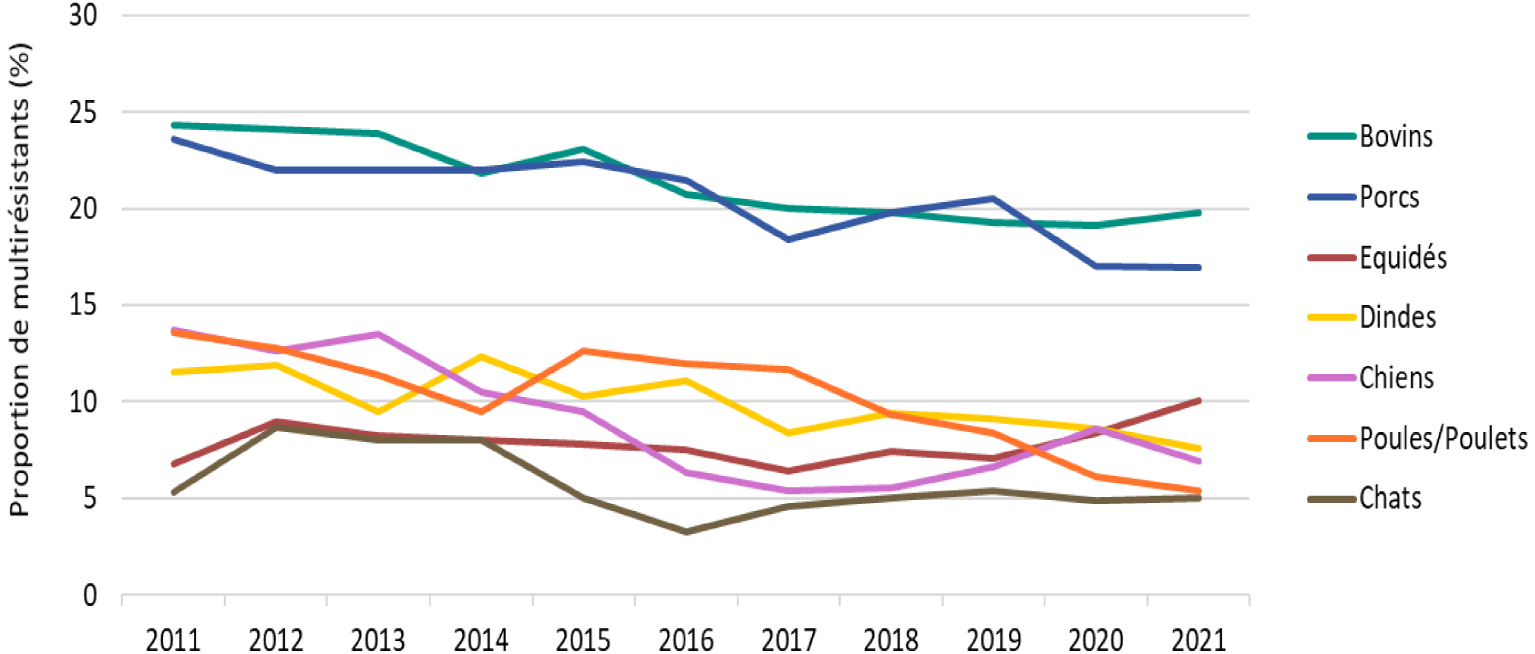
Mais lorsque les animaux n’ont reçu aucune antibiothérapie, ce sont des évènements de transmission de bactéries résistantes, ou de plasmides de résistance, qui sont à mettre en cause dans l’émergence de l’antibiorésistance. Plusieurs exemples peuvent illustrer l’importance de cette transmission de l’antibiorésistance dans le monde animal.
Récemment, une étude conduite par notre équipe [3] au sein d’un centre de soins pour animaux sauvages blessés (424 animaux analysés) a montré que près de 25 % d’entre eux étaient porteurs de bactéries multi-résistantes à la sortie de leur hospitalisation. Dans ce centre, l’usage des antibiotiques était pourtant très réduit, et ne pouvait à lui seul expliquer cette prévalence élevée. Par ailleurs, les analyses moléculaires réalisées à partir des bactéries isolées des animaux ont conduit à l’identification d’un nombre très limité de clones bactériens. Les mêmes clones étaient partagés par de multiples individus, démontrant l’existence d’une transmission bactérienne entre oiseaux au sein du centre. Les analyses des structures génétiques mobiles porteuses des gènes de résistances ont montré également que le même plasmide de multi-résistance était identifiable chez des oiseaux différents, là encore indiquant une transmission inter-individuelle de l’antibiorésistance, et en l’absence d’administration de l’antibiotique. Une telle situation résulte bien davantage de défauts de maîtrise de la transmission bactérienne plutôt que d’une antibiothérapie excessive. Des pratiques telles que la maintenance d’animaux compatibles dans les mêmes cages, ou l’absence de désinfection efficace des cages elles-mêmes, ou encore la transmission manuportée de bactéries résistantes par un personnel surchargé travaillant dans des locaux exigus, suffisent à favoriser une telle transmission.
En clinique vétérinaire canine, de telles similitudes entre bactéries multirésistantes pourtant isolées de chiens et/ou de chats différents, sont également observées. Elles signent toutes des évènements de transmissions bactériennes entre animaux non nécessairement exposés aux antibiotiques. On peut citer des épidémies intra-hospitalières de souches de Staphylococcus pseudintermedius résistants à la méticilline [4] ou de E. coli et de Klebsiella pneumoniae résistantes aux céphalosporines de 3e et 4e générations et aux fluoroquinolones [5, 6]. La transmission de plasmides de résistance peut également s’opérer entre animaux domestiques en dehors de contexte de soins, par exemple entre chiens dans des parcs publics, par l’intermédiaire de leurs déjections [7].
Chez les animaux de production également, cette transmission de l’antibiorésistance entre animaux non exposés aux antibiotiques peut être mise en évidence. C’est le cas par exemple entre fermes bovines laitières, à la faveur des nombreuses interactions entre agriculteurs (prêts de matériel agricole, échanges d’animaux, etc.), en lien avec un faible niveau de biosécurité. Cette transmission de l’antibiorésistance survient également en aval des élevages, après le stade de l’abattage des animaux. En effet, c’est l’hypothèse principale permettant d’expliquer que la surface de la viande de poulets au détail ait été contaminée dans plus de 90 % des cas par des bactéries multirésistantes à une époque où la prévalence de ces mêmes bactéries en élevage était résiduelle (2 %). Le facteur d’amplification constaté entre l’abattage et la vente de détail, dans un segment de la chaine alimentaire où l’usage d’antibiotiques post-mortem n’existe évidemment pas, ne peut être lié qu’à des évènements de transmission (dans l’environnement de l’abattoir, entre carcasses de volailles au moment de la découpe, transmission par les manipulateurs, etc.) [8].
Au niveau international, la transmission de l’antibiorésistance joue également un rôle parfois déterminant. C’est ainsi que des pays très vertueux dans l’usage des antibiotiques vétérinaires (la Suède, par exemple), ont néanmoins mesuré des taux de prévalence majeurs (jusqu’à 40 % de résistances aux céphalosporines de 3e et 4e générations dans les filières avicoles (poulets de chair et poules pondeuses)). C’est l’importation de poussins, exposés à l’antibiotique (le ceftiofur), et donc porteurs des bactéries multirésistantes dans leur pays d’origine (Royaume-Uni), qui a conduit ensuite à la diffusion de cette antibiorésistance au sein des filières suédoises [9, 10].
Rappelons enfin que des bactéries multirésistantes sont régulièrement retrouvées chez des oiseaux sauvages [11], par définition non exposés à des traitements antibiotiques, et dont la présence est très probablement liée à une contamination par voie alimentaire sur les lieux de nourrissage. A ce titre, une étude française a clairement montré des différences de colonisation par des bactéries multirésistantes entre deux espèces de goélands, l’une inféodée à son île sans contact avec le continent, l’autre effectuant de nombreux allers-retours entre l’île et le continent [12].
Tous ces éléments montrent qu’en parallèle d’une attention sur la prescription des antibiotiques, un volet tout aussi important de la lutte contre l’antibiorésistance est de maîtriser les circuits de transmissions de bactéries résistantes. En France, des efforts sur la biosécurité en élevage ont été inclus dans les plans Ecoantibio, mais à l’évidence des marges de progrès subsistent, et qui pourraient être renforcées dans un plan Ecoantibio 3. Il conviendrait de mieux identifier et documenter les situations de transmission de l’antibiorésistance au sein des différents secteurs animaux et de la chaine alimentaire, et de renforcer les mesures de prévention et de contrôle de la transmission de l’antibiorésistance dans ces mêmes secteurs.
Conflit d’intérêt
L’auteur n’a aucun conflit d’intérêt à déclarer.




 CC-BY 4.0
CC-BY 4.0