Abridged English version
1 Introduction
The physical conditions of hydrothermal systems are very contrasted between surface and the deep rock. Moreover, the discrepancy between the chemical properties of the fluid and solid phases causes a great chemical activity to get closer to equilibrium conditions. These disequilibrium conditions are present on the HDR (Hot Dry Rock) project for an industrial use of natural fluid circulation and imply mineralogical reactions that can block up the site.
2 The geothermal site of Soultz-sous-Forêts
This site is located in Alsace, France [8]. The deep rock is a fractured granite. A strong local thermal gradient up to 100 °C km−1 is measured in the sedimentary cover [6]. The HDR project has attempted to provide a continuous flow of water between two drillings: cold water (60 °C) is injected towards a deep level of the granite (−5000 m, 200 °C), then flows through the fracture network, and hot water is extracted to the surface for a future economical purpose. The strong thermal gradient and the high water/rock ratio lead to a very dynamic chemical system. Although the mineralogical evolution may be predicted by geochemical codes [10], it can also be investigated through experimental simulations. The originality of the present study lies in experiments conducted under a strong thermal gradient in order to determine the crystallizations that should occur along the fluid pathway.
3 Experimental method
Tube-in-tube experiments of the type described by [14,15] and [17] were conducted at 600 bar for 40 days. A gold capsule was filled with the starting mixtures and placed into a 15-cm long gold tube that contained only pure water. The tube was placed in a horizontal cold sealed vessel [16]. The hot and the cold extremities of the tube were respectively at 300 and 200 °C (Fig. 1). Starting mixtures representing different granite compositions were used (Tables 1 and 2). At the end of the run, quench from 300 °C to room temperature was achieved in 5 min, using a compressed air jet. The tube was cut longitudinally and the internal walls were observed with a SEM (JEOL JSM 840 with EDS) and a STEM (Philips CM12 with EDS) to detect and analyse the minerals having crystallized along the thermal profile. When enough material was available, the newly formed minerals were collected for XRD.

Position du gradient thermique imposé au cours des expériences par rapport au tube et à la capsule. Le tube représente le milieu réactionnel fermé dans lequel se produisent les cristallisations. La capsule, isolée dans le tube à son extrémité chaude, contient les produits de départ et représente le terme source de matière.
Representation of the tube-in-tube design, and temperature profile along the tube. The tube represents the reaction area where crystallizations can occur. The capsule placed at the hot extremity of the tube contains the starting products and represents the source of matter.
Conditions expérimentales et composition des mélanges de départ
Experimental conditions and composition of the starting products
| Nom du tube | Conditions P, T | Mélange initial | Durée de l'expérience |
| Proportions (en % moles) | |||
| MEL 1 | P : 600 bar | Qtz, F K, Ab | 40 jours |
| T (au point chaud) : 300 °C | |||
| GRAN 4 | P : 600 bar | Broyat de granite (1) | 40 jours |
| T (au point chaud) : 300 °C | Cf. Tableau 2 |
Compositions chimiques comparées des granites de Soultz et de Flamanville
Chemical compositions of Soultz granite compared to Flamanville granite
| Oxydes (% poids) | Granite de Flamanville (1) | Granite de Soultz (2) | Écart |
| SiO2 | 69,24 | 68,95 | 0,42% |
| TiO2 | 0,48 | 0,51 | 5,88% |
| Al2O3 | 15,29 | 15,06 | 1,53% |
| Fe2O3t | 3,36 | 3,03 | 10,89% |
| MnO | 0,04 | 0,07 | 42,86% |
| MgO | 0,40 | 1,25 | 68,00% |
| CaO | 2,41 | 2,24 | 7,69% |
| Na2O | 4,59 | 4,13 | 11,14% |
| K2O | 3,89 | 4,57 | 14,88% |
| P2O5 | 0,30 | 0,19 | 57,89% |
| Moyenne pondérée de l'écart | 2,95% |
4 Results
The capsules were still filled at the end of the runs, and a significant amount of newly formed minerals are observed at the cold extremity of the tube, which indicates a fast transport of matter by diffusion from the hot to the cold extremity (Fig. 2).

Photographie au microscope électronique à balayage (MEB) de l'intérieur du tube MEL 1 à son point froid, montrant la quantité de matière néoformée.
Scanning electron photograph of the inside walls at the cold extremity of the tube MEL 1, showing the quantity of matter produced.
A similar spatial distribution of the newly formed phases with regard to temperature was observed in both runs, i.e. from the hot to the cold extremity: quartz + K-feldspar ± plagioclase ± Mg-rich saponites; quartz + K-feldspar + plagioclase; and alkaline or Ca-rich clays + quartz ± plagioclase. The cation composition of the phyllosilicates is also reproducible: Mg-rich clays crystallize at the hot extremity of the tube, and Ca or alkaline-rich clays crystallize at the cold extremity.
In the run MEL 1, the proportion of quartz relative to other secondary minerals increases from the hot to the cold extremity, whereas the proportion of K-feldspar decreases: it is gradually overgrown by Na and K-rich clays towards the cold extremity. Albite is totally overgrown by clays at the cold extremity. These clays fill the entire volume of the cold point (Figs. 4–6). Fig. 4 shows that these clays are interstratified minerals (20.7 and 14.5 Å). They are probably, according to DRX (Fig. 4) and chemical compositions (Fig. 5), composed by mica and smectite layers, with about 80% smectite.
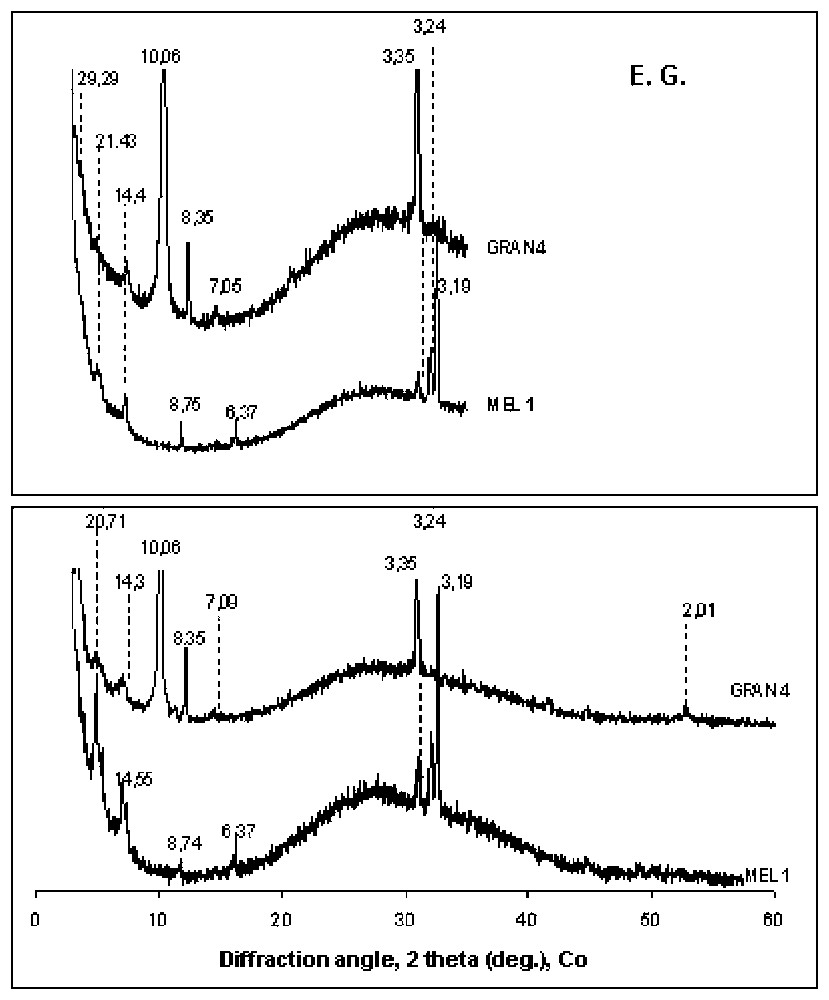
Diagrammes de diffraction aux rayons X des phases néoformées aux points froids de GRAN 4 et MEL 1 (avant – diagrammes supérieurs – et après – diagrammes inférieurs – traitement à l'éthylène glycol). Les pics sont indexés de la valeur de d, exprimée en Å.
XRD patterns of newly formed minerals at the cold extremity of GRAN 4 and MEL 1 (before (lower) and after (upper) ethylene glycol treatment). Peaks are labeled with d values, in Å.
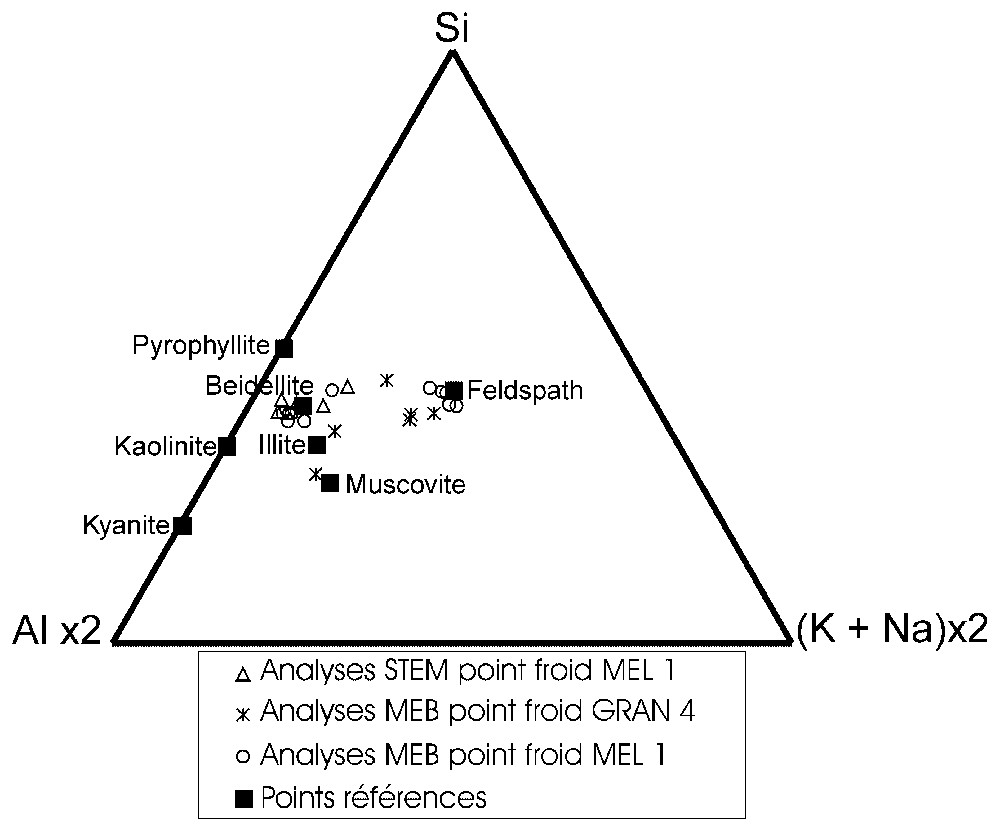
Compositions chimiques au STEM et au MEB des phases ayant cristallisé au point froid des tubes MEL 1 et GRAN 4. Les carrés pleins représentent des compositions de minéraux théoriques servant de références.
SEM and STEM chemical compositions of the newly formed minerals at the cold extremity of the tubes MEL 1 and GRAN 4. Replete squares are index minerals.

Répartition schématique des minéraux secondaires le long du tube MEL 1.
Schematic representation of the location of the newly formed products along the tube MEL 1.
The same type of evolution is evidenced in the run GRAN 4 (Fig. 7): quartz and K-feldspar are present all along the tube, and their proportion decreases with the decreasing temperature. A mica of intermediate composition between illite and muscovite crystallizes at the hot extremity. The proportion of plagioclases increases towards the cold extremity, up to 210 °C. Clays are the most abundant phase at the cold extremity (Figs. 4 and 5). Fig. 4 shows that these clays are interstratified minerals, with a structure close to those found in experience MEL 1.
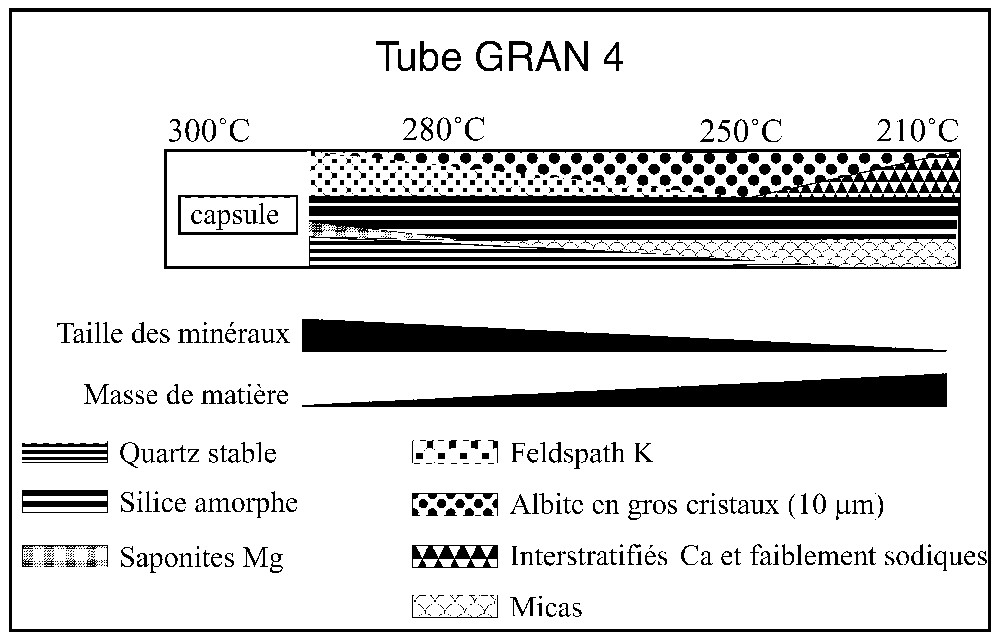
Répartition schématique des minéraux secondaires dans le tube GRAN 4.
Schematic representation of the location of the newly formed products along the tube GRAN 4.
5 Discussion and conclusion
The tube-in-tube experimental method is very successful to determine the sequence of secondary crystallizations versus temperature in a chosen chemical system. Chemical reactions occur quickly and material transport is efficient. Similar sequences of crystallization were observed in both experiments, suggesting that the transitions between phases are not only under the control of the composition of the solution, but also under thermal control.
The observed crystallization parageneses contain a significant amount of feldspars. Although feldspars are not considered to crystallize in the numerical simulations [5,11], our experimental results suggest that the crystallization of clay minerals is controlled by the previous crystallization of feldspars. Therefore, feldspars should play an important controlling role on the evolution of the mineralogy of the HDR site.
Moreover, we see dissolution evidences on some newly formed quartz and some feldspars are overgrown by clays (Fig. 3). These observations suggest that we observe temporary steps of mineralogy, but not a thermodynamic equilibrium. Each extent of the tube represents a local equilibrium that evolves with time, in relation with the local equilibrium close to it.



Photographies au MEB des phases du tube MEL 1. (a) Principales phases néoformées: Qtz, quartz; Ab, albite; Fd K, feldspath potassique. (b) Quartz présentant des figures de dissolution. (c). Remplacement d'un feldspath par des argiles alcalines.
Scanning electron micrographs of minerals that crystallize in the tube MEL 1. (a) Main newly formed phases : Qtz, quartz ; Ab, albite ; Fd K, K-feldspar. (b) Quartz in course of dissolution. (c) Feldspar replaced by alkaline clays.
The crystallization of more aluminous-rich phases at the cold extremity of the tube indicates that aluminium is a mobile element over 200 °C in dilute water. This observation agrees with similar ones [1,2,4,18], which suggests that the solubility of aluminium is controlled by the formation of a KAl(OH)4 complex. In any case, aluminium conservative models are not suitable to calculate the mineralogical evolution and the mass-transfer balance in the HDR system.
1 Introduction
La circulation d'un fluide dans une roche, à haute température et sous gradient thermique, crée des réactions de dissolution et précipitation de multiples minéraux [6,13]. L'importance et la nature de ces interactions doivent être déterminées afin de prévoir la pérennité du site ou l'éventuel colmatage des fractures permettant le passage du fluide et ainsi le risque de blocage du site. La cristallisation éventuelle d'argiles, en particulier, peut poser problème.
2 Le contexte du site géothermique de Soultz-sous-Forêts
Soultz-sous-Forêts se situe sur la bordure ouest du graben du Rhin, au nord de Strasbourg (France) [8]. Sur ce site se développe un projet géothermique européen de type « roche chaude sèche ».
Cette situation est intéressante pour un projet de géothermie : la roche réservoir est un granite hercynien sous couverture (triasique à tertiaire) présentant une forte fracturation. Le gradient géothermique est important localement dans la couverture sédimentaire (jusqu'à 100 °C km−1), puis, dans le socle, de 28 °C km−1.
Le concept de « roche chaude sèche » consiste à établir une circulation fluide entre deux forages d'un doublet en injectant une eau froide dans le premier forage [7]. Par une circulation forcée en profondeur à travers la zone chaude et fracturée, l'eau se réchauffe par transfert thermique. Elle parvient chaude au second forage, puis remonte à la surface, où son énergie calorifique peut être utilisée. Cette circulation a été testée en 1997 par des traceurs, qui ont mis en évidence l'existence d'une boucle de circulation, qui est restée stable au cours des quatre mois de l'expérimentation [9]. Le fort gradient thermique (l'eau passe de 65 °C en surface à 200 °C à 5000 m de profondeur), les grandes surfaces réactionnelles et un grand rapport eau/roche permettent un fort dynamisme chimique de ce système, comme le montrent les minéralisations secondaires nombreuses déjà décrites [7,10,13]. C'est afin d'identifier ces phénomènes de dissolution–précipitation dans un gradient thermique lors d'injection de fluides que nous avons entrepris les expériences décrites ci-après.
3 Méthodes expérimentales
3.1 Produits de départ
Deux mélanges différents ont été préparés à partir de broyats de minéraux naturels ou de roche (Tableau 1). Ces broyats maximisent les échanges eau–roche par rapport au système naturel. Le mélange appelé MEL 1 respecte les proportions relatives des minéraux clairs dans le granite sain de Soultz [10]. Le mélange GRAN 4 a été obtenu par broyage très fin d'un granite de Flamanville, dont l'analyse chimique globale est comparable à celle du granite sain de Soultz (Tableau 2).
3.2 Mise en route des expériences
0,17 à 0,21 g de mélanges de départ ont été placés dans une capsule cylindrique en or, elle-même placée à l'intérieur d'un tube en or de diamètre plus important et de 15 cm de longueur [14,15,17]. Afin de permettre les échanges ioniques entre le mélange réactionnel situé dans la capsule et l'intérieur du grand tube, la capsule est perforée par de très petits trous permettant le passage des ions en solution, mais pas celui des solides. La capsule mise en place, le tube est rempli par 1,5 g d'eau distillée (cas d'un fluide injecté), puis soudé à l'arc. Les tubes sont placés dans des autoclaves à joints froids horizontaux du type décrit par Tuttle [16]. Le profil de température le long du tube expérimental est indiqué sur la Fig. 1 ; le point chaud est toujours à 300 °C. La mesure du gradient thermique est effectuée par des thermocouples que l'on dispose le long de l'enceinte du four [14,16]. La vitesse de chauffe de 30 °C min−1 est suffisamment rapide pour empêcher la cristallisation de phases pendant la montée en température. Le Tableau 1 récapitule les conditions expérimentales pour chaque tube.
Après l'expérience, la température est brutalement diminuée en 3 min par circulation d'air comprimé jusqu'à 60 °C. L'autoclave est démonté puis refroidi à 10 °C par immersion dans l'eau froide. Le tube est ensuite sorti de l'autoclave et plongé dans l'azote liquide avant d'être coupé en morceaux. Les parois internes des tubes MEL 1 et GRAN 4 sont observées au MEB (JEOL JSM 840 + EDS) et STEM (Philips CM12, avec modèle de Cliff–Lorimer + EDS). Lorsque la quantité de matière était suffisante, on a effectué des analyses par diffraction des rayons X.
4 Résultats
Les parois des tubes sont tapissées de cristaux sur presque toute leur longueur. Cependant, la quantité de matière est plus importante au point froid (Fig. 2). Dans tous les cas, la capsule après expérience contient encore une grande partie du mélange de départ.
4.1 Les cristallisations secondaires dans le tube MEL 1
Ces observations ont été effectuées au microscope électronique à balayage. Les minéraux présents en plus grande quantité sont l'albite, le quartz, le feldspath potassique et les minéraux argileux (Fig. 3a). On observe une séquence de répartition de ces minéraux, ainsi qu'une variation de leur taille et de leur forme le long du tube.
Le quartz est toujours présent sous la forme de gros cristaux de 10 μm, dont l'abondance augmente en allant vers le point froid (Fig. 4 : pic à 3,34 Å). De 6 à 11 cm du point chaud (c'est-à-dire de 280 à 240 °C), il présente de nettes figures de dissolution (Fig. 3b).
Le feldspath potassique est présent tout le long du tube (Fig. 4 : pic à 3,24 Å). Toutefois, sa proportion par rapport aux autres minéraux diminue en allant vers le point froid. Cette diminution de la proportion de feldspath s'explique par son remplacement, à partir de 10 cm (c'est-à-dire à partir de 250 °C), par des argiles potassiques. La Fig. 3c montre ce remplacement à l'extrémité froide du tube.
L'albite est présente presque tout le long du tube (Fig. 4 : pic à 3,19 Å). De 300 à 245 °C, elle apparaı̂t sous la forme de gros cristaux de plusieurs dizaines de microns de côté. Puis jusqu'à 210 °C, elle se présente sous la forme de petits cristaux d'un micron de côté, disposés en tapis contre la paroi du tube. À l'extrémité distale du tube, l'albite est, comme le feldspath potassique, remplacée par des argiles NaK.
Les argiles tapissent les parois de l'extrémité froide du tube (Figs. 4 et 5). Par-dessus celles-ci cristallisent des cristaux de feldspath et d'albite, qui sont partiellement remplacés par des argiles NaK de petite taille. Il semble donc que nous soyons en présence d'une histoire polyphasée. La Fig. 4 montre que les argiles présentes sont des interstratifiés à grande périodicité (pic à 20,7 Å). Les pics observés (20,7 et 14,5 Å) pourraient faire penser à de la corrensite ou à un interstratifié contenant de la vermiculite, mais l'absence de magnésium dans cette expérience exclut ces possibilités. Ces pics pourraient alors, en accord avec la chimie globale de ces particules argileuses présentées sur la Fig. 5, être des interstratifiés de mica et de smectite, avec environ 80 % de smectite, un minéral qui serait ainsi intermédiaire entre la rectorite et la beidellite. Les feuillets composant cet interstratifié doivent être peu remplis en cations interfoliaires pour expliquer le très faible décalage observé après traitement à l'éthylène glycol. La Fig. 6 récapitule l'ensemble des cristallisations secondaires.
4.2 Les cristallisations secondaires dans le tube GRAN 4
On retrouve dans ce tube les minéraux néoformés dans le tube MEL 1. Le quartz, le feldspath potassique et le plagioclase (de composition intermédiaire entre l'albite et l'anorthite) sont présents sur presque toute la longueur du tube. La proportion du plagioclase augmente dans la section soumise à une température allant de 290 à 250 °C, puis diminue jusqu'à être nulle à partir de 210±5 °C. La quantité de feldspath potassique et de quartz diminue vers le point froid. Contrairement à ce qui est observé lors de l'expérience MEL 1, les feldspaths ne sont ici pas déstabilisés en argiles.
Les parois du tube sont recouvertes par un tapis de micas (Fig. 4 : pic à 10,06 Å), de composition intermédiaire entre illite et muscovite (Tableau 3).
Composition des micas ayant cristallisé sur les parois des tubes
Chemical compositions of the newly formed micas
| Expérience | Position | Phase | Formules structurales moyennes |
| calculées à partir des points de la Fig. 5 | |||
| GRAN 4 | Point froid | Micas (composition illitique) | Si7,09Al0,91Al4(K)0,91O20(OH)4 |
| GRAN 4 | Point chaud | Mica intermédiaire | Si6,2Al1,8Al4(K)1,8O20(OH)4 |
Les argiles sont présentes à l'extrémité froide du tube (Figs. 4 et 5). Elles sont calciques, avec un faible remplissage sodique. La diffraction des rayons X (Fig. 4) montre que ces argiles sont des interstratifiés très proches en structure de ceux qui ont cristallisé dans l'expérience MEL 1. À l'extrémité chaude, on observe également la présence de saponites magnésiennes. Nous avons également noté la présence importante de silice amorphe tout le long du tube, sous les formes variées de fibres, de craquelures ou de petites boules. La répartition des cristallisations secondaires le long du tube est présentée sur la Fig. 7.
5 Discussion et conclusion
5.1 Répartition des minéraux secondaires en fonction de la température
Les transferts de matière en solution observés dans les expériences ont été significatifs et rapides : nous observons des cristallisations plus importantes sur des temps plus courts que dans des expérimentations similaires précédentes [14,15,17,18]. Cela est remarquable, car les expériences menées dans ces études étaient faites entre 300 et 550 °C, alors que nous avons travaillé entre 200 et 300 °C. Nous montrons que les expériences sous gradient de température dans des conditions de relative basse température permettent de proposer des séquences probables de cristallisation en fonction de la température. Les réactions se font dans ces systèmes expérimentaux de façon rapide et la diffusion agit sur de grandes distances.
Les séquences de cristallisation sont similaires dans les deux expériences conduites avec des mélanges de départ différents (avec ou sans minéraux ferromagnésiens). Cela suggère que la répartition des minéraux reflète non seulement les conditions de saturation de la solution, mais aussi la stabilité thermique relative des minéraux secondaires, c'est-à-dire du point chaud vers le point froid : quartz + feldspath potassique (± plagioclase ± saponites) ; quartz ± feldspath potassique + plagioclase ; enfin argiles + quartz ± plagioclase. Les phyllosilicates les plus magnésiens cristallisent au point chaud, puis les phyllosilicates potassiques, sodiques et enfin les phyllosilicates ayant une composition majoritairement calcique au point froid. On trouve donc une tendance répétée à concentrer les phases magnésiennes au point chaud et les phases calciques au point froid, et une mobilité relative des éléments de type : Si>Na, Ca>Al>Mg, comme on l'a vu dans d'autres études [3].
La séquence de cristallisation observée montre une prépondérance volumique des cristallisations secondaires de feldspaths. Or, dans la plupart des modélisations d'interactions eau–roche du réservoir profond du site de Soultz, ces phases ne sont pas prises en compte [5]. Il a été calculé que les phases arrivant à saturation sont les phyllosilicates (illites et smectites) et le quartz [11], le fluide étant sous-saturé par rapport au feldspath durant toute la descente en température vers la surface et dans l'échangeur thermique. Pourtant, nos résultats expérimentaux indiquent que le feldspath potassique cristallise dans les premiers stades de la descente en température. Ces résultats expérimentaux indiquent un contrôle des feldspaths sur la cristallisation des diverses argiles, et donc sur l'évolution minéralogique et la pérennité des chemins de circulation fluide dans le granite de Soultz.
Certains modèles tiennent compte de la cristallisation des feldspaths [12] et montrent l'importance des successions de cristallisations–dissolutions des phases néoformées. On peut voir dans ces études une vision dynamique de ces équilibres successifs, mais ils sont abordés en fonction de l'avancement de réaction uniquement, à température constante. Il reste donc à introduire l'influence du gradient thermique dans l'espace sur l'existence de cette dynamique complexe.
5.2 Polyphasage et état d'équilibre
Par ailleurs, nous observons un polyphasage et des cristallisations secondaires successives dans les expériences (les feldspaths sont déstabilisés au profit des argiles, les quartz néoformés présentent des figures de dissolution). Ceci nous montre que nous observons probablement des états minéralogiques transitoires, et non un état thermodynamiquement stable. Chaque longueur unitaire du tube expérimental représente un équilibre local, qui évolue dans le temps en fonction des équilibres locaux voisins.
Or, les modèles peuvent rendre compte d'un état de saturation de la solution vis-à-vis des phases minérales et ainsi prévoir la cristallisation ou la dissolution de celles-ci, mais ils ne sont pas capables de prendre en compte un système évoluant à la fois par étapes temporelles et spatiales et précipitant des phases intermédiaires métastables. En l'absence de modèles thermodynamiques et cinétiques intégrant les processus de type dissolution–transport–cristallisation, les expériences présentées sont nécessaires pour discuter de l'évolution du site HDR pendant le régime transitoire.
5.3 Implications sur le transport de l'aluminium en solution
Ces expériences montrent que les phases qui cristallisent au point froid sont plus alumineuses que celles qui cristallisent au point chaud. L'aluminium est donc un élément mobile en solution diluée, même à relativement basse température. La présence concomitante d'alcalins au point froid permet de souligner l'importance probable des complexes aluminium–alcalins (KAl(OH)4 ou NaAl(OH)4) dans ce phénomène de transport de l'aluminium [1,2,4,18]. Au point chaud du tube, ce complexe se forme facilement, diffuse en solution (grâce au gradient de potentiel chimique présent dans le tube), tandis qu'au point froid une grande partie des complexes se dissocient sous des formes (Al(OH)4−+K+) qui participent à la cristallisation de phases alumineuses [4].
Associé aux alcalins, l'aluminium montre une grande mobilité dans ce type de système hydrothermal et permet la cristallisation de phyllosilicates alumineux éloignés des termes sources.
Remerciements
Les auteurs remercient Nicole Catel (ENS, Paris) pour ses préparations et ses mesures, ainsi que Nicolas Geoffroy (LGIT, Grenoble). Cette note constitue la contribution EOST n∘ 2002.406-UMR7517.



