1. Introduction: meeting Michel Caboche
Towards the end of my postdoctoral stay in the United States, I started looking for a position in France to join my partner, who was employed at the Pasteur Institute in Paris. I was intrigued by the work of the team of Michel Caboche on the use of genetics in the study of nitrogen assimilation [1, 2], which I found very innovative and inspiring since it used concepts and approaches borrowed from genetics in yeast or animal systems to study the mechanisms underlying nitrogen use efficiency, a topic so important for agriculture in particular in the context of the ever more pressing need to reduce fertilizer use.
I contacted him and he invited me to visit the Cell Biology Laboratory at the INRA (the institute was renamed INRAE in 2020) center in Versailles. There, I was very surprised to meet one of the most famous French plant scientists in a miniscule office, next to the toilet, under the roof of the building, with barely enough room to accommodate a visitor! Fortunately, this did not prevent our exchanges from being very friendly and interesting and as a result he offered me the chance to join his team and INRA in 1992 as a young “chargé de recherche”. I was immediately struck by the hospitality of my new colleagues and the stimulating atmosphere of cooperation and benevolence that reigned in the laboratory, inspired by the charismatic director at the time, Jean Pierre Bourgin.
Being part of a young and ebullient team under Michel Caboche’s direction, we had the ambitious goal to use the emerging model plant Arabidopsis thaliana to investigate how plants grow and develop, with the ultimate goal to use this knowledge for crop improvement. Our vision on the societal interest of our research, expressed in the refrain of a song that we wrote in 1996 to celebrate the opening of a new extension of the laboratory, may seem rather naive with today’s hindsight.
« Arabidopsis, donne-moi tes secrets,
Arabidopsis, on en fera un brevet,
avec tes gènes si facilement clonés,
on améliore colza et peuplier »
(“Arabidopsis, give me your secrets, Arabidopsis, we will use them for a patent, with your genes so easily cloned, we will improve oilseed rape and poplar”). The passage of José Bové and his friends and the concomitant change in the public perception on plant biotechnology, sadly has prevented us from realizing all our youthful dreams.
2. Arabidopsis molecular genetics
One of the first actions inspired by Michel Caboche, and led by my colleague Catherine Bellini, was to perform an EMS screen for developmental mutants [3]. The initial idea was to identify critical components of the signaling pathway of the key growth regulator auxin, by screening for mutants that showed growth defects at the seedling stage. The screen yielded a large number of mutants, many of which turned out to have altered cell walls. In this way, by following the genetics we made an involuntary dive into the intricacies of the plant wall.
In retrospect, it is not so surprising that so many mutants with developmental defects were affected in the establishment of the wall. Indeed, the crux of plant morphogenesis is the ability to generate flat solar panels with minimal metabolic cost. The trick that plants have found, is the adoption of a hydrostatic skeleton, with liquid-filled vacuoles in pressurized cells, surrounded by a wall strong enough to resist the forces generated by this pressure [4]. This wall consists for 90% of carbohydrates, an abundant and readily available raw material for photosynthetic organisms [5]. Later during development, secondary growth can give rise to specialized load-bearing structures (e.g., trunks and branches) in which the walls immobilize and become themselves carriers independently from the hydrostatic pressure of the cells.
We focus here on the walls of growing cells, or primary walls. The use of a hydrostatic skeleton imposes a major constraint on the cells of plants, but also of other walled organisms such as bacteria and fungi: they need to expand while maintaining the integrity of their walls [6]. This has become the main focus of our research.
Before discussing our work, I will first give a short reminder on the composition and architecture of the primary wall. It consists for about 60% of water, so the dry matter is extremely concentrated, and the polymers are in a semi-solid state, which complicates the biochemical processes in this compartment [7]. Cellulose is found in the form of microfibrils with a diameter of about 3 nm, which form the load-bearing network of the wall. There is also a matrix of hemicelluloses, polymers that carry branches, which prevent their association into crystalline structures, and pectins, a set of negatively charged galacturonic acid (GalA)-containing polymers. Finally, primary walls contain small amounts (about 10% in Arabidopsis leaves) of proteins. The wall polymers form a network through covalent and non-covalent bonds. At the time of our screen, virtually nothing was known about wall biosynthesis. Not a single cell wall biosynthetic enzyme had been isolated or cloned [8]. A real terra incognita at a biochemical and genetic level.
Fourier Transform InfraRed spectroscopy-based classification of Arabidopsis cell wall mutants [9, 10]. (A) Dark-grown seedling, the square indicates the zone from which the spectra were obtained. (B) Average FTIR spectra (n = 20) from wild type (red line) and mutant (white line) hypocotyl cell walls. (C) Cluster analysis of FTIR spectra. Colors refer to mutant loci for which several alleles were analyzed. Note the clustering of alleles, but also the clustering of mutants affected in cellulose synthesis (rsw1-2, kor-2, kob1-1, kob1-2, pom1 alleles, rsw1-10, pom1-21, prc1 alleles, kor-1 and rsw2-3) with wild type plants treated with cellulose synthesis inhibitors DCB or isoxaben (isox), the clustering of mutants with altered microtubules (ton1-1, bot1 alleles and sab) with wild type treated with the microtubule inhibitor oryzalin (brassinosteroid mutant det2 also has altered microtubules [11]), and mutants with altered pectins (qua1 and qua2 alleles and pme3, pme32 and pme34 mutants). Panel (C) is adapted from [12].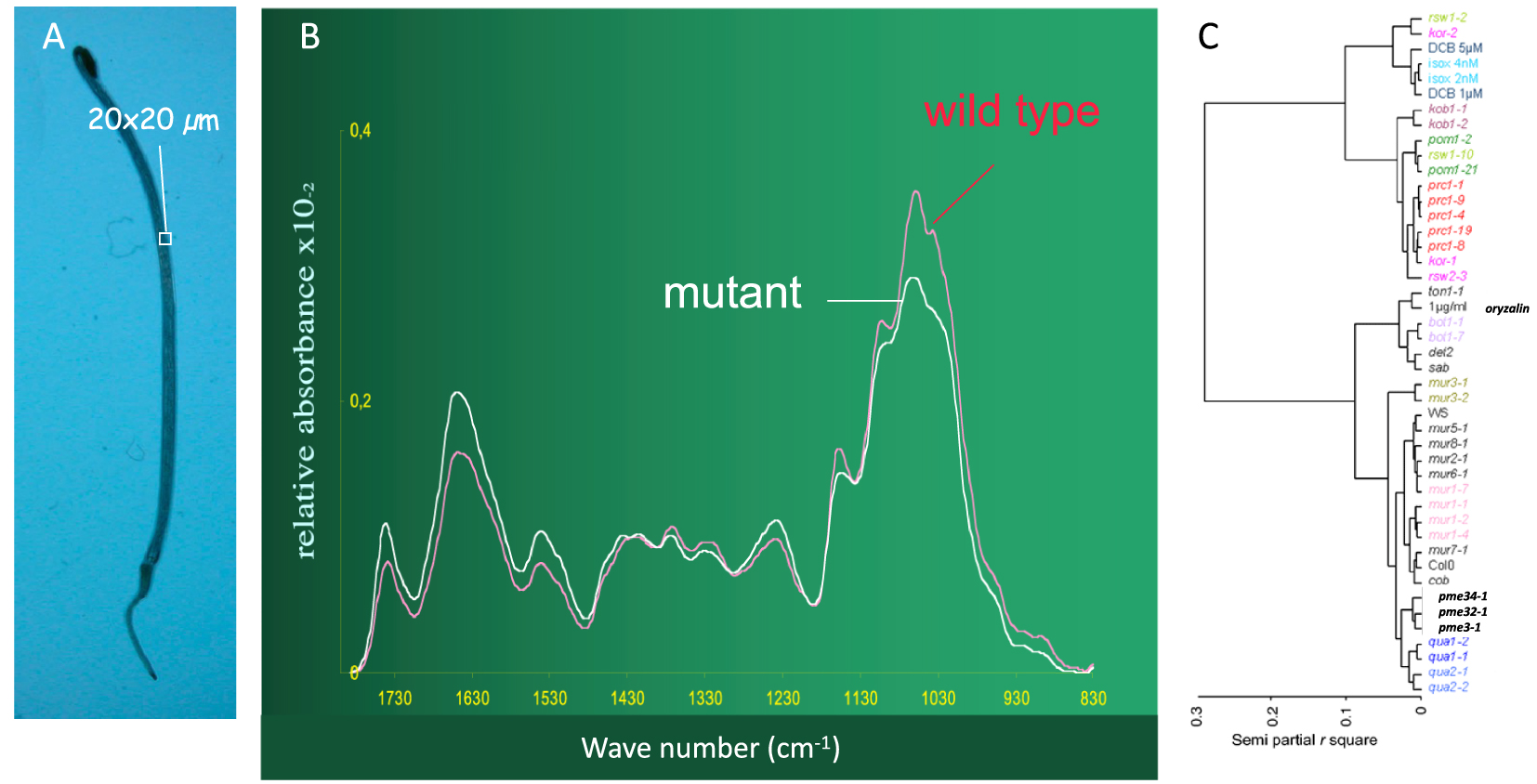
So, we isolated a large number of mutants with a short hypocotyl, the embryonic stem of the seedling. To see more clearly in this large collection of mutants, Gregory Mouille, in the team, developed a secondary screening method based on Fourier transform infrared spectroscopy, coupled to a microscope (Figure 1) [9]. Transmission infrared spectra, which essentially reflect the composition of the walls, were obtained from a window of about 20 × 20 μm of the dried hypocotyl. These spectra are difficult to interpret because of the superposition of absorbances of a multitude of chemical bonds. The FTIR profiles however, allowed an extremely accurate classification of the cell wall mutants, as we were able to show thanks to a fruitful collaboration with Stephane Robin, an expert in applied mathematics [10]. Indeed, when including several independent alleles for the same gene, we almost always observed that these alleles were grouped together, even when compared with alleles for other related genes with very similar macroscopic phenotypes. The clustering of unknown mutants with already characterized mutants or with wild type seedlings treated with specific inhibitors allowed hypotheses about the underlying genetic defects to be formulated, based on a “guilt by association” reasoning (Figure 1).
Structure and motility in plasma membrane of cellulose synthase complex (CSC). (A) Hexameric CSC in the inner leaflet of the plasma membrane shown by freeze-fracture TEM (from [13] with permission). (B) Top view of the 3D structure of a catalytic subunit trimer forming one of the 6 globules of the CSC. Glucan chains within the transmembrane channel are shown in white, yellow and orange. (C,D) Spinning disc microscopy on epidermis cells of dark-grown Arabidopsis hypocotyl, reveals GFP-labeled CESA3 punctae in rows in the plasma membrane and in Golgi bodies (larger doughnut shaped structures) (C), a time projection (10 min) shows the linear trajectories of the CSCs in the plasma membrane (D). Scalebar = 10 μm in (C,D).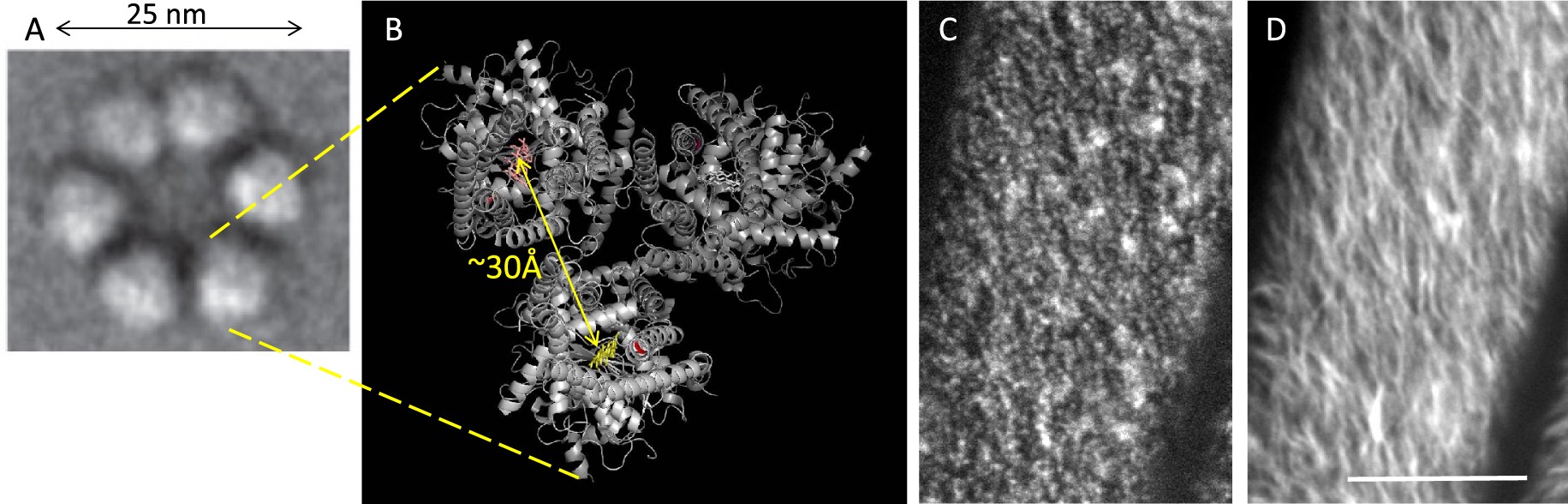
3. Cellulose synthesis
We thus found a large number of mutants clustering with wild type plants treated with cellulose synthesis inhibitors (Figure 1) [9]. Among these mutants, molecular analysis later identified 3 causative genes, which, based on the sequence similarity with bacterial cellulose synthases, were thought to encode distinct catalytic subunits (CESA1, 3 and 6) of the cellulose synthase complex [14, 15]. This Cellulose Synthase Complex (CSC) was shown to correspond to the 25 nm diameter hexameric structures, called “rosettes”, that can be observed in the freeze-fractured plasma membrane of many plant cells (Figure 2) [16]. The next major breakthrough in this field was the 3D structure determination of the cellulose synthase by the group of Jochem Zimmer, first from bacteria using X-ray crystallography [17] and later from plants, using Cryo-TEM of a trimer of identical catalytic subunits from poplar [18]. This provided insights into the reaction mechanism underlying the generation, from UDP-Glc, of a polymer with alternating glycosidic bonds, typical for the β(1–>4)-linked polysaccharides. It showed the presence of an anhydrous channel in each catalytic subunit, harboring a chain of 18 Glc residues on their way to the surface [17]. It also provided information on the mode of action of cellulose synthesis inhibitors and it confirmed the presence of three catalytic subunits in each globule of the hexameric complex (Figure 2B) [18, 19]. Assuming that one CSC produces an elementary microfibril, the association of 18 catalytic subunits implies the presence of 18 glucan chains in a typical microfibril, which is consistent with structural studies using solid state NMR [13]. Another spectacular consequence of these genetic studies was the ability to visualize fluorescently-tagged CSCs in living cells using spinning disc confocal microscopy (Figure 2C,D) [14, 20, 21]. This revealed the presence of hundreds of plasma membrane-associated CSCs, that migrate in two directions along cortical microtubules propelled by the polymerization of the glucan chains, where the observed velocity of around 300 nm/min corresponds to a synthesis rate of 10 residues/second per chain. Further live cell imaging studies and mutant analysis revealed the complexity of the cell biology of cellulose synthesis, with complex post-translational modifications of CSC components, with the CSCs cycling between Golgi bodies, the trans-Golgi network (which dissociates from the Golgi bodies in plant cells), a specialized microtubule-associated recycling compartment [21, 22] and the plasma membrane [16]. This allows temporary retrieval of the CSCs into the recycling compartments in response to environmental stresses that affect the cell wall such as salt or osmotic stress [23]. The screens also yielded a number of genes encoding other components of this multiprotein complex among which a member of the endo-(1–>4)-β-glucanase family (KORRIGAN, KOR) [24], Golgi localized CESA-binding proteins, bifunctional proteins that bind to both CESAs and microtubules, which contribute to guiding the complexes or mediate their stress-induced internalization, combined with the depolymerization of microtubules [16]. Finally, the observation of the microtubule–cellulose connection has nurtured new models for morphogenesis, where microtubules orient along stress patterns in tissues through a so far poorly characterized mechano-sensing pathway, which in turn reinforce the tissues along the main stresses, through the orientation of deposition patterns of load-bearing cellulose [25].
Despite considerable progress in our understanding of cellulose synthesis, many open questions remain. A few examples: How is the membrane insertion, activation and retrieval of CSCs regulated? How can such a large (>25 nm diameter) complex fit into ∼30 nm diameter secretory or clathrin-coated endocytotic vesicles [26], or do we have specialized larger secretory/endocytotic compartments? What is the role of the large number of fatty acid groups that are covalently attached to the complex [27]? How is cellulose synthesis coordinated with the accumulation of matrix polymers? How are the CSCs disconnected from the cell wall during their internalization? What is the role in cellulose synthesis of the cellulase KOR, the Glycosylphosphatidylinositol-anchored protein COBRA, the chitinase-like protein POMPOM1 and several Golgi-associated proteins [16]? What controls the formation of load-bearing cellulose–cellulose crosslinks in the cell wall [28]? How are the cellulose deposition patterns regulated, for instance the successive lamellae in poly-lamellate walls [29] or the, often remarkable, secondary cell wall patterns and finally how are stress patterns sensed to orient the microtubules [30]?
4. Pectins and cell expansion
Another class of FTIR-clustered cell wall mutants, christened quasimodo1 and 2, based on their crooked phenotype, with many cells coming apart from their neighbors, showed changes in pectin content (Figure 3) [31, 32]. Pectins are complex charged multiblock polymers, characterized by the presence of galacturonic acid (GalA) [33]. qua1 and 2 showed reduced levels of homogalacturonan (HG), which is an abundant (up to 50% of the cell wall content) linear pectic polymer of α(1–>4)-linked GalA (Figure 4A). Molecular and biochemical analysis revealed that QUASIMODO1 and 2 encode Golgi-localized GalA- and methyl-transferases, respectively [33, 34]. Indeed, HG is synthesized in Golgi bodies in a highly methylesterified and hence uncharged form. Upon secretion the polymer can be de-methylesterifed by Pectin Methyl Esterases (PMEs) in the cell wall [35], thus exposing the negative charges of the carboxyl groups (Figure 4B). PMEs are encoded by large gene families (66 members in Arabidopsis) and are controlled by endogenous PME inhibitors (PMEIs) encoded by equally large gene families. Different PME activities have been identified, some are processive, generating stretches of de-methylesteried residues, others are non-processive (Figure 4B) [35]. It is not known whether the latter activities act only randomly or whether they also can generate specific de-methylesterification patterns [36]. In hindsight it is easy to understand why plants put so much effort in controlling the de-methylesterification of HG. Indeed, polymer physics tells us that the charge distribution of a polymer has a dramatic influence on its physico-chemical properties. We have here to do with so called “active soft matter”, that can be defined as “soft matter systems that contain self-propelled (or active) constituents that engender emergent dynamic properties at a higher scale”. These emergent properties in this case can be changes in viscosity, phase separation or even movement as we will discuss in the next section [36].
Connecting spatial scales: pectin content and cell-cell adhesion. Z-projections of confocal stacks from propidium iodide-stained, 4-day-old dark-grown wild type and mutant hypocotyls. qua2-1 has 50% reduction in HG content and show reduced cell adhesion. Loss of function mutation esmd1 suppresses the cell adhesion phenotype without changing the HG content, suggesting that the cell adhesion defect is not a direct result of the HG defect. Scale bars = 75 μm. Adapted from [37] with permission.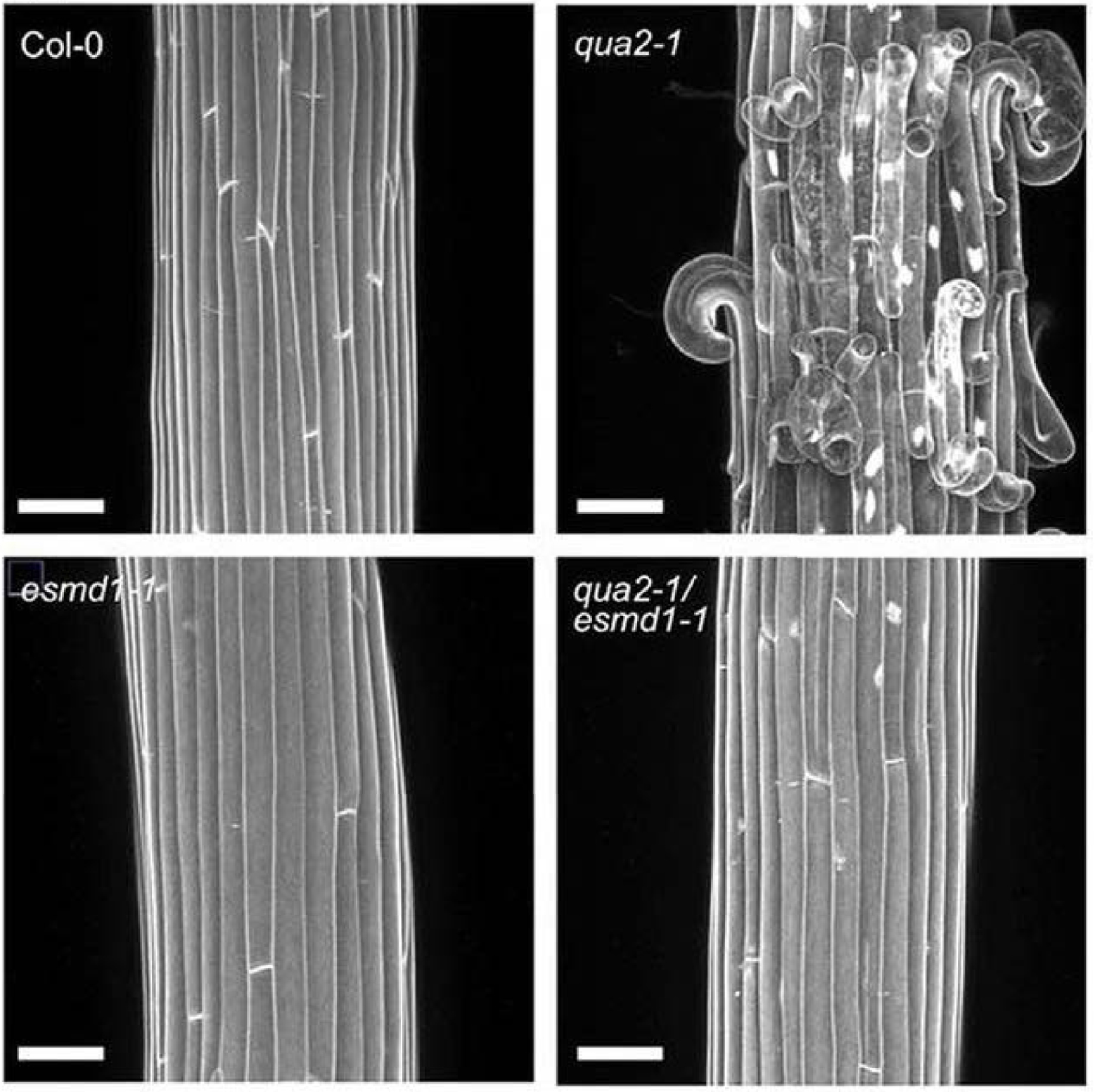
The metabolism of the pectic polymer homogalacturonan (HG) plays a key role in plant growth and morphogenesis. (A) Dimer of α(1–>4)-linked methyl-galacturonic acid (meGalA, red spheres in B) and GalA (green spheres in B). (B) HG is synthesized as a polymer of meGalA (top) and selectively demethylesterified in a random (middle) or blockwise manner (bottom) by pectin methylesterases (PMEs). (C–F) Arabidopsis flower meristem: 3D reconstruction from confocal images, top view (C,E,G) and SEM side view. Wild type (C,D); transgenic line upon induced over-expression of a PME inhibitor (PMEI3), which prevents the formation of organ primordia (E,F), or upon induced over-expression of a PME (PME5), which leads to the formation of extra primordia (G), which can also be seen in mature flowers (H). Adapted from [38] with permission.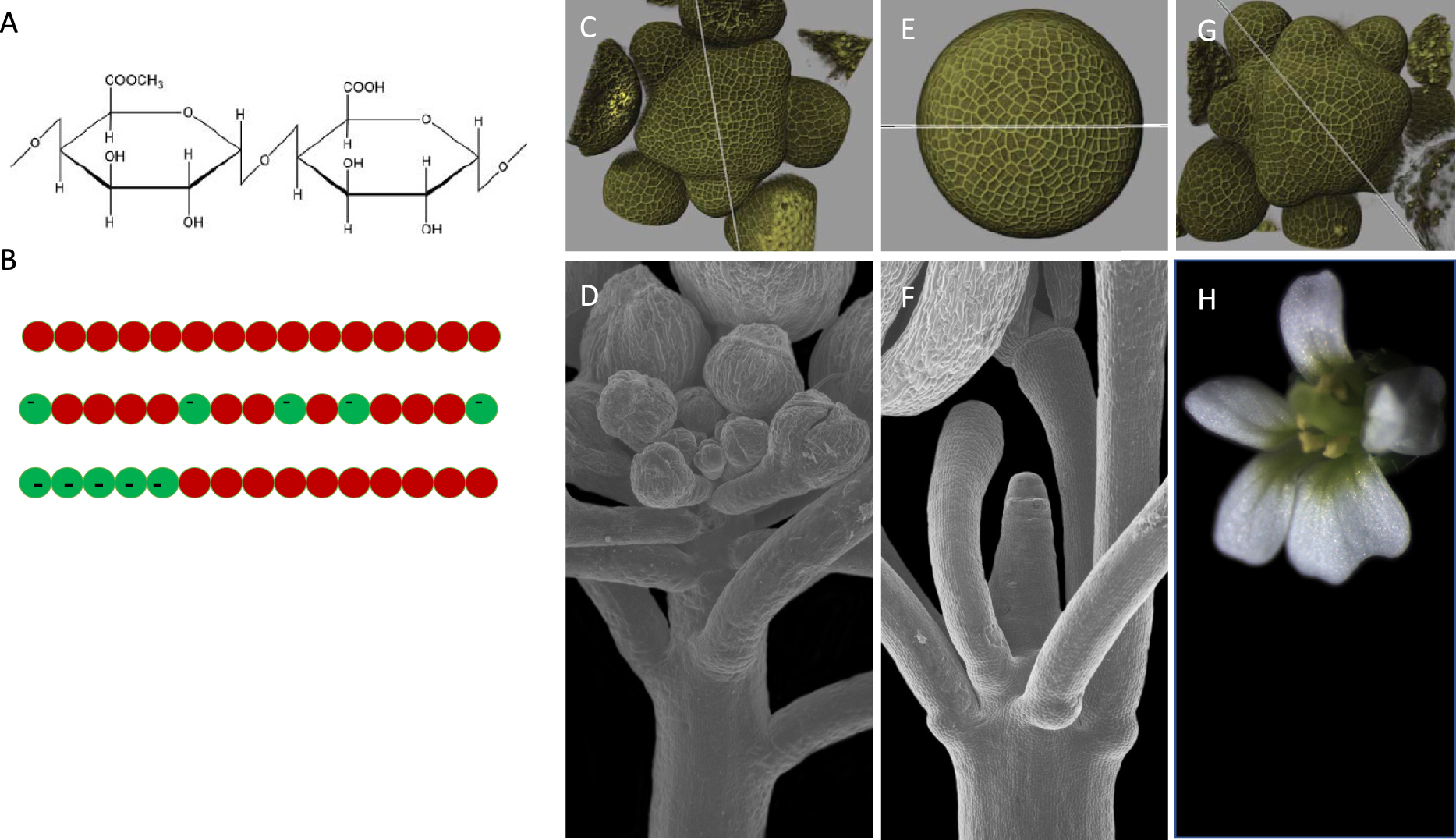
The study of the qua mutants, provided other unexpected insights into the biology of cell walls. Indeed, the cell separation phenotype (Figure 3) suggested that reduced HG levels affect the ability of the middle lamella to glue cells together [39]. This seemed logical since de-methylesterified HG can form calcium crosslinks, which can contribute to the adhesion of the pectins of adjacent cells. This narrative is alluring since it provides a direct connection between polymer properties and a macroscopic process at a cellular level. The situation, however, turned out not to be that simple. Indeed, Gregory Mouille next carried out a screen for suppressor mutants for the cell adhesion phenotype of qua1. This led to the identification of a number of mutants, called esmeralda (esmd), after the girl who saved Quasimodo in Victor Hugo’s novel [37]. Interestingly in esmd mutants, cell adhesion was restored without restoring the HG deficiency (Figure 3). ESMD1 encodes a putative glycosyl transferase. The exact link with cell adhesion remains to be determined but it is possible that EMSD1 modifies the activity of a molecule that senses pectin composition and controls cell adhesion through some other mechanism [37]. We did similar observations on cellulose-deficient mutants with a dwarf phenotype. We were able to isolate suppressor mutants that partially restore growth but not cellulose synthesis [40]. The causative gene for one of these mutants encodes a receptor kinase, which somehow senses the changes in the cell wall induced by the mutation [41]. This again showed that it is not the altered cell wall composition that prevents growth, but a secondary response of the cell to the cell wall perturbation.
These observations underline that “Occam’s Razor” (the principle of parsimony) does not always apply, due to feedback mechanisms and non-linear effects, which limits the usefulness of stable mutant phenotypes to bridge molecular and cellular scales. One way to cope with this is to make inducible changes over short time periods and assess the effects before secondary effects pile up. Alexis Peaucelle, in our group, explored this in his quest to understand the biophysical basis of cell expansion. The consensus was that the turgor pressure is the motor for cell expansion and selective wall relaxation controls the expansion rate [28]. To understand how pectin metabolism fits into this picture, he expressed a PME and a PMEI respectively in the shoot apical meristem under control of an inducible promoter (Figure 4) [38]. This led to spectacular results, where preventing HG de-methylesterification abolished primordia formation and enhancing HG de-methylesterification promoted the formation of extra organs. So, a simple modification of HG is necessary and sufficient to trigger dramatic developmental responses. Again, the exact underlying sequence of events was not clear. Using atomic force microscopy, he was able to establish a causal link between HG de-methylesterification and an increase in cell wall elasticity as measured by indentation with an atomic force microscope [42, 43]. The relation cell wall elasticity—cell expansion rate remains correlative however, even though both are triggered by the same HG modification. This relation is also not obvious since elasticity is a reversible deformation whereas growth corresponds to the irreversible deformation through removal and/or remodeling of load-bearing crosslinks (referred to as “creep”) [28]. In conclusion, it remains to be seen whether changes in wall elasticity are causative, or just an epiphenomenon, in the process that links pectin de-methylesterification to cell expansion [36].
5. The importance of cell wall architecture for cell expansion
To further investigate this connection, Alexis Peaucelle, during a sabbatical stay at the Sainsbury Laboratories in Cambridge, used the formation of the lobes of the puzzle-shaped epidermal pavement cells of Arabidopsis leaves as a model system (Figure 5). He collaborated with Kalina Haas, a postdoctoral fellow in the laboratory next door, to study the detailed architecture of the cell walls using dSTORM super-resolution light microscopy. This technique allows the visualization of fluorescently-labeled objects with a resolution, down to a few tens of nanometers, far below the diffraction limit of visible light [44]. They labeled the cell walls with specific fluorescently-tagged antibodies to reveal methylesterified and unesterified HGs respectively. When they focused on anticlinal walls (i.e., the walls perpendicular to the leaf surface), they were surprised to see that the HGs did not form a strawberry jam-like amorphous gel, as previously thought. Instead, the polymers were aligned and oriented perpendicularly to the leaf surface [45]. These aligned linear chains can actually form crystalline filaments just like the cellulose microfibrils, where the de-methylesterified HG crystals have a larger mesh size than those of the methylesterified HG. In addition, they observed that chemical de-esterification, actually promoted expansion of the walls of cells that were plasmolyzed and thus lack the turgor pressure that is thought to drive cell expansion. They also observed that HG was preferentially de-methylesterified in the walls of the cell at the convex side of the lobe. They proposed that the resulting swelling of the HG filaments on one side of the two connected cell walls was driving the formation of the lobes. This mechanism was further supported in vivo by the finding that preventing the asymmetric de-methylesterification by either promoting or inhibiting PME activity in all cells prevented the formation of the lobes. In conclusion, they provided evidence for a turgor-independent growth process, referred to as the “expanding beam” model, where enzymatically-induced swelling of oriented pectin filaments drives cell wall expansion [45]. This raises many new questions: (i) is this process applicable only to the formation of lobes of pavement cells or can it also explain growth of other cell types? (ii) how is the asymmetric HG de-methylesterification regulated? (iii) how is the “expanding beam” process integrated with turgor-dependent processes such as acid growth, where the removal, by the cell wall proteins “expansins”, of the crosslinks that connect load-bearing cellulose microfibrils (the so called “biomechanical hotspots” [28]), leads to cell wall relaxation and expansion?
Pectin de-methylesterification can confer intrinsic growth capacity to plant cell walls. (A) Development of puzzle-shaped pavement cells in Arabidopsis leaf epidermis. (B) HGs in anticlinal (perpendicular to the surface) cell walls form nanofibrils (orange and red bars), which are oriented transversely to the growth direction along cellulose microfibrils (blue lines). Asymmetric de-methylesterification of HG on the convex side of the lobe (red bars) promote its outgrowth [45].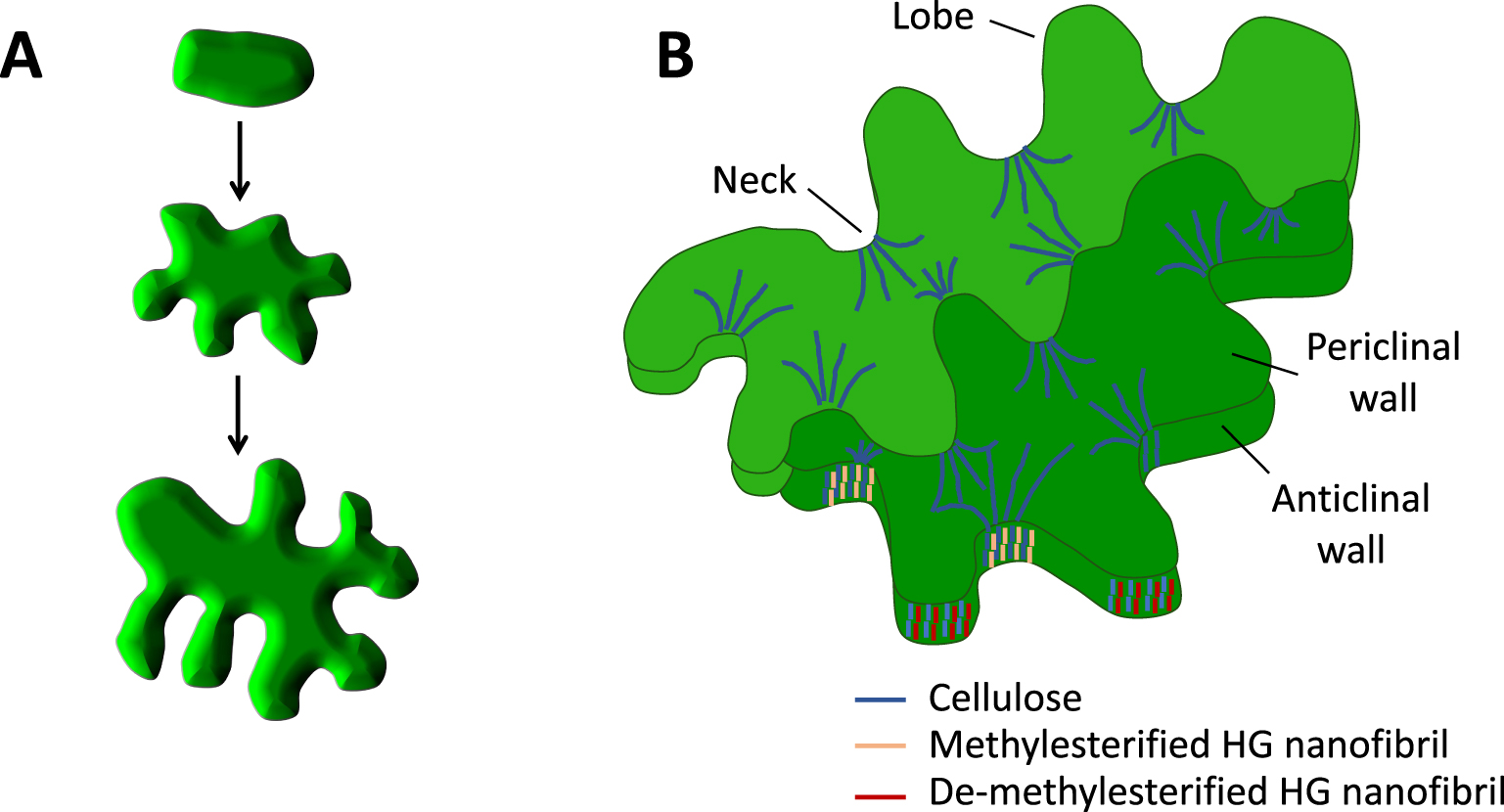
6. Connecting spatio-temporal scales in root hairs
To address these questions, we need a simple, preferentially single celled system and procedures for rapid modifications and read outs so that effects can be observed before feedback processes kick in. In addition, computational modeling is needed to bridge the different spatial (molecules, polymer assemblies, cell walls, cells) and temporal (seconds, minutes, hours, days) scales that link polymer physico-chemistry to cellular properties. We chose the root hair, which is an outgrowth of root epidermis cells and an “almost” single celled system [46]. Kinematic analysis shows that the growth rate oscillates together with a number of cellular parameters (cytosolic calcium, surface pH, reactive oxygen species levels, cell wall charge), which all oscillate at the same frequency (with a period of around 30 s) but with different phases [47]. Surface pH for instance is an important parameter, since almost all enzyme activities in the cell wall are strongly pH dependent, with for instance high and low pH optima for PMEs and expansins respectively. To investigate potential causality among these parameters one needs to be able to manipulate one parameter and observe the responses at a time scale smaller than the 30 s period. To this end, our team is currently developing optogenetics tools for rapid light mediated activation or inactivation of enzyme activities [48]. For instance, a light-activated proton pump from Archae [49] expressed in root hairs, allowed a light-induced acidification of the root hair surface within seconds upon light treatment. The next step is to evaluate the impact of the pH changes on the other parameters, cell wall properties and growth behavior. These approaches will now be further developed in the framework of an ERC starting grant to Kalina Haas in our team.
7. Michel Caboche’s intellectual heritage
Thirty years after my first encounter with Michel Caboche, and thanks to his early intuition and infallible support, enormous progress has been made in our understanding of the metabolism of plant cell walls and its relation to cell expansion. The use of Arabidopsis mutants that we pioneered together with the team of Chris Somerville in Michigan [50], has become completely mainstream in cell wall research. This has led to important new insights into the synthesis of cell wall polysaccharides and the molecular mechanisms that underlie plant growth. Whereas the cell wall composition can vary widely among cell types and plant species [51], many of the discoveries in Arabidopsis turned out to be relevant also in other plant species including major crops. For instance, the dissection of the lignin and pectin biosynthetic pathways has led to strategies to improve the digestibility of maize biomass for ruminants [52] or of energy crops and trees for conversion into second-generation biofuel [53, 54]. Knowledge about cellulose biosynthesis and its relation to cell elongation is being used for the improvement of cotton fiber quality [55]. The knowledge of structural determinants governing cellulose–hemicellulose interactions can be harnessed for the design of new nanomaterials [56]. The understanding of cell wall integrity signaling leads to new strategies for breeding or engineering pathogen resistance [57, 11]. Finally the understanding of the biophysical basis of plant cell expansion is essential for the development of reliable computational multiscale models predicting plant growth in a changing climate [12, 58] and for breeding better adapted crop varieties [59]. Michel has raised an important family of intellectual children, grand and grand-grand children and there is no reason that this will not continue in the future! Many thanks for all this Michel!
Conflicts of interest
The author has no conflict of interest to declare.
Version française
1. Introduction : la rencontre avec Michel Caboche
Vers la fin de mon séjour postdoctoral aux Etats-Unis, j’ai commencé à chercher un poste en France pour rejoindre ma compagne, qui était employée à l’Institut Pasteur à Paris. J’ai été intrigué par les travaux de l’équipe de Michel Caboche sur l’utilisation de la génétique dans l’étude de l’assimilation de l’azote [1, 2], que j’ai trouvés très innovants et inspirants puisqu’ils utilisaient des concepts et des approches empruntés à la génétique dans les levures ou les systèmes animaux pour étudier les mécanismes sous-jacents à l’efficacité de l’utilisation de l’azote, un sujet si important pour l’agriculture, en particulier dans le contexte de la nécessité toujours plus pressante de réduire l’utilisation des engrais.
Je l’ai contacté et il m’a invité à visiter le laboratoire de biologie cellulaire du centre INRA (renommé INRAE en 2020) à Versailles. Là, j’ai été très surpris de rencontrer l’un des plus célèbres biologistes végétal français dans un minuscule bureau, à côté des toilettes, sous le toit du bâtiment, avec à peine assez de place pour accueillir un visiteur ! Heureusement, cela n’a pas empêché nos échanges d’être très amicaux et intéressants et il m’a proposé de rejoindre son équipe et l’INRA en 1992 en tant que jeune « chargé de recherche ». J’ai été immédiatement frappé par l’hospitalité de mes nouveaux collègues et par l’atmosphère stimulante de coopération et de bienveillance qui régnait dans le laboratoire, sous l’impulsion du charismatique directeur de l’époque, Jean Pierre Bourgin.
Faisant partie d’une équipe jeune et bouillonnante sous la direction de Michel Caboche, nous avions l’objectif ambitieux d’utiliser la nouvelle plante modèle Arabidopsis thaliana pour étudier la croissance et le développement des plantes, dans le but ultime d’utiliser ces connaissances pour améliorer les plantes cultivées. Notre vision sur l’intérêt sociétal de nos recherches, exprimée dans le refrain d’une chanson que nous avons écrite en 1996 pour célébrer l’ouverture d’une nouvelle extension du laboratoire, peut sembler assez naïve avec le recul d’aujourd’hui.
« Arabidopsis, donne-moi tes secrets,
Arabidopsis, on en fera un brevet,
avec tes gènes si facilement clonés,
on améliore colza et peuplier »
Le passage de José Bové et de ses amis et le changement concomitant de la perception du public sur la biotechnologie végétale, nous a malheureusement empêchés de réaliser tous nos rêves de jeunesse.
2. Génétique moléculaire d’Arabidopsis
L’une des premières actions inspirées par Michel Caboche, et menée par ma collègue Catherine Bellini, a été de réaliser un crible EMS pour les mutants de développement [3]. L’idée initiale était d’identifier les composants critiques de la voie de signalisation du régulateur de croissance clé qu’est l’auxine, en recherchant les mutants qui présentaient des défauts de croissance au stade plantule. Le criblage a donné un grand nombre de mutants, dont beaucoup se sont avérés avoir des parois cellulaires altérées. Ainsi, en suivant la génétique, nous avons fait une plongée involontaire dans les méandres de la paroi végétale.
Rétrospectivement, il n’est pas si surprenant que tant de mutants présentant des défauts de développement soient affectés dans l’établissement de la paroi. En effet, le cœur de la morphogenèse végétale est la capacité de générer des panneaux solaires plats avec un coût métabolique minimal. L’astuce que les plantes ont trouvée est l’adoption d’un squelette hydrostatique, avec des vacuoles remplies de liquide dans des cellules pressurisées, entourées d’une paroi suffisamment solide pour résister aux forces générées par cette pression [4]. Cette paroi est constituée à 90% de carbohydrates, une matière première abondante et facilement disponible pour les organismes photosynthétiques [5]. Plus tard au cours du développement, la croissance secondaire peut donner naissance à des structures porteuses spécialisées (par exemple, des troncs et des branches) dans lesquelles les parois s’immobilisent et deviennent elles-mêmes porteuses indépendamment de la pression hydrostatique des cellules.
Nous nous concentrons ici sur les parois des cellules en croissance, ou parois primaires. L’utilisation d’un squelette hydrostatique impose une contrainte majeure aux cellules des plantes, mais aussi d’autres organismes à parois comme les bactéries et les champignons : elles doivent se dilater tout en maintenant l’intégrité de leurs parois [6]. Cette contrainte est devenue l’objet principal de nos recherches.
Avant de parler de notre travail, je vais d’abord faire un bref rappel sur la composition et l’architecture de la paroi primaire. Elle est constituée pour environ 60% d’eau, la matière sèche est donc extrêmement concentrée, et les polymères sont dans un état semi-solide, ce qui complique les processus biochimiques dans ce compartiment [7]. La cellulose se trouve sous forme de microfibrilles d’un diamètre d’environ 3 nm, qui forment le réseau porteur de la paroi. On trouve également une matrice d’hémicelluloses, des polymères porteurs de branches qui empêchent leur association en structures cristallines, et de pectines, un ensemble de polymères chargés négativement contenant de l’acide galacturonique (GalA). Enfin, les parois primaires contiennent de petites quantités (environ 10% dans les feuilles d’Arabidopsis) de protéines. Les polymères de la paroi forment un réseau grâce à des liaisons covalentes et non covalentes. Au moment de notre examen, on ne savait pratiquement rien de la biosynthèse des parois. Pas une seule enzyme de biosynthèse de la paroi cellulaire n’avait été isolée ou clonée [8]. Une véritable terra incognita au niveau biochimique et génétique.
Nous avons donc isolé un grand nombre de mutants présentant un hypocotyle court, la tige embryonnaire de la plantule. Pour y voir plus clair dans cette grande collection de mutants, Grégory Mouille, dans l’équipe, a développé une méthode de criblage secondaire basée sur la spectroscopie infrarouge à transformée de Fourier, couplée à un microscope (Figure 1) [9]. Les spectres infrarouges de transmission, qui reflètent essentiellement la composition des parois, ont été obtenus à partir d’une fenêtre d’environ 20 × 20 μm de l’hypocotyle séché. Ces spectres sont difficiles à interpréter en raison de la superposition des absorbances d’une multitude de liaisons chimiques. Les profils FTIR ont cependant permis une classification extrêmement précise des mutants de la paroi cellulaire, comme nous avons pu le montrer grâce à une collaboration fructueuse avec Stéphane Robin, un expert en mathématiques appliquées [10]. En effet, en incluant plusieurs allèles indépendants pour un même gène, nous avons presque toujours observé que ces allèles étaient regroupés, même lorsqu’ils étaient comparés à des allèles pour d’autres gènes apparentés ayant des phénotypes macroscopiques très similaires. Le regroupement de mutants inconnus avec des mutants déjà caractérisés ou avec des plantules de type sauvage traitées avec des inhibiteurs spécifiques a permis de formuler des hypothèses sur les défauts génétiques sous-jacents, sur la base d’un raisonnement de type « culpabilité par association » (Figure 1).
Classification des mutants de la paroi cellulaire d’Arabidopsis basée sur la spectroscopie infrarouge à transformée de Fourier [9, 10]. (A) Semis cultivé à l’obscurité, le carré indique la zone à partir de laquelle les spectres ont été obtenus. (B) Moyenne des spectres FTIR (n = 20) des parois cellulaires de l’hypocotyle du type sauvage (ligne rouge) et des mutants (ligne blanche). (C) Analyse groupée des spectres FTIR. Les couleurs font référence aux loci mutants pour lesquels plusieurs allèles ont été analysés. Notez le regroupement des allèles, mais aussi le regroupement des mutants affectés dans la synthèse de la cellulose (rsw1-2, kor-2, kob1-1, kob1-2, allèles pom1, rsw1-10, pom1-21, allèles prc1, kor-1 et rsw2-3) avec les plantes de type sauvage traitées avec les inhibiteurs de synthèse de la cellulose DCB ou isoxaben (isox), le regroupement des mutants avec des microtubules altérés (ton1-1, allèles bot1 et sab) avec le type sauvage traité avec l’inhibiteur de microtubules oryzalin (le mutant brassinostéroïde det2 a également des microtubules altérés [11]), et les mutants avec des pectines altérées (allèles qua1 et qua2 et mutants pme3, pme32 et pme34). Le panneau C est adapté de [12].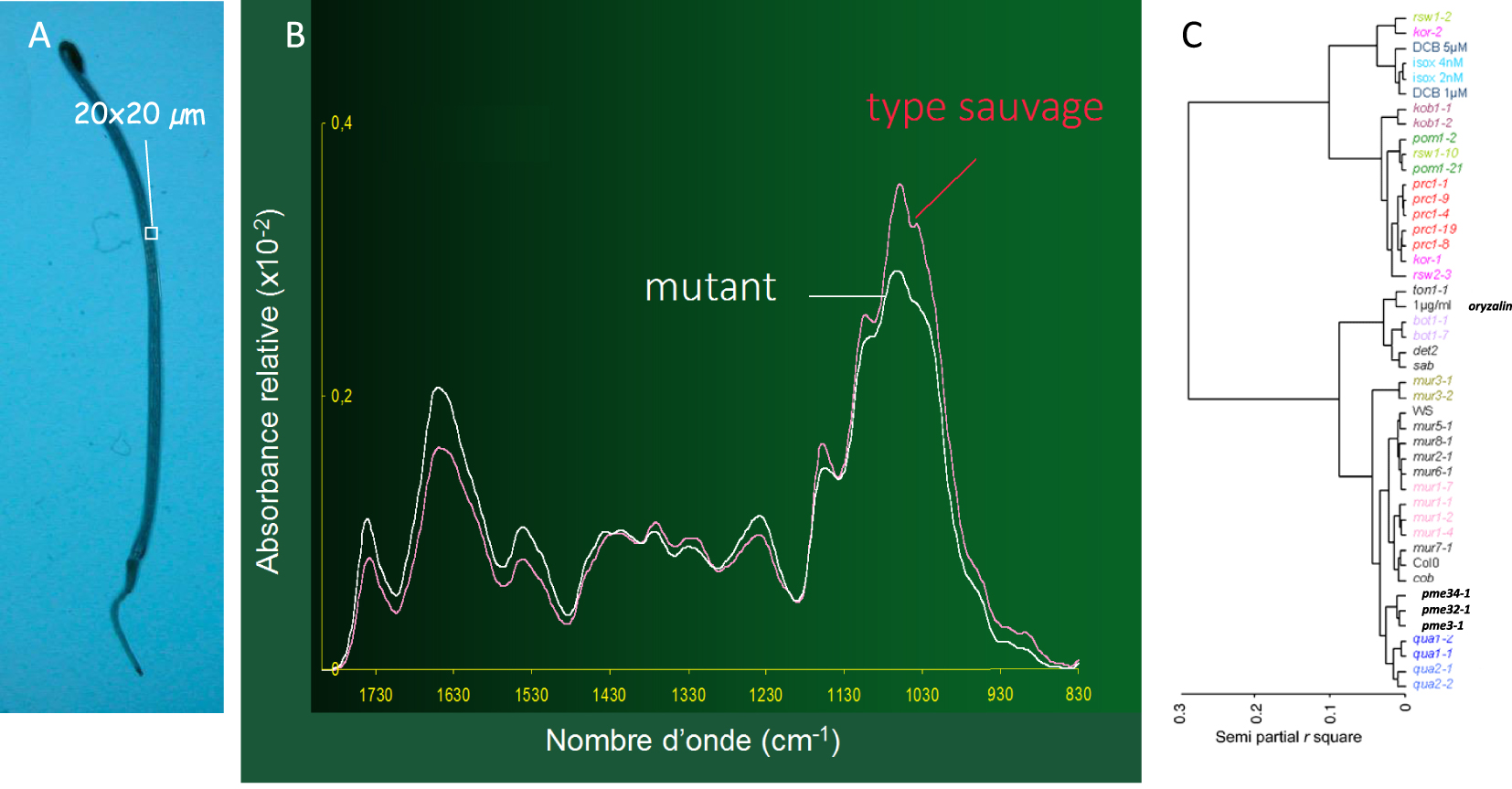
Structure et motilité dans la membrane plasmique du complexe cellulose synthase (CSC). (A) CSC hexamérique dans le feuillet interne de la membrane plasmique montré par TEM « freeze-fracture » (de [13] avec permission). (B) Vue de dessus de la structure 3D d’un trimère de sous-unité catalytique formant l’un des 6 globules du CSC. Les chaînes de glucane dans le canal transmembranaire sont représentées en blanc, jaune et orange. (C,D) La microscopie à disque rotatif sur les cellules de l’épiderme de l’hypocotyle d’Arabidopsis cultivé à l’obscurité, révèle des ponctuations CESA3 marquées par la GFP en rangées dans la membrane plasmique et dans les corps de Golgi (structures plus grandes en forme de beignets) (C), une projection temporelle (10 min) montre les trajectoires linéaires des CSC dans la membrane plasmique (D). Barre d’échelle = 10 μm en (C,D).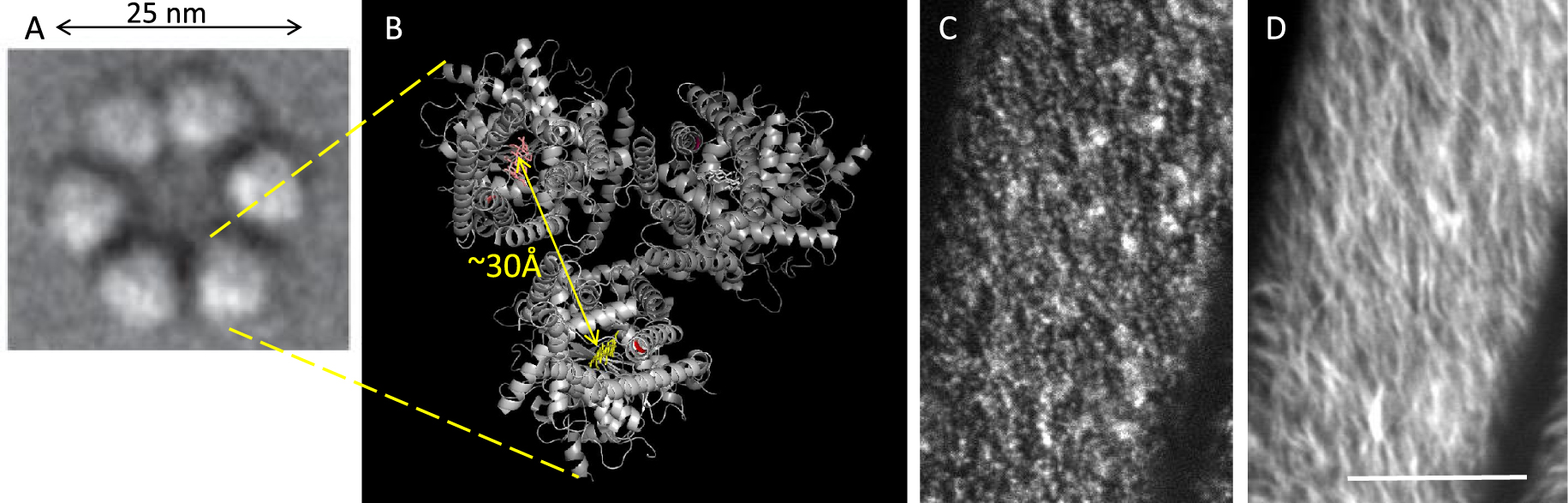
3. Synthèse de la cellulose
Nous avons ainsi trouvé un grand nombre de mutants se regroupant avec les plantes de type sauvage traitées avec des inhibiteurs de la synthèse de cellulose (Figure 1) [9]. Parmi ces mutants, l’analyse moléculaire a permis d’identifier 3 gènes, qui, sur la base de la similarité de séquence avec les synthases de cellulose bactériennes, ont été considérés comme codant pour des sous-unités catalytiques distinctes (CESA1, 3 et 6) du complexe cellulose synthase [14, 15]. Il a été démontré que ce complexe cellulose-synthase (CSC) correspond aux structures hexamériques de 25 nm de diamètre, appelées « rosettes », que l’on peut observer dans la membrane plasmique des cellules végétales (Figure 2) [16]. L’avancée majeure suivante dans ce domaine a été la détermination de la structure 3D de la cellulose synthase par le groupe de Jochem Zimmer, d’abord à partir de bactéries en utilisant la cristallographie aux rayons X [17], puis à partir de plantes, en utilisant la Cryo-TEM d’un trimère de sous-unités catalytiques identiques provenant du peuplier [18]. Cela a permis de comprendre le mécanisme de réaction qui sous-tend la génération, à partir de l’UDP-Glc, d’un polymère à liaisons glycosidiques alternées, typique des polysaccharides à liaison β(1–>4). Elle a montré la présence d’un canal anhydre dans chaque sous-unité catalytique, abritant une chaîne de 18 résidus Glc sur leur chemin vers la surface [17]. Elle a également fourni des informations sur le mode d’action des inhibiteurs de la synthèse de la cellulose et a confirmé la présence de trois sous-unités catalytiques dans chaque globule du complexe hexamérique (Figure 2B) [18, 19]. En supposant qu’une CSC produit une microfibrille élémentaire, l’association de 18 sous-unités catalytiques implique la présence de 18 chaînes de glucane dans une microfibrille typique, ce qui est cohérent avec les études structurales utilisant la RMN à l’état solide [13]. Une autre conséquence spectaculaire de ces études génétiques a été la possibilité de visualiser des CSC marqués par fluorescence dans des cellules vivantes en utilisant la microscopie confocale à disque rotatif (Figure 2C,D) [14, 20, 21]. Cela a révélé la présence de centaines de CSC associés à la membrane plasmique, qui migrent dans deux directions le long des microtubules corticaux, propulsés par la polymérisation des chaînes de glucane, où la vitesse observée d’environ 300 nm/min correspond à un taux de synthèse de 10 résidus/seconde par chaîne. D’autres études d’imagerie de cellules vivantes et l’analyse de mutants ont révélé la complexité de la biologie cellulaire de la synthèse de la cellulose, avec des modifications post-traductionnelles complexes des composants des CSC, les CSC circulant entre les corps de Golgi, le réseau trans-Golgi (qui se dissocie des corps de Golgi dans les cellules végétales), un compartiment de recyclage spécialisé associé aux microtubules [21, 22] et la membrane plasmique [16]. Cela permet de récupérer temporairement les CSC dans les compartiments de recyclage en réponse à des stress environnementaux qui affectent la paroi cellulaire, comme le stress salin ou osmotique [23]. Les cribles ont également permis d’identifier un certain nombre de gènes codant pour d’autres composants de ce complexe multiprotéique, parmi lesquels un membre de la famille des endo-(1–>4)-β-glucanases (KORRIGAN, KOR) [24], des protéines de liaison CESA localisées dans le Golgi, des protéines bifonctionnelles qui se lient à la fois aux CESA et aux microtubules, qui contribuent à guider les complexes ou à médier leur internalisation induite par le stress, combinée à la dépolymérisation des microtubules [16]. Enfin, l’observation de la connexion entre les microtubules et la cellulose a donné naissance à de nouveaux modèles de morphogenèse, dans lesquels les microtubules s’orientent le long des schémas de contrainte dans les tissus par une voie mécanosensible jusqu’ici mal caractérisée, qui à son tour renforce les tissus le long des contraintes principales, par l’orientation des schémas de dépôt de cellulose porteuse [25].
Malgré des progrès considérables dans notre compréhension de la synthèse de la cellulose, de nombreuses questions restent ouvertes. En voici quelques exemples : Comment l’insertion, l’activation et la récupération de la membrane des CSC sont-elles régulées ? Comment un complexe aussi grand (>25 nm de diamètre) peut-il s’insérer dans des vésicules sécrétoires ou endocytotiques recouvertes de clathrine de ~30 nm de diamètre [26], ou disposons-nous de compartiments sécrétoires/endocytotiques spécialisés plus grands ? Quel est le rôle du grand nombre de groupes d’acides gras qui sont attachés de manière covalente au complexe [27] ? Comment la synthèse de la cellulose est-elle coordonnée avec l’accumulation des polymères de la matrice ? Comment les CSC sont-ils déconnectés de la paroi cellulaire lors de leur internalisation ? Quel est le rôle dans la synthèse de la cellulose de la cellulase KOR, de la protéine COBRA à ancrage glycosylphophatidylinositol, de la protéine POM1 de type chitinase et de plusieurs protéines associées au Golgi [16] ? Qu’est-ce qui contrôle la formation des liaisons transversales cellulose–cellulose porteuses dans la paroi cellulaire [28] ? Comment les modèles de dépôt de cellulose sont-ils régulés, par exemple les lamelles successives dans les parois poly-lamellaires [29] ou les profils de dépôts, souvent remarquables, dans les parois cellulaires secondaires, et enfin comment les modèles de stress sont-ils détectés pour orienter les microtubules [30] ?
Connexion des échelles spatiales : contenu en pectine et adhésion cellule-cellule. Projections en Z d’empilements confocaux d’hypocotyles de type sauvage et mutants, colorés à l’iodure de propidium, âgés de 4 jours et cultivés à l’obscurité. qua2-1 a une réduction de 50% du contenu en HG et montre une adhésion cellulaire réduite. la mutation de perte de fonction esmd1 supprime le phénotype d’adhésion cellulaire de qua2-1 sans changer le contenu en HG, suggérant que le défaut d’adhésion cellulaire n’est pas un résultat direct du défaut en HG. Barres d’échelle = 75 μm. Adapté de [37] avec permission.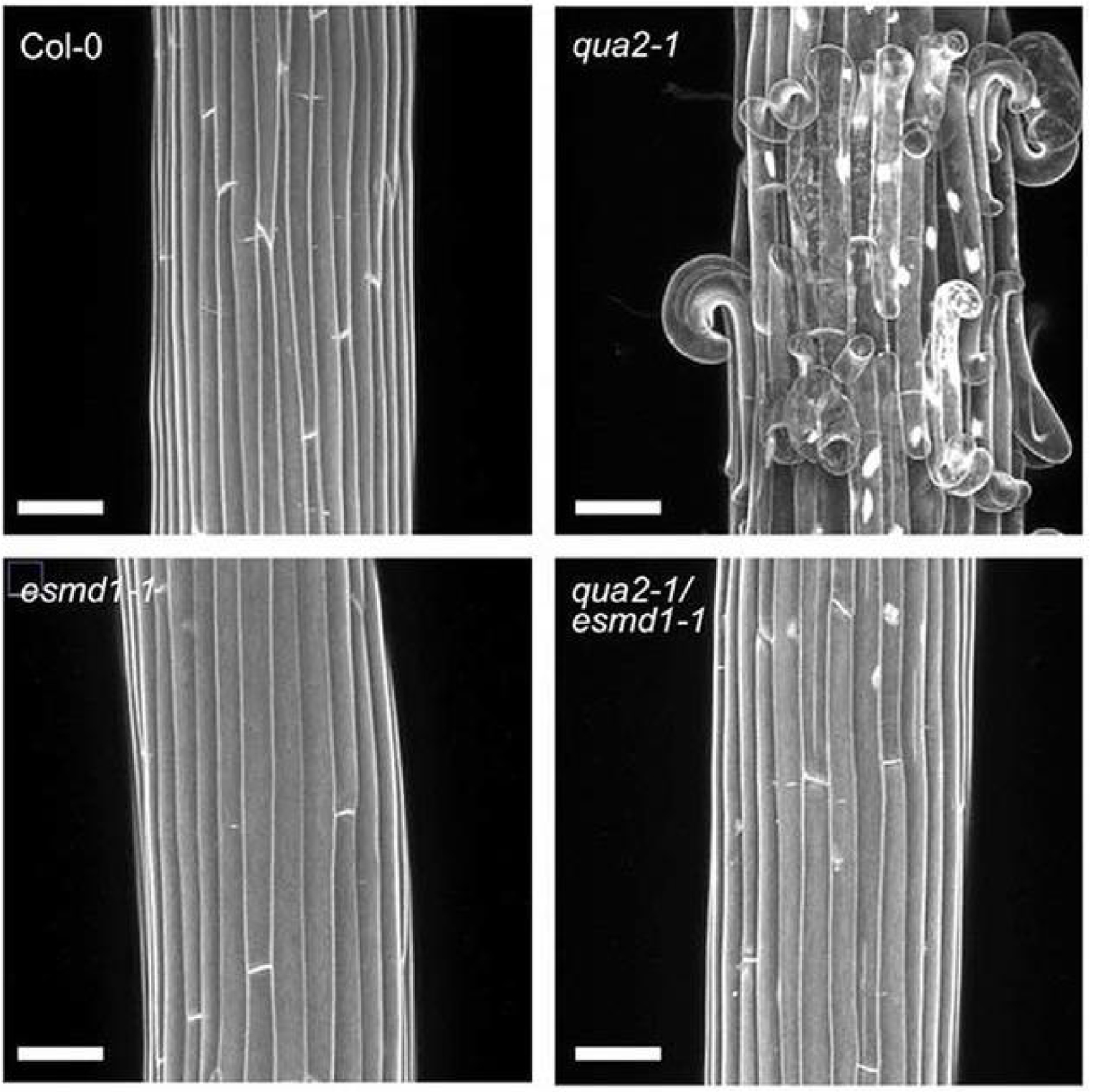
Le métabolisme du polymère pectique homogalacturonan (HG) joue un rôle clé dans la croissance et la morphogenèse des plantes. (A) Dimère de l’acide galacturonique methyl-estérifié (meGalA, sphères rouges dans B) lié en α(1–>4) à GalA (sphères vertes dans B). (B) L’HG est synthétisé sous forme de polymère de meGalA (en haut) et déméthylestérifié sélectivement de manière aléatoire (au milieu) ou par blocs (en bas) par des pectine méthylestérases (PMEs). (C–F) Méristème de la fleur d’Arabidopsis : Reconstruction 3D à partir d’images confocales, vue de dessus (C,E,G) et vue latérale en microscopie électronique à balayage. Type sauvage (C,D) ; lignée transgénique lors de la surexpression induite d’un inhibiteur de PME (PMEI3), qui empêche la formation des primordia d’organes (E,F), ou lors de la surexpression induite d’une PME (PME5), qui conduit à la formation de primordia supplémentaires (G), qui peuvent également être observés dans les fleurs matures (H). Adapté de [38] avec permission.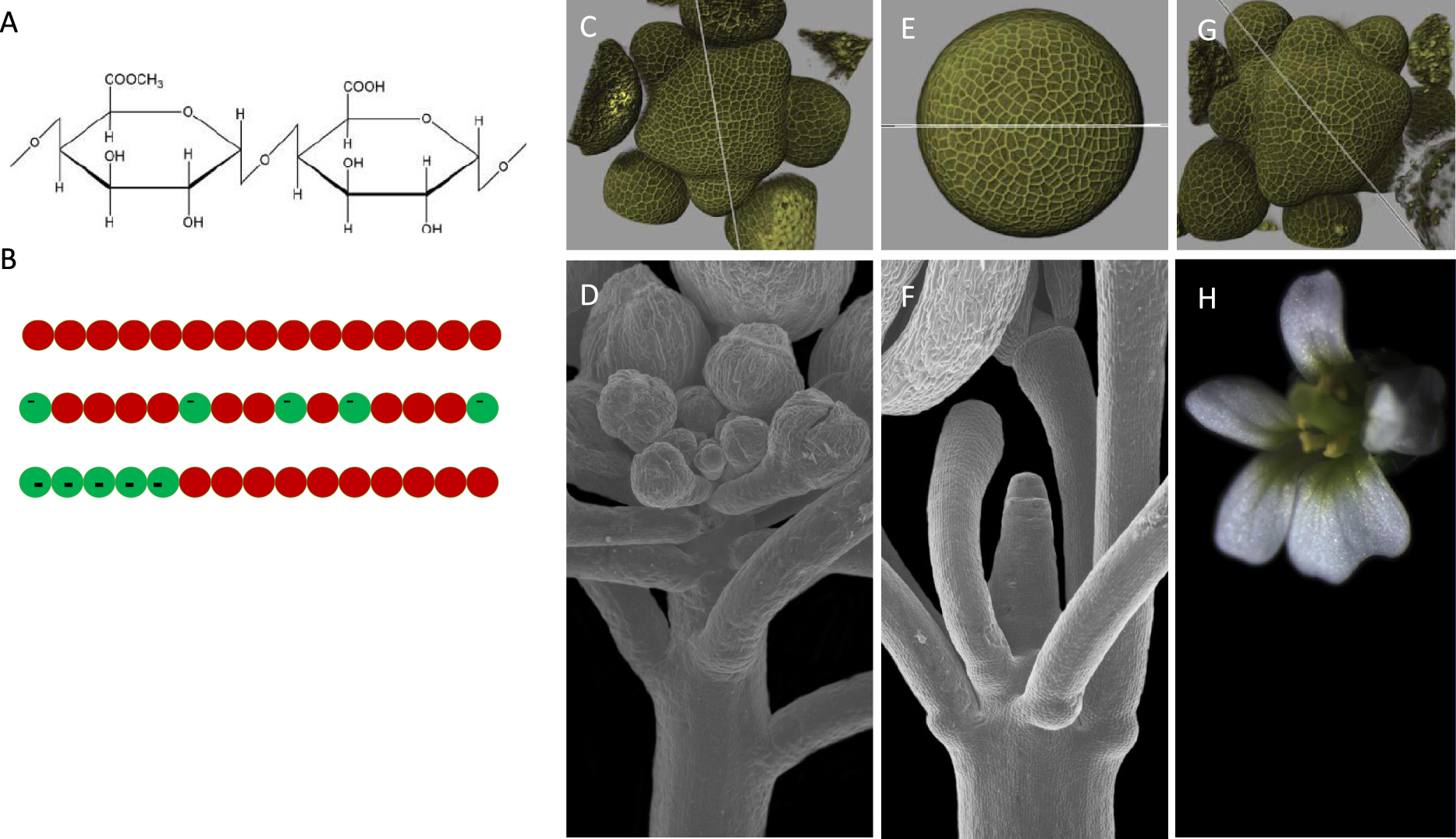
4. Pectines et expansion cellulaire
Une autre classe de mutants de paroi cellulaire regroupés par FTIR, baptisés quasimodo (qua) 1 et 2, en raison de leur phénotype tordu, avec de nombreuses cellules séparées de leurs voisines, a montré des changements dans la teneur en pectine (Figure 3) [31, 32]. Les pectines sont des polymères multiblocs complexes chargés, caractérisés par la présence d’acide galacturonique (GalA) [33]. qua1 et 2 ont montré des niveaux réduits d’homogalacturonane (HG), qui est un polymère pectique linéaire abondant (jusqu’à 50% du contenu de la paroi cellulaire) de GalA α(1–>4)-liés (Figure 4A). Des analyses moléculaires et biochimiques ont révélé que les QUASIMODO1 et 2 codent pour des GalA- et méthyl-transférases respectivement, tous les deux localisées dans le Golgi, [33, 34]. En effet, l’HG est synthétisée dans les corps de Golgi sous une forme hautement méthylestérifiée et donc non chargée. Lors de la sécrétion, le polymère peut être déméthylestérifié par les Pectine Methyl Esterases (PMEs) dans la paroi cellulaire [35], exposant ainsi les charges négatives des groupes carboxyles (Figure 4B). Les PME sont codées par de grandes familles de gènes (66 membres chez Arabidopsis) et sont contrôlées par des inhibiteurs de PME endogènes (PMEI) codés par des familles de gènes tout aussi grandes. Différentes activités des PME ont été identifiées, certaines sont processives, générant des tronçons de résidus déméthylés, d’autres sont non-processives (Figure 4B) [35]. On ne sait pas si ces dernières activités agissent uniquement de manière aléatoire ou si elles peuvent également générer des schémas de déméthylestérification spécifiques [36]. Avec le recul, il est facile de comprendre pourquoi les plantes déploient tant d’efforts pour contrôler la déméthylestérification de l’HG. En effet, la physique des polymères nous apprend que la distribution des charges d’un polymère a une influence considérable sur ses propriétés physico-chimiques. Nous sommes ici en présence de ce que l’on appelle la « matière molle active », qui peut être définie comme « des systèmes de matière molle contenant des constituants autopropulsés (ou actifs) qui engendrent des propriétés dynamiques émergentes à une échelle supérieure ». Dans ce cas, ces propriétés émergentes peuvent être des changements de viscosité, une séparation de phases ou même un mouvement, comme nous le verrons dans la section suivante [36].
L’étude des mutants qua a fourni d’autres informations inattendues sur la biologie des parois cellulaires. En effet, le phénotype de séparation cellulaire (Figure 3) suggère que des niveaux réduits d’HG affectent la capacité de la lamelle centrale à coller les cellules ensemble [39]. Cela semblait logique puisque l’HG déméthylestérifiée peut former des réticulations avec du calcium, qui peuvent contribuer à l’adhésion des pectines des cellules adjacentes. Ce récit est séduisant car il établit un lien direct entre les propriétés des polymères et un processus macroscopique au niveau cellulaire. Cependant, la situation ne s’est pas avérée aussi simple. En effet, Gregory Mouille a ensuite procédé à un criblage de mutants suppresseurs du phénotype d’adhésion cellulaire de qua1. Cela a conduit à l’identification d’un certain nombre de mutants, appelés esmeralda (esmd), du nom de la fille qui a sauvé Quasimodo dans le roman de Victor Hugo [37]. Il est intéressant de noter que chez les mutants esmd, l’adhésion cellulaire a été restaurée sans rétablir la déficience en HG (Figure 3). ESMD1 code pour une glycosyltransférase putative. Le lien exact avec l’adhésion cellulaire reste à déterminer mais il est possible que l’ESMD1 modifie l’activité d’une molécule qui détecte la composition de la pectine et contrôle l’adhésion cellulaire par un autre mécanisme [37]. Nous avons fait des observations similaires sur des mutants déficients en cellulose présentant un phénotype nain. Nous avons pu isoler des mutants suppresseurs qui restaurent partiellement la croissance mais pas la synthèse de la cellulose [40]. Le gène touché dans une classe de ces mutants code pour une kinase réceptrice, qui détecte d’une manière ou d’une autre les modifications de la paroi cellulaire induites par la mutation [41]. Cela montre à nouveau que ce n’est pas la composition altérée de la paroi cellulaire qui empêche la croissance, mais une réponse secondaire de la cellule à la perturbation de la paroi cellulaire.
Ces observations soulignent que le « rasoir d’Occam » (le principe de parcimonie) ne s’applique pas toujours, en raison des mécanismes de rétroaction et des effets non linéaires, ce qui limite l’utilité des phénotypes mutants stables pour établir un pont entre les échelles moléculaire et cellulaire. Une façon de faire face à cette situation est d’effectuer des changements inductibles sur de courtes périodes de temps et d’évaluer les effets avant que les effets secondaires ne s’accumulent. Alexis Peaucelle, dans notre groupe, a exploré cette possibilité dans sa quête pour comprendre les bases biophysiques de l’expansion cellulaire. Le consensus était que la pression de turgescence est le moteur de l’expansion cellulaire et que la relaxation sélective de la paroi contrôle le taux d’expansion [28]. Pour comprendre comment le métabolisme de la pectine s’intègre dans ce tableau, il a exprimé respectivement une PME et une PMEI dans le méristème apical sous le contrôle d’un promoteur inductible (Figure 4) [38]. Cela a conduit à des résultats spectaculaires : empêcher la déméthylestérification de l’HG abolit la formation de primordia et augmenter la déméthylestérification de l’HG favorise la formation d’organes supplémentaires. Ainsi, une simple modification de l’HG est nécessaire et suffisante pour déclencher des réponses développementales spectaculaires. Là encore, la séquence exacte des événements sous-jacents n’était pas claire. Il a pu établir un lien de causalité entre la déméthylestérification de l’HG et une augmentation de l’élasticité de la paroi cellulaire mesurée par indentation avec un microscope à force atomique [42, 43]. La relation élasticité de la paroi cellulaire — taux d’expansion cellulaire reste cependant corrélative, même si les deux sont déclenchés par la même modification de l’HG. Cette relation n’est pas non plus évidente puisque l’élasticité est une déformation réversible alors que la croissance correspond à une déformation irréversible par la suppression et/ou remodelage des réticulations porteuses (appelée « creep ») [28]. En conclusion, il reste à voir si les changements dans l’élasticité de la paroi sont une cause, ou simplement un épiphénomène, dans le processus qui lie la déméthylestérification de la pectine à l’expansion cellulaire [36].
La déméthylestérification de la pectine peut conférer une capacité de croissance intrinsèque aux parois cellulaires des plantes. (A) Développement de cellules de pavage en forme de puzzle dans l’épiderme des feuilles d’Arabidopsis. (B) Les HGs dans les parois cellulaires anticlinales (perpendiculaires à la surface) forment des nanofibrilles (barres orange et rouges), qui sont orientées transversalement à la direction de croissance le long des microfibrilles de cellulose (lignes bleues). La déméthylestérification asymétrique de l’HG sur le côté convexe du lobe (barres rouges) favorise le gonflement de la paroi et la croissance du lobe [45].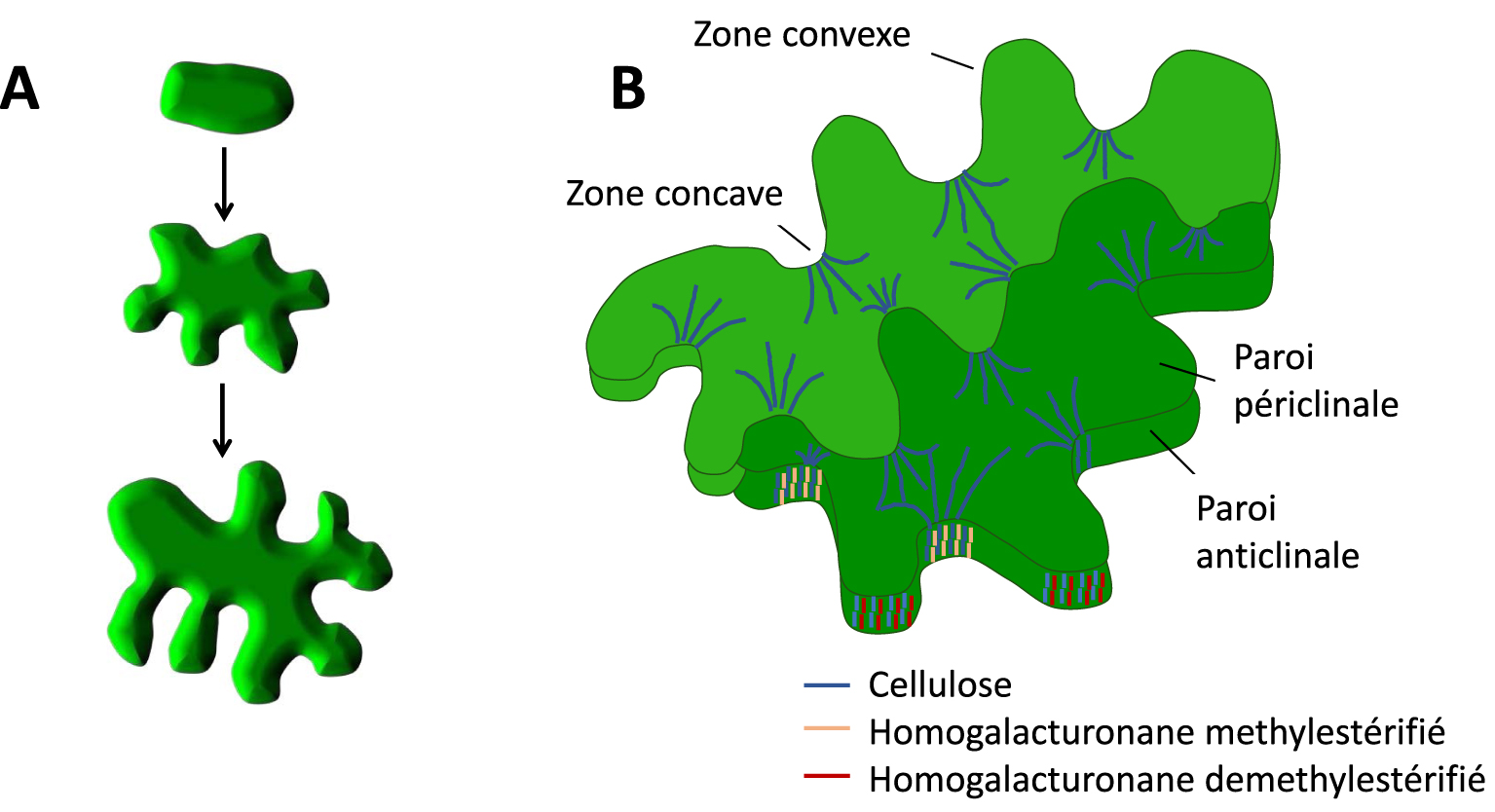
5. L’importance de l’architecture de la paroi cellulaire pour l’expansion cellulaire
Pour approfondir ce lien, Alexis Peaucelle, lors d’un séjour sabbatique aux Sainsbury Laboratories à Cambridge, a utilisé comme système modèle la formation des lobes des cellules du pavé épidermique en forme de puzzle, des feuilles d’Arabidopsis (Figure 5). Il a collaboré avec Kalina Haas, une boursière postdoctorale du laboratoire voisin, pour étudier l’architecture détaillée des parois cellulaires à l’aide de la microscopie optique à super-résolution dSTORM. Cette technique permet de visualiser des objets marqués par fluorescence avec une résolution de quelques dizaines de nanomètres, bien en dessous de la limite de diffraction de la lumière visible [44]. Ils ont marqué les parois cellulaires avec des anticorps spécifiques marqués par fluorescence pour révéler les HGs méthylestérifiées et non-estérifiées respectivement. Lorsqu’ils se sont concentrés sur les parois anticlinales (c’est-à-dire les parois perpendiculaires à la surface de la feuille), ils ont été surpris de constater que les HG ne formaient pas un gel amorphe semblable à de la confiture, comme on le pensait auparavant. Au contraire, les polymères étaient alignés et orientés perpendiculairement à la surface de la feuille [45]. Ces chaînes linéaires alignées peuvent en fait former des filaments cristallins tout comme les microfibrilles de cellulose, où les cristaux d’HG déméthylestérifiés ont une taille de maille plus grande que ceux de l’HG méthylestérifié. En outre, ils ont observé que la désestérification chimique favorisait en fait l’expansion des parois des cellules qui étaient plasmolysées et n’avaient donc pas la pression de turgescence qui est censée propulser l’expansion cellulaire. Ils ont également observé que l’HG était préférentiellement dé-méthylestérifié dans les parois de la cellule du côté convexe du lobe. Ils proposent que le gonflement des filaments d’HG qui s’ensuit d’un côté des deux parois cellulaires connectées conduise à la formation des lobes. Ce mécanisme a été confirmé in vivo par le fait que la prévention de la déméthylestérification asymétrique par la promotion ou l’inhibition de l’activité de la PME dans toutes les cellules a empêché la formation des lobes. En conclusion, ils ont fourni des preuves d’un processus de croissance indépendant de la turgescence, appelé modèle de la « poutre en expansion », dans lequel le gonflement enzymatiquement induit des filaments de pectine orientés entraîne l’expansion de la paroi cellulaire [45]. Cela soulève de nombreuses nouvelles questions : (i) ce processus s’applique-t-il uniquement à la formation des lobes des cellules du pavé ou peut-il également expliquer la croissance d’autres types de cellules ? (ii) comment la déméthylestérification asymétrique de l’HG est-elle régulée ? (iii) comment le processus d’expansion de la poutre s’intègre-t-il aux processus dépendant de la turgescence, comme la croissance acide, où la suppression des liaisons transversales qui relient les microfibrilles de cellulose porteuses (les « points chauds biomécaniques ») par des protéines de la paroi cellulaire, les « expansines » [28], conduit à la relaxation et à l’expansion de la paroi cellulaire ?
6. Connexion des échelles spatio-temporelles dans les poils absorbants
Pour répondre à ces questions, nous avons besoin d’un système simple, de préférence unicellulaire, et des procédures permettant des modifications et des lectures rapides afin que les effets puissent être observés avant que les processus de rétroaction ne se déclenchent. En outre, la modélisation informatique est nécessaire pour établir un pont entre les différentes échelles spatiales (molécules, assemblages de polymères, parois cellulaires, cellules) et temporelles (secondes, minutes, heures, jours) qui relient la physico-chimie des polymères aux propriétés cellulaires. Nous avons choisi le poil absorbant, qui est une excroissance des cellules de l’épiderme racinaire et un système « presque » unicellulaire [46]. L’analyse cinématique montre que le taux de croissance oscille avec un certain nombre de paramètres cellulaires (calcium cytosolique, pH de surface, niveaux d’espèces réactives de l’oxygène, charge de la paroi cellulaire), qui oscillent tous à la même fréquence (avec une période d’environ 30 s) mais avec des phases différentes [47]. Le pH de surface, par exemple, est un paramètre important, car presque toutes les activités enzymatiques dans la paroi cellulaire dépendent fortement du pH, avec par exemple des pH optimaux élevés et faibles pour les PME et les expansines respectivement. Pour étudier la causalité potentielle entre ces paramètres, il faut pouvoir manipuler un paramètre et observer les réponses à une échelle de temps inférieure à la période de 30 s. À cette fin, notre équipe développe actuellement des outils d’optogénétique pour l’activation ou l’inactivation rapide des activités enzymatiques par la lumière [48]. Par exemple, une pompe à protons d’Archae [49] activée par la lumière et exprimée dans les poils absorbants a permis une acidification de la surface du poil induite par la lumière en quelques secondes après le traitement lumineux. L’étape suivante consiste à évaluer l’impact des changements de pH sur les autres paramètres, les propriétés des parois cellulaires et le comportement de croissance. Ces approches vont maintenant être développées dans le cadre d’une bourse « starting grant » ERC accordée à Kalina Haas dans notre équipe.
7. L’héritage intellectuel de Michel Caboche
Trente ans après ma première rencontre avec Michel Caboche, et grâce à son intuition précoce et à son soutien infaillible, d’énormes progrès ont été réalisés dans notre compréhension du métabolisme des parois cellulaires végétales et de sa relation avec l’expansion cellulaire. L’utilisation de mutants d’Arabidopsis, dont nous avons été les pionniers avec l’équipe de Chris Somerville dans le Michigan [50], est devenue une pratique courante dans la recherche sur les parois cellulaires. Cela a permis de mieux comprendre la synthèse des polysaccharides de la paroi cellulaire et les mécanismes moléculaires qui sous-tendent la croissance des plantes. Alors que la composition de la paroi cellulaire peut varier considérablement d’un type de cellule à l’autre et d’une espèce végétale à l’autre [51], bon nombre des découvertes faites sur Arabidopsis se sont avérées pertinentes pour d’autres espèces végétales, y compris les espèces cultivées. Par exemple, la dissection des voies de biosynthèse de la lignine et de la pectine a conduit à des stratégies visant à améliorer la digestibilité de la biomasse du maïs pour les ruminants [52] ou des cultures énergétiques et des arbres pour la conversion en biocarburant de deuxième génération [53, 54]. Les connaissances sur la biosynthèse de la cellulose et sa relation avec l’élongation cellulaire sont utilisées pour améliorer la qualité de la fibre de coton [55]. La connaissance des déterminants structurels régissant les interactions cellulose–hémicellulose peut être exploitée pour la conception de nouveaux nanomatériaux [56]. La compréhension de la signalisation de l’intégrité de la paroi cellulaire conduit à de nouvelles stratégies de sélection ou d’ingénierie de la résistance aux pathogènes [57, 11]. Enfin, la compréhension des bases biophysiques de l’expansion des cellules végétales est essentielle pour le développement de modèles informatiques multi-échelles fiables permettant de prédire la croissance des plantes dans un climat changeant [12, 58] et pour la sélection de variétés végétales mieux adaptées [59]. Michel a élevé une importante famille d’enfants, d’arrière-petits-enfants et d’arrière-petits-enfants intellectuels et il n’y a aucune raison pour que cela ne continue pas à l’avenir ! Merci beaucoup pour tout cela Michel !
Conflit d’intérêt
L’auteur n’a aucun conflit d’intérêt à déclarer.




 CC-BY 4.0
CC-BY 4.0