1. Introduction
Metastatic progression—the last step of the multistage carcinogenesis process—is ultimately leading to the development of metastases that are usually responsible for the death of cancer patients [1, 2]. It begins when malignant cancer cells escape from the primary tumor and its microenvironment, invade the patient’s body through the lymphatic and/or the vascular systems, and finally reach distant organs. The colonization of these organs, an inefficient process requiring the conjunction of multiple helping factors, leads to the formation of secondary tumors called metastases. In support of Steven Paget’s “seed and soil” concept [3] there are considerable evidences to suggest that the development of metastasis is induced by intrinsic characteristics of tumor cells—notably their genetic and epigenetic alterations– as well as organ-specific environmental factors [4]. This so-called “organotropism” has been extensively studied from a medical, biological and chemical perspective in order to understand and anticipate tumor and metastatic progression in patients. Insofar as the metastases are largely incurable and currently very difficult to detect early enough during the natural history of the pathology, the exploration of the molecular and cellular pathways leading to the establishment of site-specific metastasis are thus in the forefront of cancer research. Other factors promote metastasis, among which the formation of permissive microenvironments, the so-called pre-metastatic niche priming. This mechanism occurs when factors secreted and released by the primary tumor create, in organs distant to the primary tumor, an environment where extravasation and growth of disseminating cancer cells are facilitated [5]. The discovery of the role of extracellular vesicles (EVs) in intercellular communication, and in our case of their role (in particular that of exosomes) in the promotion of the formation of the pre-metastatic niche (PMN) is the subject of intense research, including in our laboratory.
In recent years, we have seen the emergence of biomechanical studies—in addition to our own—aimed at understanding the contribution of fundamental driving forces and their involvement in each stage of the metastatic progression (Figure 1—highlighted in yellow). During growth of solid tumors for instance, the increased interstitial pressure has been shown to promote invasion and concomitantly limit access to chemotherapeutic molecules [6]. Later during the metastatic cascade—after invasion through complex extracellular matrix environments and intravasation through blood vessels of cancer cells evading from the primary tumor—the vascular tree will mechanically disseminate and guide circulating tumor cells to a first capillary bed, often a highly metastatic organ (i.e. the lungs in breast cancer, the liver in colorectal cancer). At the level of blood capillaries, hemodynamic parameters and the topography of the vessels themselves influence the sites of tumor cell arrest [7]. This is also probably true for soluble pro-metastatic factors—including EVs—secreted by the primary tumor, suggesting that the locations of the pre-metastatic niches must themselves respond to this set of physical constraints. Although these aspects are well described, their real biological impacts remain only poorly described in vivo, particularly in the later steps that occur in and off the bloodstream. Our laboratory primary objective is to continue to further elucidate the central role of biomechanics on the entire metastatic cascade, from the tumor progression to the metastasis itself (Figure 1—red star references). To this end, we combine state-of-the-art sophisticated tools (notably microfluidics-based), in vitro and in vivo models (mouse and zebrafish) with high-resolution imaging—such as correlated light and electron microscopy [8]—and biophysical approaches to mimic pathological situations highly relevant to cancer research. In doing so, we aim to ultimately identify innovative therapeutic alternatives.
Biomechanics of the metastatic cascade: a schematic representation of the path of cancer cells and extracellular vesicles during the cascade of events leading to the formation of metastases. The nine major steps are indicated in black on a white background, large font, and are referenced in the text. The biomechanical forces involved are highlighted in yellow. There are two legends on the right: the first one on top gives the references of the laboratory studies (red stars, numbered). A second one on the bottom references the types of cells and factors.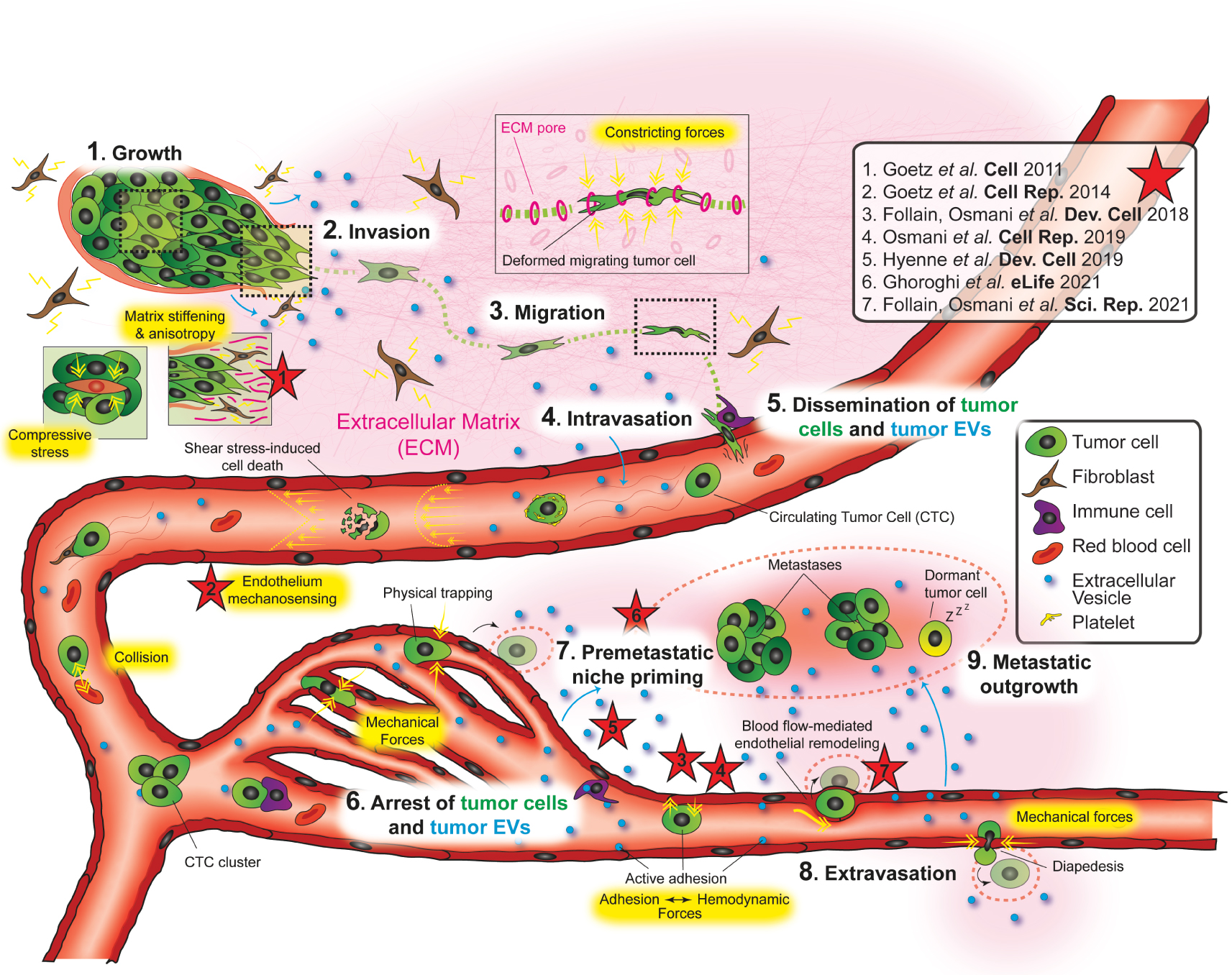
2. Forces that shape tumors and its microenvironment (TME)
A primary tumor and its highly-plastic microenvironment (TME) form an intricate non-homogeneous structure composed of different elements: the cancer cells themselves, a broad spectrum of stromal cells that can be activated including notably cancer-associated fibroblasts (CAFs), immune cells, and the lymphatic and blood vessels. It also includes the extracellular matrix (ECM) which contains, in addition to fiber-like molecules such as collagen and fibronectin, cell-secreted products (i.e. cytokine, chemokines, extracellular vesicles), various metabolites, and present hypoxic and acidic properties [4]. The growth of the primary tumor (Figure 1—1. Growth) results from uncontrolled proliferation in a healthy tissue and creates solid stress, which in turn induces various forces and tensile stress around and within the tumor itself [9]. This, in conjunction with the activation of neighboring stromal cells with high contractibility potential, results in the extracellular matrix becoming significantly stiffer and anisotropic, a feature correlated with a malignant tumor phenotype. We, and others, have previously demonstrated that the contractility of these stromal cells is a key factor in metastatic progression. In particular, we observed that Caveolin-1—a multifunctional scaffolding protein associated with cell-surface caveolae [10]—is a major regulator of tumor cell invasion and subsequent metastasis (Figure 1—2. Invasion) through the control of focal adhesion dynamics within tumor cells [11] and the biomechanical remodeling of the tumor-associated microenvironment by stromal cells [12]. The microenvironment of the tumor, influenced by the increased forces and abnormal fluids flows, will gradually transition from an anti-malignancy to a pro-malignancy behavior [13], promote the migration of cancer cells through the extracellular matrix (Figure 1—3. Migration), their intravasation in the body circulatory systems (Figure 1—4. Intravasation) and/or by lymphatic diffusion, and ultimately trigger circulating cancer cells (CTCs) dissemination (Figure 1—5. Dissemination). On a side note, while angiogenesis and lymphangiogenesis of the primary tumor play a potentiating role [14], tumor dissemination is an event that can also be observed in early lesions [7]. In conclusion, identifying and characterizing the flow-based mechanical constraints inherent to the tumor progression and metastasis cascade is of the utmost importance [15] and at the heart of our laboratory’s efforts [7].
To understand the mechanical forces at work, it is necessary to consider the primary tumor and TME irrigating fluids, namely the interstitial fluid, the lymph and the blood circulation. Each has its own biochemical characteristics, cellular content and flow patterns. The interstitial fluid, originating from blood capillaries’ leakiness and surrounding the cells, has a laminar flow heading towards the lymphatic draining sites. In a primary tumor, such flow is driven by the decreasing interstitial pressure gradient directed outward from its center (schematically its highest-pressure point). Lymphatic vessels exhibit a weakly pulsatile laminar flow, draining material from the primary tumor outward to the lymph nodes. Finally, the blood system, which presents different types of vessels (capillaries, veins and arteries), irrigates the primary tumor and delivers oxygen but also connects the growing tumor to distant parts of the organism. While capillaries and veins present a laminar flow of low to medium intensity, and a rather reduced pulsativity, they are supply and dissemination routes of the primary tumor (as illustrated in Figure 1), a phenomenon reinforced by their neo-formations following the release of pro-angiogenic factors from the tumor and its TME. The arteries present a laminar or turbulent flow of high intensity as well as a strong pulsativity and also participate to this process. Arterial circulation is a particularly hostile environment for the propagation of CTCs, since they exhibit the highest shear stresses [7]. Altogether, lymph and blood circulation offer optimal platforms to tumor cells for colonizing distant lands. Remarkably, CTCs are not the only ones to disseminate through these fluids and vasculatures: other tumor-secreted factors such as extracellular vesicles, some of which have pro-metastatic properties, use similar strategies to the benefit of metastatic fitness of CTCs.
3. The pre-metastatic niche (PMN) priming
Lymphatic and blood vessels allow the dissemination of various tumor-secreted factors such as cytokines, chemokines, growth factors, matrix metalloproteinases, circulating tumor DNA, antigens and extracellular vesicles (Figure 1—EVs, in blue) [16, 17]. Given their abundance in the body fluids of patients and their short half-life, it is likely that the primary tumor and its TME release them consistently and regularly. Yet, this remains poorly understood and should provide fertile grounds for future research. These tumor-secreted factors are subjected to hemodynamic constraints [18]—similarly to CTCs—and may arrest in various metastasis-free organs where they can locally modify the microenvironment and create so-called “pre-metastatic niches” (PMNs), which are ideal sites for CTC targeting and metastases formation (Figure 1—7. Premetastatic niche priming). Extracellular vesicles (EVs) in particular—small lipid bilayer particles that serve as signaling cargoes and which can be quickly cleared from the blood by intravascular macrophages/monocytes [18] and endothelial cells of the PMNs—have been demonstrated to exhibit specific organotropism depending on their primary tumor of origin, a feature made possible by the exposure of a variable repertoire of surface adhesion molecules [19]. Because they are transported by the blood flow, these non-inert circulating objects may “stop” in specific vascular regions as a function of their adhesive potential and the hemodynamic forces at play [18]. In relation to this mechanism, we have recently demonstrated that the Ral GTPases control the biogenesis, the secretion and the content of tumor extracellular vesicles [20] that favor tumor metastasis in mouse syngeneic models of breast cancer [21]. It appears thus likely that the formation of the PMNs depends not only on physical factors such as the architecture, permeability, leakiness, local flux and hemodynamic forces existing in the vasculatory system, but also on biological factors such as cell-adhesion molecules or intravesicular cargoes (i.e. proteins or nucleic acids) that make these extracellular vesicles important actors of the metastatic cascade. It is interesting to note at this point that EVs and CTCs might share similar targeting strategies for colonizing distant organs. Subsequently to the PMN priming process, cancer cells that have completed their migration and intravasation steps will be able to begin their intravascular journey as “circulating tumor cells” (CTC) until reaching their final destination.
4. Intravascular journey of a CTCs: flow forces, adhesion and extravasation
Steven Paget’s concept of “seed and soil” [3]—while remaining a central principle—was somewhat challenged by James Ewing (as early as 1928) and Dale Coman [22] by the introduction of the concept that the mechanics of the bloodstream were responsible for the dissemination of tumors to secondary organs followed by the demonstration that the frequency of occurrence of metastases and the vascular architecture as well as the capillary nature of the vessels in the heavily affected target organs were correlated [23]. Hematogenous circulation mechanics appeared thus responsible for the distribution of tumor cells in target organs. These two models, which may appear to be independent or even contradictory, actually represent two aspects of a single combinatorial “bio-mechanical” phenomenon. Indeed, although the non-specific and mechanical arrest of CTCs is an existing mechanism, the fate of these depends also on the organ in which they are located [24]. Numerous works, including our own, have since demonstrated that the metastatic process results from multifactorial physical and biochemical selective events where fluid biomechanics is an essential element [4, 7]. As soon as a cancer cell escapes from the primary tumor, intravasates in the blood circulation and becomes a CTC, an essential parameter for its survival and intravascular arrest is the shear stress, which depends on the fluid viscosity and the velocity gradient. Concretely, the more a CTC moves away from the center of the vessel—which it does naturally thanks to its margination properties—the more it will be deformed by the shearing phenomenon (this is especially true in blood due to its high viscosity) (Figure 1—5. Dissemination, shear stress-induced cell death). When entering the lymphatic or venous system, the shear stress remains low and the friction with the membrane of the vascular endothelium presumably harmless. Some CTCs will succeed in reaching the arteries, where the shear stress is high and where the risks of collision are statistically important: there, cells might undergo deformation, fragmentation and ultimately death [25]. This bottleneck results in the selection of CTCs with the most suitable properties for their survival—both physico-chemically and physiologically with reported modification of genes expression [26]—, and promotes their patterning into more resistant cell clusters, either among themselves as CTC clusters [27] or in association with other cell types (fibroblasts, neutrophils or blood platelets) [7] (Figure 1—5. Dissemination, illustrated). CTCs that have survived collision events, shear stress, and escape the immune system during their migration will exploit their adhesive potential and the hemodynamic properties of the vessels that carry them to colonize specific and permissive regions [28, 29], presumably PMNs in vivo. However, it is not so much when the CTCs are free within the circulation that they undergo the greatest stress, but when they attach and try to extravasate: one indication is that upon injection of tumor cells into the afferent vessel of metastatic organs, although 80% of the cells are thought to stably arrest one day after injection, less than 4% of injected cells efficiently form metastatic foci [30]. Although the intravascular arrest process of CTCs can occur passively by physical occlusion of small capillaries [31] (Figure 1—6. Arrest, physical trapping), which is currently a subject of research of our laboratory, the active adhesion to the vessel wall has been also reported to participate—at least in part—to further extravasation [28]. Adhesion between CTCs and the endothelium of the blood vasculature is only possible if the binding forces (i.e. ligand—receptor interaction) between them is greater than the forces exerted by the flow and shear stress [29] (Figure 1—8. Extravasation, active adhesion). This essential step can be influenced by the physicochemical characteristics of the vascular wall, the viscoelastic properties of the CTCs, but also by the homogenous or polarized distribution of the ligands and receptors. Different mechanisms/models—though not necessarily exclusive—have been proposed to describe the arrest and extravasation steps of CTCs. They could follow strategies similar to those of leukocytes, namely a rolling along the endothelial wall and then a (paracellular or transcellular) diapedesis step (Figure 1—8. Extravasation, diapedesis). The formation of “low adhesive strength—rapid activation” followed by “higher adhesive strength—slow activation” ligand–receptor bonds through a tug-of-war with blood flow has been documented [28, 29], and could explain both the rolling and arrest. However, our own observations tend to suggest that CTCs arrest intravascularly rather abruptly, with a risk of detachment: more work is thus needed to clarify this behavior. Furthermore, we demonstrated that CTCs do not only use diapedesis to leave the bloodstream and form secondary tumor foci: they can also use a flow-dependent endothelial remodeling mechanism [28] (Figure 1—8. Extravasation, endothelial remodeling), which is characterized by the formation of protrusions leading to the creation of new vascular lumens (pocketing), and the passive exclusion of CTCs from the vascular environment. Indeed, the vascular endothelium displays considerable mechano-sensing abilities that make it likely to sense, react and adapt to any conditions [32]. In the context of intravascular CTC dissemination, we recently observed that the VEGFR2-dependent pathway as a signaling node sensitive to flow forces and driver of tumor metastasis through endothelial remodeling [33]. Doing so, we identified a potential therapeutical target in the fight against tumor metastases. Finally,—although dormancy phenomena (ranging from a few hours to years) have been reported [34]—the CTC will eventually initiate extravascular proliferation to form a secondary tumor called metastases (Figure 1—9. Metastatic outgrowth). The proliferation efficiency will arguably depend on the metastatic microenvironment characteristics, and presumably on its further remodeling by pro-tumor factors such as EVs. Then, the new-formed metastases will, in turn, potentially initiate their own process of tumor progression and metastasis in the manner of the primary tumor, and dramatically accelerate the worsening of the cancer patient’s health condition.
5. Conclusion and perspectives
Our ability to effectively treat cancer depends in large part on our ability to decipher, correctly diagnose and prevent cancer progression and metastasis. In this regard, research on the role played by mechanical forces in these processes is fundamental and complementary to other approaches. The different body fluids, due to the types of flows that animate them and their resulting constraints (notably shear stress in blood circulation), are responsible for the dissemination of secreted tumor factors and CTCs. They play a central role in the selection and preparation of pre-metastatic niche for the formation of metastases, thus preparing an ideal soil. They are also key elements in selecting CTCs capable of surviving during the metastatic process, whether during their migration, adhesion, arrest or extravasation—each of them requiring biomechanical and physiological adaptations—thus carrying the metastatic seed. We recently demonstrated that fluid forces are also key in activating flow sensing receptors (in our models, but presumably in cancer patients PMN as well) and promote extravasation processes and thus metastasis. The pervasiveness of biomechanics in solid cancers (some elements of which also apply to blood cancers) makes research efforts in this area relevant. Although many studies have focused in the past decade on understanding forces within the primary tumor, more work is needed to understand, for example, how these can tune the secretion and nature of tumor-promoting factors such as extracellular vesicles. To understand how shear stress and flow forces impact the secretion, dissemination and uptake of factors secreted by the primary tumor and its TME, and to what extent they are involved in their cancer-dependent organotropism, are major challenges. Furthermore, how mechanical properties of CTCs themselves impact their metastatic fitness is conceptually appealing and thus studied in our laboratory. A detailed understanding of the forces at play could allow the development of innovative therapeutics taking advantage of biomechanical constraints to specifically target pre-metastatic niches—in the manner of factors secreted by tumors, i.e. engineered drug delivery EVs—and block or delay their establishment and subsequent endothelial remodeling and metastasis. The fragility of CTCs to shear stress must also be considered: if the use of drugs targeting blood pressure does not appear to be in the best interest of a cancer patient, tools allowing their continuous removal from the blood are already being developed [35] and more work is needed to understand whether their mechanical profiles are involved in such behavior. Understanding the biomechanics at work in a patient will also require considering the parameters acting on them. The physical/physiological characteristics of a patient—in particular age [36]—the potential effects of the treatments followed, and finally their evolution during the natural history of the pathology are all elements that could enable more efficient and personalized therapies. Another axis is the study of the effect of factors secreted by tumor and non-tumor cells, of their possible pro- vs. anti-tumor competition during the metastatic cascade, as well as their potential involvement in a biomechanical modification of the PMN.
Acknowledgments
We thank particularly Vincent Hyenne, Naël Osmani and Sébastien Harlepp, but also all members of Jacky G. Goetz’s team for their discussions, explanations and ideas to improve the manuscript. Florent Colin is funded by the NANOTUMOR Consortium (PFA), a program from ITMO Cancer of AVIESAN (Alliance Nationale pour les Sciences de la Vie et de la Santé, National Alliance for Life Sciences and Health) within the framework of the Cancer Plan (France). Valentin Gensbittel is funded by Région Alsace—Inserm. Jacky G. Goetz is a Research Director at Inserm and 2020 Grand Prize of Cancerology of the “Fondation Del Duca” (Académie de Sciences, France). Work in the lab of Jacky G. Goetz is mostly supported by the INCa (Institut National Du Cancer), La Ligue contre le Cancer, the ARC Foundation, the FRM (Fondation pour la Recherche Médicale), Le Plan Cancer, the Region Est, the INSERM and the University of Strasbourg.
French version
1. Introduction
La progression métastatique — la dernière des étapes du processus de carcinogenèse — conduit finalement au développement de métastases qui sont généralement responsables de la mort des patients atteints de cancer [1, 2]. Le processus commence lorsque des cellules cancéreuses malignes s’échappent de la tumeur primaire et de son microenvironnement, envahissent le corps du patient par les systèmes lymphatique et/ou vasculaire, et atteignent finalement des organes distants. La colonisation de ces organes, un processus inefficace nécessitant la conjonction de multiples facteurs facilitateurs, conduit à la formation de tumeurs secondaires appelées métastases. A l’appui du concept de « graine et sol » de Steven Paget [3], de nombreuses preuves suggèrent que le développement des métastases est induit par les caractéristiques intrinsèques des cellules tumorales — notamment leurs altérations génétiques et épigénétiques — ainsi que par des facteurs environnementaux spécifiques aux organes [4]. Cet « organotropisme » a été largement étudié d’un point de vue médical, biologique et chimique afin de comprendre et d’anticiper la progression des tumeurs et des métastases chez les patients. Dans la mesure où les métastases sont en grande partie incurables et encore actuellement difficiles à détecter suffisamment tôt au cours de l’histoire naturelle de la pathologie, l’exploration des voies moléculaires et cellulaires conduisant à l’établissement de métastases dans des organes / sites spécifiques est donc au premier plan de la recherche sur le cancer. D’autres facteurs favorisent les métastases parmi lesquels le mécanisme de formation de microenvironnements permissifs appelés niches pré-métastatiques. Ce mécanisme se produit lorsque des facteurs sécrétés et libérés par la tumeur primaire créent, dans des organes distants de la tumeur primaire, un environnement où l’extravasation et la croissance des cellules cancéreuses disséminées sont facilitées [5]. La découverte du rôle des vésicules extracellulaires (VEs) dans la communication intercellulaire, et dans notre cas de leur rôle (en particulier celui des exosomes) dans la promotion de la formation de la niche pré-métastatique (PMN) fait l’objet d’intenses recherches, y compris dans notre laboratoire.
Biomécanique de la cascade métastatique : représentation schématique du parcours des cellules cancéreuses et des vésicules extracellulaires au cours de la cascade d’événements conduisant à la formation de métastases. Les neuf étapes majeures sont indiquées en noir sur fond blanc, en gros caractères, et sont référencées dans le texte. Les forces biomécaniques impliquées sont mises en évidence en jaune. Il y a deux légendes sur la droite : la première en haut donne les références des études de laboratoire (étoiles rouges, numérotées). Une deuxième légende, en bas, donne les références des types de cellules et de facteurs.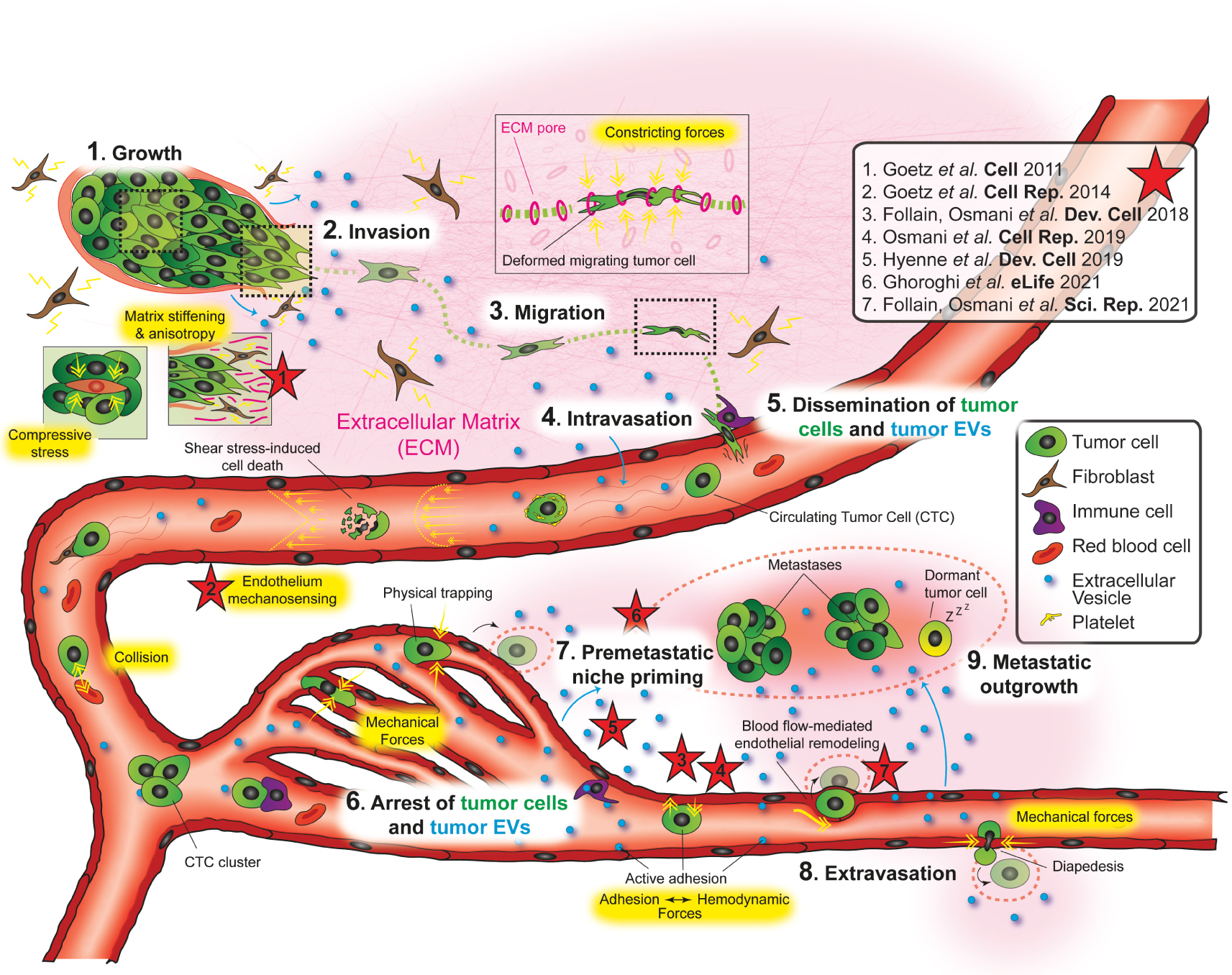
Ces dernières années, nous avons assisté à l’émergence d’études biomécaniques — en plus des nôtres — visant à comprendre la contribution des forces mécaniques fondamentales et leur implication dans chaque étape de la progression métastatique (Figure 1 — surligné en jaune). Pendant la croissance des tumeurs solides, par exemple, il a été démontré que l’augmentation de la pression interstitielle favorise l’invasion et limite simultanément l’accès aux molécules chimiothérapeutiques [6]. Plus tard, au cours de la cascade métastatique — après l’invasion à travers des environnements complexes de la matrice extracellulaire et l’intravasation à travers les vaisseaux sanguins des cellules cancéreuses qui ont échappé à la tumeur primaire — le réseau vasculaire va disséminer mécaniquement et guider les cellules tumorales circulantes vers un premier lit capillaire, souvent un organe hautement métastatique (par exemple les poumons dans le cancer du sein, le foie dans le cancer colorectal). Au niveau des capillaires sanguins, les paramètres hémodynamiques et la topographie des vaisseaux eux-mêmes influencent les sites d’arrêt des cellules tumorales [7]. Ceci est probablement aussi vrai pour les facteurs solubles pro-métastatiques — y compris les VEs — sécrétés par la tumeur primaire, ce qui suggère que les emplacements des niches pré-métastatiques doivent eux-mêmes répondre à cet ensemble de contraintes physiques. Bien que ces aspects soient bien décrits, leurs impacts biologiques réels ne sont que peu décrits in vivo, en particulier dans les étapes ultérieures qui se produisent dans et hors de la circulation sanguine. L’objectif principal de notre laboratoire est de continuer à élucider le rôle central de la biomécanique sur l’ensemble de la cascade métastatique, de la progression de la tumeur à la métastase elle-même (Figure 1 — références en étoile rouge). À cette fin, nous combinons des outils sophistiqués de pointe (notamment basés sur la microfluidique), des modèles in vitro et in vivo (souris et poisson-zèbre) avec une imagerie à haute résolution — comme la microscopie optique et électronique corrélée ou microscopie corrélative [8] — et des approches biophysiques pour imiter des situations pathologiques très pertinentes pour la recherche sur le cancer. Ce faisant, nous visons à identifier des alternatives thérapeutiques innovantes.
2. Les forces qui façonnent les tumeurs et leur microenvironnement (TME)
Une tumeur primaire et son microenvironnement (TME) hautement plastique forment une structure complexe et non homogène composée de différents éléments : les cellules cancéreuses elles-mêmes, un large éventail de cellules stromales qui peuvent être activées, notamment les fibroblastes associés au cancer (CAFs), les cellules immunitaires et les vaisseaux lymphatiques et sanguins. Elle comprend également la matrice extracellulaire (MEC) qui contient, outre des molécules fibreuses telles que le collagène et la fibronectine, des produits sécrétés par les cellules (c’est-à-dire des cytokines, des chimiokines, des vésicules extracellulaires), divers métabolites, et présente des propriétés hypoxiques et acides [4]. La croissance de la tumeur primaire (Figure 1 — 1. Growth) résulte d’une prolifération incontrôlée dans un tissu sain et crée un stress solide, qui à son tour induit diverses forces et tensions autour et à l’intérieur de la tumeur elle-même [9]. Ce phénomène, associé à l’activation des cellules stromales voisines à fort potentiel de contractilité, a pour conséquence de rendre la matrice extracellulaire nettement plus rigide et anisotrope, une caractéristique corrélée à un phénotype tumoral malin. Nous et d’autres avons précédemment démontré que la contractilité de ces cellules stromales, les CAFs, est un facteur clé dans la progression métastatique. Nous avons notamment observé que la cavéoline-1 — une protéine d’échafaudage multifonctionnelle associée aux cavéoles de la surface cellulaire [10] — est un régulateur majeur de l’invasion des cellules tumorales et des métastases qui s’ensuivent (Figure 1 — 2. Invasion) par le biais du contrôle de la dynamique des adhésions focales au sein des cellules tumorales [11] et du remodelage biomécanique du microenvironnement associé à la tumeur par les cellules stromales ou CAFs [12]. Le microenvironnement de la tumeur, influencé par les forces accrues et les flux de fluides anormaux, passe progressivement d’un comportement anti-maligne à un comportement pro-maligne [13], favorise la migration des cellules cancéreuses à travers la matrice extracellulaire (Figure 1 — 3. Migration), leur intravasation dans les systèmes circulatoires du corps (Figure 1 — 4. Intravasation) et/ou par diffusion lymphatique, et déclenche finalement la dissémination des cellules cancéreuses circulantes (CTCs) (Figure 1 — 5. Dissémination). Par ailleurs, alors que l’angiogenèse et la lymphangiogenèse de la tumeur primaire jouent un rôle de potentialisation [14], la dissémination tumorale est un événement qui peut également être observé dans les lésions précoces [7]. En conclusion, l’identification et la caractérisation des contraintes mécaniques liées à l’écoulement, inhérentes à la cascade de progression tumorale et de métastases sont de la plus haute importance [15] et sont au cœur des efforts de notre laboratoire [7].
Pour comprendre les forces mécaniques à l’œuvre, il est nécessaire de considérer les fluides d’irrigation de la tumeur primaire et de la TME, à savoir le fluide interstitiel, la lymphe et la circulation sanguine. Chacun d’entre eux possède ses propres caractéristiques biochimiques, son contenu cellulaire et ses schémas d’écoulement. Le fluide interstitiel, provenant de la fuite des capillaires sanguins et entourant les cellules, a un flux laminaire se dirigeant vers les sites de drainage lymphatique. Dans une tumeur primaire, ce flux est entraîné par le gradient de pression interstitielle décroissant dirigé vers l’extérieur à partir de son centre (schématiquement, son point de pression le plus élevé). Les vaisseaux lymphatiques présentent un flux laminaire faiblement pulsatile, drainant la matière de la tumeur primaire vers les ganglions lymphatiques. Enfin, le système sanguin, qui présente différents types de vaisseaux (capillaires, veines et artères), irrigue la tumeur primaire et fournit de l’oxygène mais relie également la tumeur en croissance à des parties distantes de l’organisme. Alors que les capillaires et les veines présentent un flux laminaire d’intensité faible à moyenne, et une pulsativité plutôt réduite, ils sont des voies d’approvisionnement et de dissémination de la tumeur primaire (comme illustré dans la Figure 1), un phénomène renforcé par leurs néo-formations suite à la libération de facteurs pro-angiogéniques de la tumeur et de sa TME. Les artères présentent un flux laminaire ou turbulent de haute intensité ainsi qu’une forte pulsativité et participent également à ce processus. La circulation artérielle est un environnement particulièrement hostile à la propagation des CTCs, car elle présente les contraintes de cisaillement les plus élevées [7]. Dans l’ensemble, les circulations lymphatique et sanguine offrent aux cellules tumorales des plateformes optimales pour coloniser des terres lointaines. Il est remarquable que les CTCs ne soient pas les seules à se disséminer par ces fluides et ces vaisseaux : d’autres facteurs sécrétés par les tumeurs, comme les vésicules extracellulaires, dont certains ont des propriétés pro-métastatiques, utilisent des stratégies similaires au profit de la capacité métastatique des CTCs.
3. La formation de la niche pré-métastatique (PMN)
Les vaisseaux lymphatiques et sanguins permettent la dissémination de divers facteurs sécrétés par la tumeur tels que les cytokines, les chimiokines, les facteurs de croissance, les métalloprotéinases matricielles, l’ADN tumoral circulant, les antigènes et les vésicules extracellulaires (Figure 1 — EVs, en bleu) [16, 17]. Étant donné leur abondance dans les fluides corporels des patients et leur courte demi-vie, il est probable que la tumeur primaire et sa TME les libèrent de manière constante et régulière. Pourtant, cela reste mal compris et devrait fournir un terrain fertile pour de futures recherches. Ces facteurs sécrétés par la tumeur sont soumis à des contraintes hémodynamiques [18] — tout comme les CTCs — et peuvent s’arrêter dans divers organes exempts alors de métastases où ils peuvent modifier localement le microenvironnement et créer des « niches prémétastatiques » (PMNs), qui sont des sites idéaux pour le ciblage des CTCs et la formation de métastases (Figure 1 — 7. Premitastatic niche priming). Il a été démontré que les vésicules extracellulaires (VEs) en particulier — de petites particules entourées d’une bicouche lipidique qui servent de transporteurs et qui peuvent être rapidement éliminées du sang par les macrophages/monocytes intravasculaires [18] ou captées par les cellules endothéliales des PMNs — présentent un organotropisme spécifique en fonction de leur tumeur d’origine primaire, une caractéristique rendue possible par l’exposition d’un répertoire variable de molécules d’adhésion de surface [19]. Parce qu’ils sont transportés par le flux sanguin, ces objets circulants non inertes peuvent « s’arrêter » dans des régions vasculaires spécifiques en fonction de leur potentiel adhésif et des forces hémodynamiques en jeu [18]. En relation avec ce mécanisme, nous avons récemment démontré que les GTPases de la famille Ral contrôlent la biogenèse, la sécrétion et le contenu des vésicules extracellulaires tumorales [20] qui favorisent les métastases tumorales dans des modèles murins syngéniques de cancer du sein [21]. Il semble donc probable que la formation des PMNs dépend non seulement de facteurs physiques tels que l’architecture, la perméabilité, les fuites, les flux locaux et les forces hémodynamiques existant dans le système vasculaire, mais aussi de facteurs biologiques tels que les molécules d’adhésion cellulaire ou les cargaisons vésiculaires (c’est-à-dire les protéines ou les acides nucléiques) qui font de ces vésicules extracellulaires des acteurs importants de la cascade métastatique. Il est intéressant de noter à ce stade que les VEs et les CTCs pourraient partager des stratégies de ciblage similaires pour coloniser des organes distants. Après le processus d’amorçage des PMN, les cellules cancéreuses qui ont terminé leurs étapes de migration et d’intravasation pourront commencer leur voyage intravasculaire en tant que « cellules tumorales circulantes » (CTC) jusqu’à atteindre leur destination finale.
4. Voyage intravasculaire d’une CTC : forces d’écoulement, adhésion et extravasation
Le concept de Steven Paget de « graine et sol » [3] — tout en restant un principe central — a été quelque peu remis en question par James Ewing (dès 1928) et Dale Coman [22] par l’introduction du concept selon lequel la mécanique de la circulation sanguine était responsable de la dissémination des tumeurs dans les organes secondaires, suivie de la démonstration de la corrélation entre la fréquence d’apparition des métastases et l’architecture vasculaire ainsi que la nature capillaire des vaisseaux dans les organes cibles fortement touchés [23]. La mécanique de la circulation hématogène semblait donc responsable de la distribution des cellules tumorales dans les organes cibles. Ces deux modèles, qui peuvent sembler indépendants, voire contradictoires, représentent en fait deux aspects d’un même phénomène « bio-mécanique » combinatoire. En effet, bien que l’arrêt mécanique et non spécifique des CTCs soit un mécanisme existant, le destin de ces dernières dépend également de l’organe dans lequel elles se trouvent [24]. De nombreux travaux, dont les nôtres, ont depuis démontré que le processus métastatique résulte d’événements sélectifs physiques et biochimiques multifactoriels où la biomécanique des fluides est un élément essentiel [4, 7]. Dès qu’une cellule cancéreuse s’échappe de la tumeur primaire, s’infiltre dans la circulation sanguine et devient une CTC, un paramètre essentiel pour sa survie et son arrêt intravasculaire est la contrainte de cisaillement, qui dépend de la viscosité du fluide et du gradient de vitesse. Concrètement, plus une CTC s’éloigne du centre du vaisseau — ce qu’il fait naturellement de par ses propriétés de margination — plus elle sera déformée par le phénomène de cisaillement (ceci est particulièrement vrai dans le sang en raison de sa forte viscosité) (Figure 1 — 5. Dissémination, mort cellulaire induite par la contrainte de cisaillement). Lors de la pénétration dans le système lymphatique ou veineux, la contrainte de cisaillement reste faible et la friction avec la membrane de l’endothélium vasculaire vraisemblablement inoffensive. Certaines CTCs parviendront à atteindre les artères, où la contrainte de cisaillement est élevée et où les risques de collision sont statistiquement importants : là, les cellules peuvent subir une déformation, une fragmentation et finalement la mort [25]. Ce goulot d’étranglement entraîne la sélection des CTCs ayant les propriétés les plus favorables à leur survie — tant sur le plan physico-chimique que physiologique, avec une modification de l’expression des gènes [26] — et favorise leur structuration en groupes cellulaires plus résistants, soit entre elles en tant que groupes de CTCs [27], soit en association avec d’autres types de cellules (fibroblastes, neutrophiles ou plaquettes sanguines) [7] (Figure 1 — 5. Dissémination, illustrée). Les CTCs qui ont survécu aux événements de collision, aux contraintes de cisaillement et qui échappent au système immunitaire au cours de leur migration vont exploiter leur potentiel adhésif et les propriétés hémodynamiques des vaisseaux qui les transportent pour coloniser des régions spécifiques et permissives [28, 29], vraisemblablement les PMNs in vivo. Cependant, ce n’est pas tant lorsque les CTCs sont libres dans la circulation qu’elles subissent le plus grand stress, mais lorsqu’elles se fixent et tentent de quitter la circulation par le processus d’extravasation : une indication est que lors de l’injection de cellules tumorales dans le vaisseau afférent d’organes métastatiques, bien que 80% des cellules soient censées s’arrêter de manière stable un jour après l’injection, moins de 4% des cellules injectées forment efficacement des foyers métastatiques [30]. Bien que le processus d’arrêt intravasculaire des CTCs puisse se produire de manière passive par l’occlusion physique dans des petits capillaires [31] (Figure 1 — 6. Arrest, physical trapping), dont l’impact est actuellement un sujet de recherche de notre laboratoire, l’adhésion active à la paroi du vaisseau a également été signalée comme favorisant — au moins en partie — l’extravasation [28]. L’adhésion entre les CTCs et l’endothélium du système vasculaire sanguin n’est possible que si les forces de liaison (c’est-à-dire l’interaction ligand–récepteur) entre eux sont supérieures aux forces exercées par le flux et la contrainte de cisaillement [29] (Figure 1 — 8. Extravasation, adhésion active). Cette étape essentielle peut être influencée par les caractéristiques physicochimiques de la paroi vasculaire, les propriétés viscoélastiques des CTCs, mais aussi par la distribution homogène ou polarisée des ligands et des récepteurs. Différents mécanismes/modèles — mais pas nécessairement exclusifs — ont été proposés pour décrire les étapes d’arrêt et d’extravasation des CTCs. Ils pourraient suivre des stratégies similaires à celles des leucocytes, à savoir un roulement le long de la paroi endothéliale puis une étape de diapédèse (paracellulaire ou transcellulaire) (Figure 1 — 8. Extravasation, diapedesis). La formation de liaisons ligand–récepteur de « faible force adhésive — activation rapide » suivie de « force adhésive plus élevée — activation lente » par un tiraillement avec le flux sanguin a été documentée [28, 29], et pourrait expliquer à la fois le roulement et l’arrêt. Cependant, nos propres observations tendent à suggérer que les CTCs s’arrêtent de manière intravasculaire plutôt abrupte, avec un risque de détachement : des travaux supplémentaires sont donc nécessaires pour clarifier ce comportement. De plus, nous avons démontré que les CTC n’utilisent pas seulement la diapédèse pour quitter la circulation sanguine et former des foyers tumoraux secondaires : ils peuvent également utiliser un mécanisme de remodelage endothélial dépendant du flux [28] (Figure 1 — 8. Extravasation, endothelial remodeling), qui se caractérise par la formation de protrusions conduisant à la création de nouvelles lumières vasculaires (pocketing), et l’exclusion passive des CTCs de l’environnement vasculaire. En effet, l’endothélium vasculaire présente des capacités de mécanosensibilité considérables qui lui permettent de détecter, de réagir et de s’adapter à toutes les conditions [32]. Dans le contexte de la dissémination intravasculaire des CTCs, nous avons récemment observé que la voie dépendante du VEGFR2 est un nœud de signalisation sensible aux forces d’écoulement et un moteur des métastases tumorales par le biais du remodelage endothélial [33]. Nous avons ainsi identifié une cible thérapeutique potentielle dans la lutte contre les métastases tumorales. Enfin, bien que des phénomènes de dormance (allant de quelques heures à plusieurs années) aient été rapportés [34], les CTCs vont finalement initier une prolifération extravasculaire pour former une tumeur secondaire appelée métastase (Figure 1 — 9. Croissance métastatique). L’efficacité de la prolifération dépendra sans doute des caractéristiques du microenvironnement métastatique, et vraisemblablement de son remodelage ultérieur par des facteurs pro-tumoraux tels que les VEs. Ensuite, les métastases nouvellement formées pourront, à leur tour, initier leur propre processus de progression tumorale et de métastase à la manière de la tumeur primaire, et accélérer considérablement l’aggravation de l’état de santé du patient cancéreux.
5. Conclusion et perspectives
Notre capacité à traiter efficacement le cancer dépend en grande partie de notre capacité à décrypter, diagnostiquer correctement et prévenir la progression du cancer et des métastases. A cet égard, la recherche sur le rôle joué par les forces mécaniques dans ces processus est fondamentale et complémentaire à d’autres approches. Les différents fluides corporels, de par les types d’écoulements qui les animent et les contraintes qui en résultent (notamment la contrainte de cisaillement dans la circulation sanguine), sont responsables de la dissémination des facteurs tumoraux sécrétés et des CTCs. Ils jouent un rôle central dans la sélection et la préparation de la niche pré-métastatique pour la formation des métastases, préparant ainsi un terrain idéal. Elles sont également des éléments clés dans la sélection des CTCs capables de survivre au cours du processus métastatique, que ce soit lors de leur migration, de leur adhésion, de leur arrêt ou de leur extravasation — chacune d’entre elles nécessitant des adaptations biomécaniques et physiologiques — portant ainsi la graine métastatique. Nous avons récemment démontré que les différentes forces présentes au sein des divers fluides corporels sont également essentielles à l’activation des récepteurs de détection du flux (dans nos modèles, mais probablement aussi dans les PMNs des patients cancéreux) et favorisent les processus d’extravasation et donc les métastases. L’omniprésence de la biomécanique dans les cancers solides (dont certains éléments s’appliquent également aux cancers du sang) rend les efforts de recherche dans ce domaine pertinents. Bien que de nombreuses études se soient concentrées au cours de la dernière décennie sur la compréhension des forces à l’intérieur de la tumeur primaire, des travaux supplémentaires sont nécessaires pour comprendre, par exemple, comment ces forces peuvent influencer la sécrétion et la nature des facteurs favorisant la tumeur, tels que les vésicules extracellulaires. Comprendre comment la contrainte de cisaillement et les forces d’écoulement ont un impact sur la sécrétion, la dissémination et l’absorption des facteurs sécrétés par la tumeur primaire et sa TME, et dans quelle mesure ils sont impliqués dans leur organotropisme (lui-même variable en fonction du cancer), sont des défis majeurs. En outre, la manière dont les propriétés mécaniques des CTCs elles-mêmes influent sur leur aptitude métastatique est conceptuellement intéressante et donc étudiée dans notre laboratoire. Une compréhension détaillée des forces en jeu pourrait permettre le développement de thérapies innovantes tirant parti des contraintes biomécaniques pour cibler spécifiquement les niches pré-métastatiques — en s’inspirant des facteurs sécrétés par les tumeurs et en désignant, par exemple, des VEs porteuses de médicaments — et bloquer ou retarder leur établissement, puis le remodelage endothélial et les métastases. La fragilité des CTCs à la contrainte de cisaillement doit également être prise en compte : si l’utilisation de médicaments ciblant la pression sanguine ne semble pas être dans le meilleur intérêt d’un patient cancéreux, des outils permettant leur élimination continue du sang sont déjà en cours de développement [35] et des travaux supplémentaires sont nécessaires pour comprendre si leurs profils mécaniques sont impliqués dans un tel comportement. Comprendre la biomécanique à l’œuvre chez un patient nécessitera également de considérer les paramètres qui agissent sur eux. Les caractéristiques physiques/physiologiques d’un patient — notamment l’âge [36] — les effets potentiels des traitements suivis, et enfin leur évolution au cours de l’histoire naturelle de la pathologie sont autant d’éléments qui pourraient permettre des thérapies plus efficaces et personnalisées. Un autre axe est l’étude de l’effet des facteurs sécrétés par les cellules tumorales et non tumorales, de leur éventuelle compétition pro- vs anti-tumorale au cours de la cascade métastatique, ainsi que de leur implication potentielle dans une modification biomécanique des PMNs.
Remerciements
Nous remercions particulièrement Vincent Hyenne, Naël Osmani et Sébastien Harlepp, mais aussi tous les membres de l’équipe de Jacky G. Goetz pour leurs discussions, explications et idées pour améliorer le manuscrit. Florent Colin est financé par le Consortium NANOTUMOR (PFA), un programme de l’ITMO Cancer d’AVIESAN (Alliance Nationale pour les Sciences de la Vie et de la Santé) dans le cadre du Plan Cancer (France). Valentin Gensbittel est financé par la Région Alsace — Inserm. Jacky G. Goetz est Directeur de Recherche à l’Inserm et Grand Prix 2020 de Cancérologie de la Fondation Del Duca (Académie de Sciences, France). Les travaux du laboratoire de Jacky G. Goetz sont principalement soutenus par l’INCa (Institut National Du Cancer), la Ligue contre le Cancer, la Fondation ARC, la FRM (Fondation pour la Recherche Médicale), Le Plan Cancer, la Région Est, l’Inserm et l’Université de Strasbourg.




 CC-BY 4.0
CC-BY 4.0