1 Introduction
Dans une note précédente, nous avons décrit une nouvelle méthode de préparation pour les complexes endoédriques atome de gaz rare–fullerène C60, basée sur l’utilisation d’un puissant faisceau de lumière, de longueur d’onde λ = 532 nm, provenant d’un laser Nd–YAG impulsionnel et doublé, pour exciter l’échantillon de C60 placé au sein d’un gaz rare comprimé à haute pression [1]. Cette méthode nous a permis d’obtenir des concentrations élevées en complexes endoédriques, allant jusqu’à 20%, alors que, dans leurs expériences, Saunders et al. n’obtenaient pas des concentrations supérieures à 0,5% [2].
Nous montrons dans la présente note que notre méthode de préparation peut aussi s’appliquer pour produire des complexes endoédriques gaz moléculaire–fullerène. Nous avons réalisé, par exemple, des expériences avec de l’hydrogène comprimé à haute pression pour traiter le fullerène C60, ce qui nous a permis de mettre en évidence le complexe endoédrique H2@C60, associé à du C60 hydrogéné.
2 Mode opératoire
En utilisant le même montage expérimental que celui décrit précédemment [1], nous avons traité à l’hydrogène comprimé, sous une pression de 0,1 GPa, un échantillon de C60 de 50 mg environ en masse. Ces produits présentaient au départ les concentrations suivantes : 99,99% pour le C60, que nous avons ensuite chauffé à 400 °C sous vide secondaire pendant 2 h, afin d’éliminer toute trace de solvant. Par ailleurs, la cuve haute pression a été soumise à un pompage sous vide secondaire pendant plusieurs heures, et le compresseur à membranes a été nettoyé au moyen de rinçages à l’hydrogène. Enfin, le faisceau laser, d’une énergie de l’ordre de 100 mJ par impulsion, était légèrement focalisé sur l’échantillon. L’expérience durait 5 h et, après récupération de la poudre traitée, était renouvelée afin d’améliorer encore le rendement de la méthode.
3 Résultats et discussion
La poudre de C60 récupérée après ces deux expériences successives présente une structure cristallographique identique à celle de la poudre de C60 non traitée, cubique à face centrée, avec un paramètre de maille égal à celui de la référence, dans la limite des erreurs d’expérience, tandis que, dans le cas du traitement avec l’hélium, nous avions observé une structure amorphe pour la poudre de C60 récupérée [1]. Nous pensons que cette différence de structure pourrait dépendre des interactions du C60 avec les modes rovibrationnels de H2, inexistantes avec les gaz atomiques.
Une analyse d’un échantillon de C60 traité sous H2 a été faite par RMN du proton à 400 MHz, en mode MAS, avec rotation de l’échantillon à la fréquence de 30 kHz. La Fig. 1 présente deux signaux, le spectre I se rapportant à l’échantillon conservé à l’air libre pendant plusieurs semaines, tandis que le spectre II a été obtenu avec un échantillon chauffé à 80 °C pendant quelques heures sous vide secondaire, afin d’éliminer toute trace d’eau et d’hydrogène interstitiel, et maintenu ensuite sous atmosphère d’argon. On voit sur cette figure que les structures du spectre II sont un peu moins nombreuses et mieux définies que celles du spectre I. Par ailleurs, le spectre II a pu être décomposé en six raies et un épaulement près du sommet du signal ; le Tableau 1 donne les intensités relatives de ces composantes, leurs positions et leurs largeurs, ainsi que la position de l’épaulement.

Spectres de résonance magnétique nucléaire du proton, en mode MAS et une fréquence de rotation de l’échantillon de 30 kHz, obtenus avec de la poudre de C60 traitée avec H2. Voir le texte pour les détails.
Caractérisation des six composantes et de l’épaulement, obtenues par analyse du spectre II de la Fig. 1, qui présente la RMN du proton pour le fullerène C60 traité avec H2.
| Numéro des composantes | Intensité en % des composantes | Position en ppm des composantes | Largeur en Hz des composantes |
| 1 | 4,2 | 6,9 | 398 |
| 2 | 1,9 | 2,3 | 131 |
| 3 | 43,7 | 1,0 | 581 |
| 4 | 0,8 | 4,2 | 71 |
| 5 | 18,4 | –2,8 | 4005 |
| 6 | 31,1 | 5,0 | 2719 |
| épaulement | — | 1,5 | — |
Nous proposons d’interpréter l’origine de ces diverses composantes de la manière suivante. Tout d’abord, la composante 3, située à 1 ppm et dont l’intensité est la plus grande, serait due au proton libre ou à la molécule H2 libre, dans la cage de la molécule de C60. Une interprétation similaire a été donnée dans le cas des couches de carbone amorphe hydrogéné [3], pour lesquelles les auteurs ont observé une raie fine, dont la position à 1,1 ppm est très proche de celle de la composante 3. Ensuite, les composantes 1,2 et 4, ainsi que l’épaulement, pourraient représenter le résultat du couplage entre les deux protons de la molécule H2 piégée dans la cage du C60, couplage lié à l’influence du potentiel d’interaction H2–C60. En effet, nous estimons que, si l’on accepte le rapprochement de notre hypothèse avec l’interprétation donnée par Henderson et al. pour rendre compte du spectre RMN du produit d’addition C60 H4 [4], nous pouvons comparer les caractéristiques des composantes citées ci-dessus à celles fournies par ces auteurs : (i) système de spins AA′BB′ centré à 5,03 ppm, alors que, dans notre cas, nous trouvons 5,27 ppm ; (ii) les quatre types d’interaction de deux spins ont des coefficients de couplage qui présentent une décroissance qualitativement en bon accord avec nos données (voir Tableau 2). En conséquence, suivant notre hypothèse, les deux protons de H2 seraient soumis à quatre types d’interactions au cours des mouvements de la molécule piégée dans la cage de C60, ce qui expliquerait l’existence des quatre structures observées.
Comparaison des caractéristiques des composantes 1, 2 et 4, ainsi que de l’épaulement, données dans le Tableau 1, avec l’interprétation du spectre RMN du composé C60H4 proposée par Henderson et al. [4].
| Type d'interaction de deux spins [4] | Coefficient de couplage (Hz) [4] | Numéros des composantes [ce travail] | Intensité relative en % | Position (ppm) | Largeur (Hz) |
| AB | 14,1 | 1 | 4,2 | 6,9 | 398 |
| BB′ | 9,8 | 2 | 1,9 | 2,3 | 131 |
| AA′ | 1,7 | 4 | 0,8 | 4,2 | 71 |
| AB′ | –0,2 | épaulement | — | 1,5 | — |
En ce qui concerne les deux composantes 5 et 6, elles sont beaucoup plus larges que les précédentes ; leur centre se situe à 2,1 ppm, valeur très proche de celle trouvée à 1,6 ppm pour la composante large, observée dans le cas des couches de carbone amorphe hydrogéné [3]. Nous proposons donc d’associer les deux composantes 5 et 6 à la présence dans notre échantillon de nombreuses liaisons C–H, les protons étant en forte interaction dipolaire.
Par ailleurs, l’existence de complexes endoédriques H2@C60, associés à du C60 hydrogéné, a été mise directement en évidence au moyen de la spectroscopie infrarouge par transformée de Fourier ; l’échantillon étudié était formé d’une couche de C60 traité avec H2 ou de C60 non traité, dont l’épaisseur était d’environ 0,1 mm, et qui était placée entre deux fenêtres de KBr. Ainsi, nous avons observé, pour la première fois à notre connaissance, la bande de vibration de la molécule H2 à 4139 cm–1, induite par les interactions moléculaires H2–C60 et déplacée vers les faibles fréquences d’environ 16 cm–1 (voir Fig. 2). Quatre faibles structures l’accompagnent, que nous proposons d’interpréter comme des bandes d’addition dont les fréquences correspondraient aux sommes de la fréquence de vibration de H2 avec celles des deux phonons et d’une vibration du C60 solide ; les valeurs de ces trois dernières fréquences ont été déterminées à basse température (55, 41 et 21 cm–1) [5], en bon accord avec celles données par la théorie [6], et se rapprochent assez bien de celles trouvées à partir de la Fig. 2 (62, 38 et 27 cm–1). On observe aussi, sur la Fig. 2, deux autres bandes, à 4392 et 4556 cm–1, que nous proposons d’interpréter comme des bandes d’addition dont les fréquences correspondraient aux sommes de la fréquence de vibration de H2 avec celles des modes de vibration 1Hg et 1Ag de la molécule de C60.
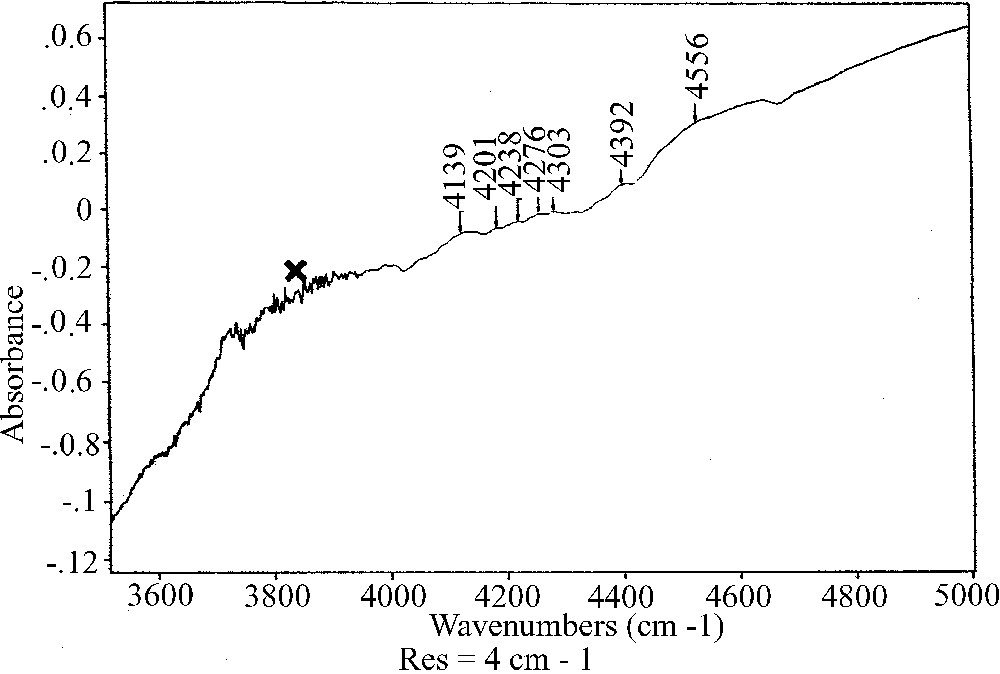
Spectre d’absorption infrarouge dans la région 3600–5000 cm–1 du C60 traité avec H2, obtenu par spectroscopie à transformée de Fourier et une accumulation de 1000 interférogrammes ; ce spectre a été rationalisé par rapport au C60 non traité. La croix désigne le restant d’absorption de la vapeur d’eau dû à un défaut dans le calcul de rationalisation.
En ce qui concerne le C60 hydrogéné, la Fig. 3 présente le spectre infrarouge caractéristique des liaisons C–H, dont les fréquences et attributions sont données dans le Tableau 3. En outre, nous avons observé deux bandes d’absorption à 1598 et 1075 cm–1, correspondant respectivement aux vibrations d’élongation de la double liaison C=C et de la simple liaison C–C. Enfin, la présence du C60 hydrogéné a pu être confirmée par la mise en évidence, dans l’ultraviolet lointain, d’une bande d’absorption très large dans la région 170–190 nm, à partir d’une solution très diluée dans le n-hexane, du C60 traité avec H2 (5 μg ml–1), comme le montre la Fig. 4 ; en revanche, aucune absorption n’a été trouvée dans cette même région spectrale avec le C60 non traité. Cette bande comporte deux composantes, l’une à 185 nm et l’autre à 177 nm, que nous proposons d’interpréter comme représentant deux transitions électroniques dans le groupe C–H, déplacées vers les grandes longueurs d’onde par rapport à celles observées pour la molécule C–H dans l’état isolé, respectivement à 169 et 155 nm [7].

Spectre d’absorption infrarouge dans la région 2600–3200 cm–1 du C60 traité avec H2, obtenu par spectroscopie à transformée de Fourier et une accumulation de 25 000 interférogrammes ; ce spectre a été rationalisé par rapport au C60 non traité.
Fréquences des bandes d’absorption du spectre infrarouge présenté sur la Fig. 3, et tentative d’attribution de ces bandes.
| Fréquence (cm–1) | Attribution |
| 2852 | sp3 CH2 (sym.) |
| 2872 | sp3 CH3 (sym.) |
| 2923 | sp3 CH2 (asym.) et sp3 CH |
| 2955 | sp3 CH3 (asym.) |
| 3043 | sp2 CH (arom.) |
| 3088 et 3128 | sp1 CH |
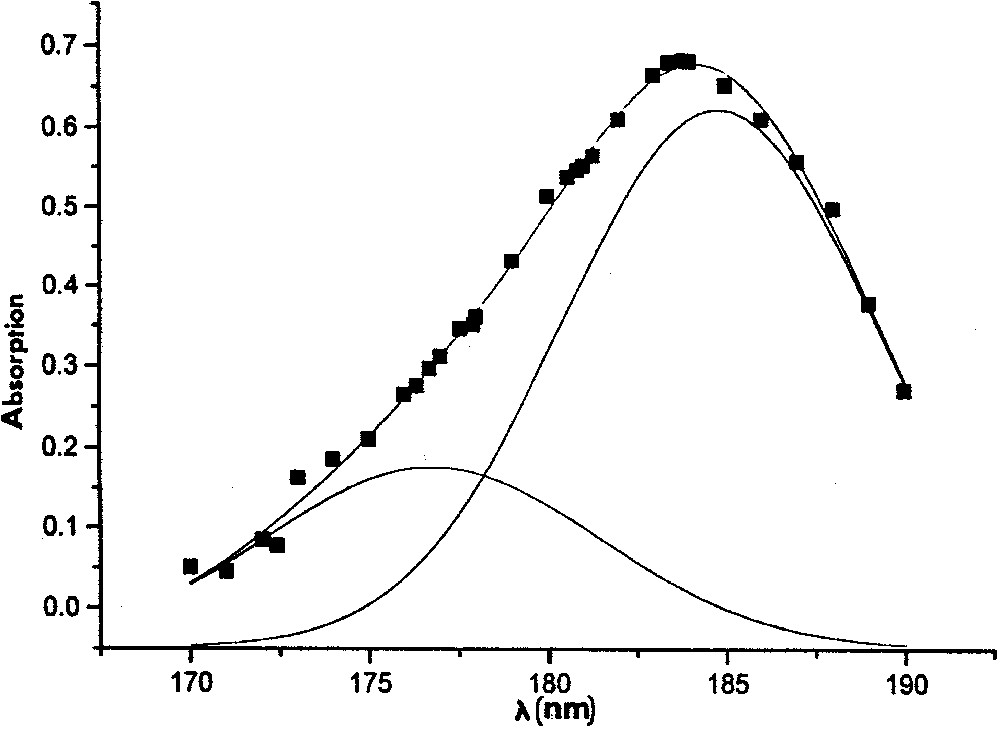
Spectre d’absorption, dans l’ultraviolet lointain, d’une solution très diluée de C60 traité avec H2 dans le n-hexane, à la concentration de 5 μg ml–1.
Par ailleurs, nous avons étudié le spectre d’absorption dans les régions visible et ultraviolet proche, pour les solutions très diluées dans le n-hexane du C60 traité avec H2 et du C60 non traité, avec la même concentration de 5 μg ml–1. Nous avons trouvé que, dans le cas du C60 traité avec H2, l’intensité de l’absorption était fortement diminuée, d’un facteur 10 environ par rapport à la référence du C60 non traité, ainsi que le montre la Fig. 5 dans la région de l’ultraviolet proche. Ce résultat est similaire à ceux que nous avons trouvés dans les traitements avec les gaz rares 4He et Ar, mais l’effet d’atténuation de l’absorption est beaucoup plus important avec la molécule diatomique H2 qu’avec ces deux gaz atomiques [1]. Pour expliquer ces phénomènes dans des échantillons contenant encore une proportion non négligeable de C60 qui n’a pas réagi avec le gaz comprimé, on pourrait avancer l’hypothèse suivante : les interactions dans les complexes influenceraient très fortement les structures électroniques du fullerène, masquant ainsi le phénomène normal d’absorption. Toutefois, il est évident qu’une étude approfondie ne pourrait être entreprise que sur des échantillons présentant une concentration très élevée en complexes. En outre, nous avons observé dans cette région spectrale des déplacements des bandes vers les grandes longueurs d’onde, croissant lorsque la longueur d’onde diminue, de 1,8 à 8,3 nm.
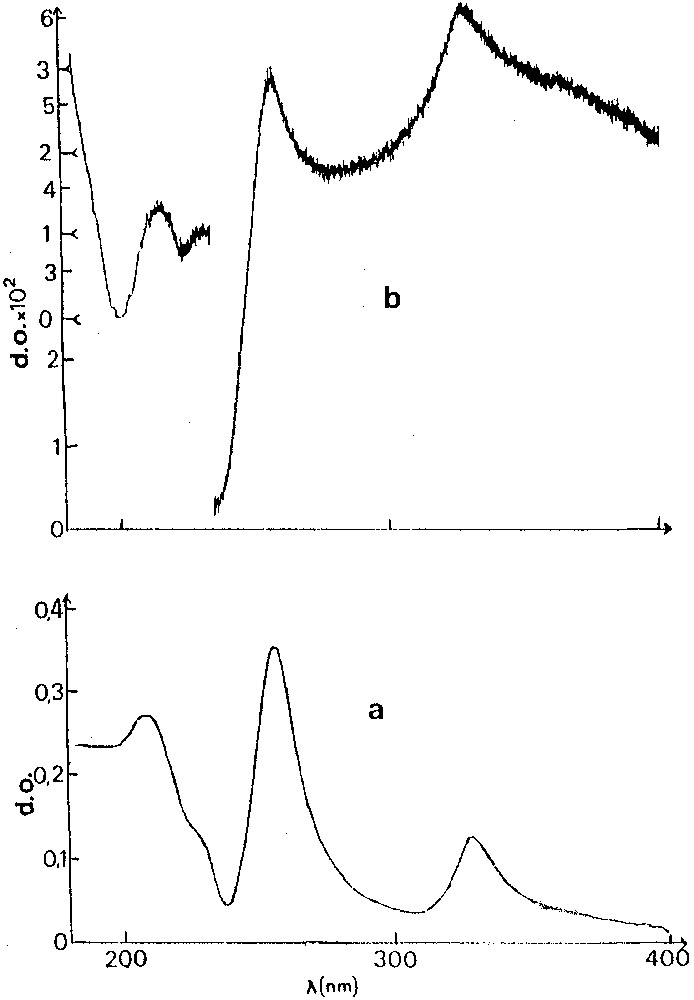
(a) Spectre d’absorption dans l’ultraviolet proche d’une solution très diluée de C60 non traité, dans le n-hexane à la concentration de 5 μg ml–1. (b) Spectre d’absorption dans l’ultraviolet proche d’une solution très diluée de C60 traité avec H2, dans le n-hexane à la concentration de 5 μg ml–1.
Enfin, sur le plan quantitatif, nous avons utilisé une méthode basée sur la spectroscopie d’émission, que nous avions développée précédemment [1]. L’étalonnage du montage expérimental a été effectué avec de l’hydrogène moléculaire, en fonction de la pression du gaz, et à la longueur d’onde de 656,3 nm de la raie émise par l’hydrogène atomique produit au cours de l’excitation de l’hydrogène au moyen d’une source micro-onde, conduisant à une dissociation partielle du gaz. Ensuite, nous avons mesuré l’intensité de la même raie émise par le gaz recueilli après chauffage à 800 °C et pendant 2 h, d’une quantité connue de C60 traité avec H2, ce qui nous a permis de déterminer la pression du gaz recueilli, provenant de l’échantillon de produit utilisé dans cette expérience (voir Fig. 6). Nous avons trouvé une concentration en hydrogène moléculaire de l’ordre de 35% et, en tenant compte des concentrations relatives données dans le Tableau 1, nous avons pu estimer la concentration en complexes endoédriques à 18%, et celle du C60 hydrogéné à 35%, ce qui donnerait pour ce dernier composé la formule C60H21. Ce dernier résultat semble être corroboré par l’allure du spectre de masse obtenu avec le C60 traité avec H2 ; ainsi, on voit sur la Fig. 7 une distribution assez régulière de pics, après la structure isotopique du C60, allant jusqu’à la masse de C60H21, avec un maximum pour la masse de C60H16. En outre, l’intensité de ces pics entre les masses 724 et 741 se révèle très faible, probablement à cause d’un important phénomène de fragmentation de la molécule de C60, dû à l’utilisation de sources de grande énergie pour la désorption et l’ionisation, comme dans le cas du spectre de masse de la Fig. 7, pour lequel un laser émettant dans l’ultraviolet a été utilisé. Par ailleurs, nous avons observé que les masses 721 et 722 avaient des intensités de 25% plus fortes que celles présentées par les masses correspondantes de fullerène non traité.
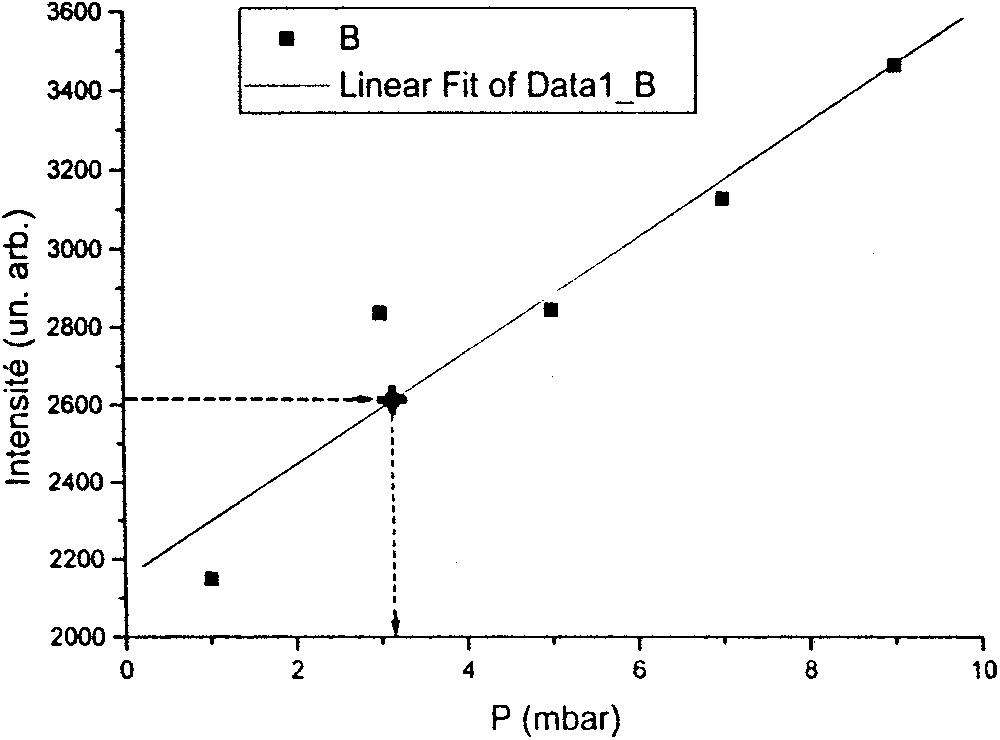
Étalonnage en intensité de la raie spectrale d’émission de l’hydrogène atomique H I à λ = 656,3 nm, en fonction de la pression de l’hydrogène moléculaire, et mesure de l’intensité de cette même raie émise à partir du gaz recueilli après chauffage à 800 °C d’un échantillon de C60 traité avec H2, de masse égale à 2,9 mg.
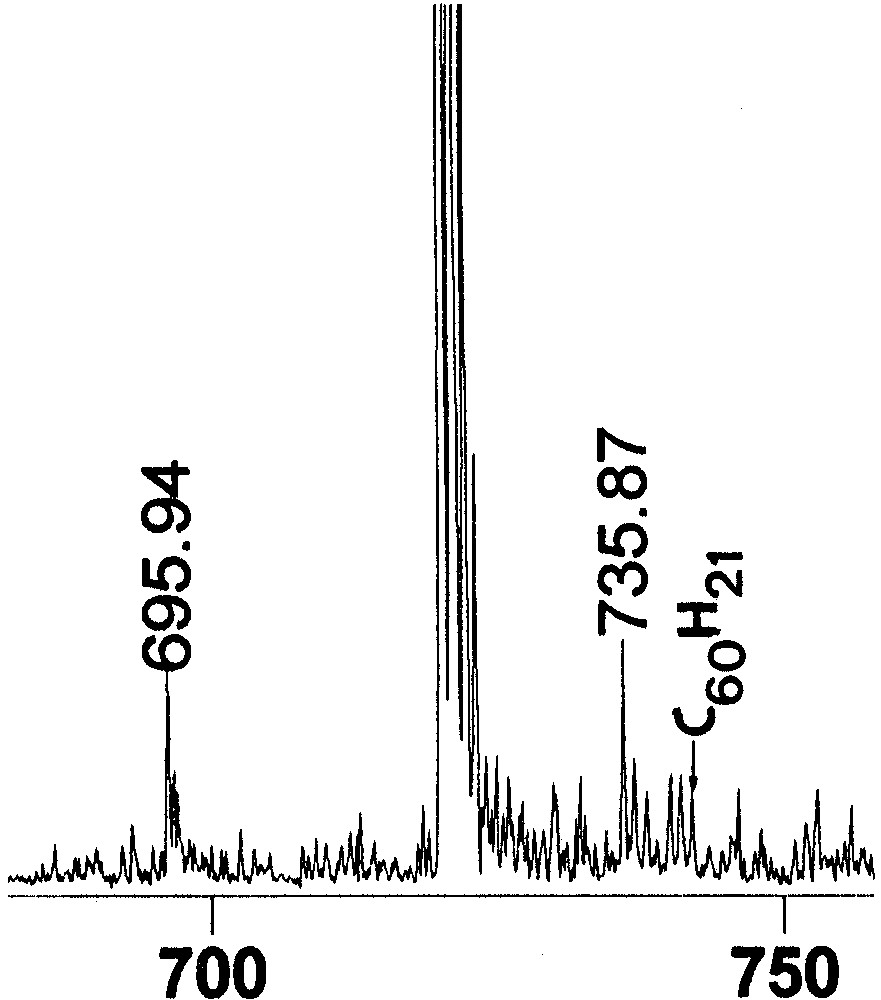
Spectre de masse à haute résolution, obtenu par ionisation laser, du C60 traité avec H2. La masse 696 correspond au C58 provenant de la fragmentation partielle du C60, avec perte d’un C2 ; la masse 736 représente le composé d’addition C60H16.
Par ailleurs, il nous semble intéressant de rapprocher nos résultats sur le C60 hydrogéné de ceux obtenus par Kolesnikov et al. [8], qui ont trouvé la formule C60H24 à partir de mesures de rétrodiffusion Rutherford d’ions He et de diffusion inélastique de neutrons, pour du C60 hydrogéné obtenu par un traitement à la température de 620 K et sous une pression de 0,6 GPa d’hydrogène.
4 Conclusion
Nous avons obtenu une préparation du complexe endoédrique hydrogène moléculaire–fullerène C60, associé à du C60 hydrogéné, en utilisant une nouvelle méthode décrite précédemment [1] et reposant sur l’excitation par un laser impulsionnel, travaillant à λ = 532 nm, d’un échantillon de C60 placé au sein d'un volume d’hydrogène comprimé à 0,1 GPa. Nous avons effectué des caractérisations du produit ainsi traité, obtenues par RMN du proton, d’une part, et par les spectroscopies infrarouge et ultraviolet lointain, d’autre part. Ces expériences ont démontré que les deux types de composés cités ci-dessus étaient bien produits avec notre nouvelle méthode. En outre, l’étude des spectres d’absorption dans les régions du visible et de l’ultraviolet proche ont montré que la structure électronique de la molécule de C60 traité avec l’hydrogène était profondément modifiée par rapport à celle du C60 non traité, conclusion reposant sur la forte diminution des intensités des bandes d’absorption, qui sont largement déplacées vers les grandes longueurs d’onde. Enfin, nous avons pu obtenir, au moyen d’une méthode basée sur la spectroscopie d’émission [1], une estimation de la concentration, d’une part, en complexes endoédriques H2@C60, d’environ 18% et, d’autre part, en C60 hydrogéné, de l’ordre de 35%.
Remerciements
Nous tenons à remercier vivement M. P. Florian, du Centre de recherches sur les matériaux à haute température, CNRS, Orléans–La Source, pour les expériences de résonance magnétique nucléaire, M. P. Marteau, du laboratoire d’ingénierie des matériaux et des hautes pressions, CNRS, université Paris-13, Villetaneuse, pour les travaux de spectroscopie infrarouge, Melle M.-C. Castex, du laboratoire de physique des lasers, université Paris-13, Villetaneuse, pour les expériences de spectroscopie dans l’ultraviolet lointain, et M. J.-C. Blais, du laboratoire de chimie structurale, organique et biologique, CNRS, université Pierre-et-Marie-Curie, Paris, pour les expériences en spectrométrie de masse.



