1 Introduction
Les Uvaria sont des arbustes fortement odoriférants [1]. Les espèces Uvaria chamae et Uvaria afzelii sont utilisées à la fois comme aliment pour leurs fruits et comme médicament dans le traitement de certaines maladies, telles que la dysenterie, la fatigue, la sénescence, les douleurs abdominales et la cicatrisation des plaies [2]. En ce qui concerne Uvaria sp., il s'agit d'une nouvelle espèce découverte dans la forêt de Dabou, en Côte-d'Ivoire (dans la région du Sud). Dans la bibliographie, seules deux publications portent sur les huiles essentielles de Uvaria chamae. Oguntimein et coll. [3] ont identifié le 2,5-dimethoxy-paracymene (26,13 %) et le benzoate de benzyle (25,7 %) comme produits majoritaires de l'essence des racines de cette espèce au Nigeria, alors qu'au Bénin, Ayedoun et coll. [4] ont trouvé en plus de ces deux derniers, avec des taux respectifs de 38,3 % et 13,5 %, le thymol méthyl éther (12,6 %). Quant aux deux autres, aucune publication ne fait, à notre connaissance, mention de leurs huiles essentielles. Il s'agit dans ce travail, d'identifier les constituants chimiques des huiles essentielles des racines et des écorces de ces espèces ivoiriennes afin d'apporter notre contribution à une meilleure connaissance et à une meilleure utilisation des Uvaria.
2 Matériels et méthodes
2.1 Matériel végétal et méthode d'extraction des huiles
Les échantillons des racines et des écorces de Uvaria chamae ont été récoltés à Bouaké (ville située au centre de la Côte-d'Ivoire) en juillet 2001, tandis que ceux de Uvaria afzelii proviennent de Bingerville et que ceux de Uvaria sp. ont été collectés au Centre national de floristique (CNF) de l'université de Cocody–Abidjan, au cours de la même période. Les espèces Uvaria chamae et Uvaria afzelii ont été identifiées par le professeur Aké Assi au CNF. Les huiles essentielles ont été obtenues par hydrodistillation du matériel végétal frais (500 g pour chaque échantillon) pendant 4 h dans un appareil de type Clevenger. Les échantillons d'huiles ont été séchés sur du sulfate de magnésium anhydre. Les rendements des différents échantillons sont présentés dans le Tableau 1.
Rendements et caractéristiques des huiles essentielles
| Rendement en pourcentages (%) | Couleur | ||
| Uvaria chamae | racines | 0,5 | jaune |
| écorces | 0,15 | incolore | |
| Uvaria afzelii | racines | 0,05 | jaune clair |
| écorces | 0,01 | incolore | |
| Uvaria sp. | racines | 0,6 | jaune orangé |
| écorces | 0,06 | jaune clair |
2.2 Méthode d'analyse
L'identification des constituants des huiles essentielles a été réalisée à l'aide du couplage chromatographie en phase gazeuse–spectrométrie de masse (CPG–SM), à l'exception du composé majoritaire de l'essence des racines de Uvaria sp. L'analyse de l'huile a été faite à l'aide d'un chromatographe de type DELSI DI 200, équipé d'une colonne capillaire DB5 de 0,25 mm de diamètre et 25 m de longueur, avec une épaisseur du film de 0,25 μm. La température du four est programmée à 50 °C pendant 5 min, puis subit une augmentation de 3 °C/min jusqu'à 220 °C. La température de l'injecteur est fixée à 235 °C et celle du détecteur à 250 °C. Le gaz vecteur utilisé est l'azote. Le spectromètre de masse couplé au chromatographe est un modèle Hewlett Packard de type HP6890 et HP5973, équipé d'une colonne capillaire DB5, dont le diamètre est de 0,25 μm. L'énergie d'ionisation utilisée est égale à 70 eV, la température du four est programmée à 50 °C pendant 5 min, puis est augmentée de 5 °C/min jusqu'à 300 °C, et enfin maintenue à 300 °C pendant 5 min. Le gaz vecteur utilisé est l'hélium. Les pourcentages des composés ont été obtenus à l'aide du couplage CPG–FID. Les spectres de masse des différents composés ont été comparés aux spectres de masse des banques de données de la littérature [5].
2.3 Séparation, purification et identification du composé majoritaire de l'huile essentielle des racines de Uvaria sp.
Le couplage CPG–SM n'ayant pas permis d'identifier le principal produit (72 %) de l'essence des racines de Uvaria sp., il a été fait appel aux méthodes chromatographiques. En effet, par chromatographie sur colonne de gel de silice couplée à la chromatographie sur couche mince, nous avons séparé et purifié le composé inconnu. Nous avons obtenu 45,1 mg d'un produit pur à 99 %, de couleur jaune et d'odeur agréable. Ce dernier a été soumis aux techniques d'analyse habituelles, à savoir la résonance magnétique nucléaire du proton et du carbone (RMN 1H, 13C), la spectrométrie de masse (SM) et spectrométrie infrarouge (IR).
3 Résultats
3.1 Analyses spectrométriques
- • RMN 1H (CDCl3, 400 MHz)
δ (ppm) : 1,22 [d, 6H, (CH3)2–CH–Ar] ; 2,12 [s, 3H, CH3–Ar] ; 3,25 [m,1H, (CH3)2–CH–Ar] ; 3,6–3,7 [large singulet, 6H, (OCH3)2–Ar] ; 5,40 [s, 1H, OH–Ar] ; 6,35 [s, 1H, Ar-H].
- • RMN 13C (CDCl3, 100 MHz)
δ (ppm): 16,4 (CH3–Ar) ; 21,63 (CH3)2–CH); 26,3 (CH3)2–CH) ; 56,25 (O−CH3); 62,2 (O−CH3), 110,51; 121,94 ;127,28 ; 141,57 ; 145,28 ; 52,44 C (Ar).
- • IR (dissout dans CDCl3 évaporé sur lame KBr) : ν (cm–1)
3445 (OH); 1211 et 1261 (OCH3)
- • Spectre de masse
C12H18O3; M = 210 g mol–1 ; M+ = 195
3.2 Compositions chimiques des huiles essentielles
Les résultats de l'analyse des compositions chimiques des différents échantillons d'huiles essentielles sont reportés dans le Tableau 2.
Étude comparative des compositions chimiques des huiles essentielles des racines et des écorces de Uvaria chamae, Uvaria afzelii et Uvaria sp.
| Composés identifiés | KI | Uvaria chamae | Uvaria afzelii | Uvaria sp. | |||
| racines | écorces | racines | écorces | racines | écorces | ||
| Monoterpènes hydrocarbonés | |||||||
| Tricyclène | 921 | 0,61 | — | — | — | 0,45 | — |
| α-Thujène | 925 | — | — | — | — | 0,35 | — |
| α-Pinène | 933 | 0,38 | — | 4,59 | 0,65 | 0,93 | 0,23 |
| Camphène | 953 | 7 | — | 11,43 | 0,49 | 10,03 | 0,23 |
| Sabinène | 971 | — | — | — | tr | 0,03 | — |
| β-Pinène | 976 | — | tr | 0,36 | 0,27 | 0,1 | 0,48 |
| Myrcène | 991 | 0,35 | tr | 0,1 | 0,17 | 1,24 | 0,15 |
| δ-3- Carène | 1009 | 0,64 | tr | 0,27 | tr | 0,88 | 0,04 |
| α-terpinène | 1015 | 0,03 | — | — | — | 0,05 | 0,5 |
| p-cymène | 1024 | 0,27 | 0,05 | 0,02 | — | 0,26 | 0,24 |
| Limonène | 1029 | 0,22 | tr | 0,31 | 0,33 | 0,69 | 0,35 |
| (Z)-β-Ocimène | 1041 | 2,48 | 0,2 | 0,24 | 0,1 | 0,02 | 0,28 |
| (E)-β-Ocimène | 1048 | 0,11 | — | — | — | — | tr |
| γ-Terpinène | 1058 | 0,23 | tr | 0,06 | 0,11 | 0,03 | tr |
| Terpinolène | 1083 | 0,03 | — | 0,03 | tr | ||
| Total en % | 12,35 | 0,25 | 17,38 | 2,12 | 15,09 | 2,5 | |
| Monoterpènes oxygénés | |||||||
| 1,8-Cinéole | 1032 | 0,32 | tr | 5,56 | 6,03 | 0,1 | 1,14 |
| Camphre | 1145 | 0,12 | — | — | — | — | — |
| Isomenthone | 1157 | — | — | — | 0,06 | — | — |
| Bornéol | 1171 | 0,24 | — | — | — | — | — |
| Terpinène-4-ol | 1178 | 0,1 | tr | 0,34 | 0,05 | 0,16 | tr |
| α-Terpinéol | 1194 | 0,04 | tr | 1,45 | 0,06 | 0,1 | 0,16 |
| Acétate d'endo fenchyle | 1215 | 0,11 | — | — | — | 0,04 | — |
| Néral | 1233 | — | tr | — | — | 0,22 | 0,02 |
| Thymol méthyl ether | 1236 | 6,64 | tr | 0,2 | — | 0,05 | 0,1 |
| Carvacrol méthyl ether | 1244 | 2,27 | tr | 0,35 | — | — | — |
| Géraniol | 1246 | — | tr | 0,72 | — | — | 0,14 |
| Thymol | 1287 | — | 0,42 | 2,79 | — | — | 0,21 |
| Acétate de bornyle | 1290 | 5,04 | — | 13,67 | 0,12 | 3,42 | 0,16 |
| Carvacrol | 1294 | — | tr | 0,1 | 0,15 | 0,46 | 0,11 |
| Acétate de géranyle | 1372 | — | 0,11 | — | — | — | — |
| 2,5 diméthoxy-para-cymène | 1419 | 28,55 | 0,33 | 14,97 | 2,56 | 0,83 | 0,69 |
| 1-hydroxy-2,5-diméthoxy-para-cymène | 1520 | 0,62 | — | 1,86 | 1 | 72,01 | 4,55 |
| Total en % | 44,05 | 0,86 | 42,01 | 10,03 | 77,39 | 7,28 | |
| Sesquiterpènes hydrocarbonés | |||||||
| α-Cubébène | 1341 | — | — | — | — | — | 0,2 |
| α-Copaène | 1368 | 0,25 | 0,22 | 0,41 | 1,05 | 0,1 | 1,44 |
| β-Élémène | 1389 | — | — | — | tr | 0,14 | 0,05 |
| Cyperène | 1399 | 0,17 | — | 1,62 | 1,47 | 0,49 | 0,78 |
| β-Caryophyllène | 1412 | — | — | 0,67 | 1,38 | — | 0,96 |
| Trans-α-bergamotène | 1432 | — | — | 0,41 | — | — | — |
| α-Humulène | 1456 | — | 0,13 | 0,63 | tr | — | 0,73 |
| (E)-β-Farnésène | 1456 | — | — | — | 0,34 | — | — |
| Rotudène | 1463 | — | — | — | — | 0,1 | tr |
| γ-Muurolène | 1474 | — | — | tr | tr | 0,2 | 1 |
| Germacrène D | 1482 | — | — | 0,71 | 1,69 | — | tr |
| α-Sélinène | 1490 | — | 0,15 | tr | — | tr | |
| α-Muurolène | 1499 | — | — | — | — | tr | 0,12 |
| β-Bisabolène | 1507 | — | — | 0,59 | — | — | — |
| γ-Cadinène | 1512 | 0,18 | — | — | — | tr | 0,82 |
| δ-Cadinène | 1517 | 0,18 | 0,9 | tr | 2,93 | — | — |
| Total en % | 0,78 | 1,25 | 5,19 | 8,86 | 1,03 | 6,1 | |
| Sesquiterpènes oxygénés | |||||||
| (E) Nérolidol | 1560 | — | — | 0,72 | 0,18 | — | — |
| Oxyde de caryophyllène | 1583 | — | tr | 0,75 | — | — | 0,57 |
| Gaïol | 1597 | — | — | 0,54 | — | — | — |
| 1,10-diépi-cubénol | 1612 | 0,26 | 0,1 | — | — | — | — |
| 1-Épi-Cubénol | 1625 | 0,23 | 0,64 | — | — | — | 0,88 |
| γ-Eudesmol | 1633 | — | — | 1,43 | 0,31 | — | — |
| Cubébol | 1645 | — | — | — | — | — | 0,78 |
| α-Épi-Cadinol | 1649 | 7,03 | 2,24 | 12,28 | 4,78 | — | — |
| α-Muurolol | 1650 | — | — | — | — | tr | 3,76 |
| α-Cadinol | 1654 | 0,21 | 0,18 | — | — | — | 0,3 |
| α-Bisabolol | 1685 | — | — | 0,12 | tr | — | — |
| Total en % | 7,73 | 3,16 | 15,84 | 5,27 | tr | 6,29 | |
| Dérivés benzéniques | |||||||
| Benzaldéhyde | 960 | — | tr | — | — | — | 0,02 |
| Benzoate de benzyle | 1769 | 30,42 | 90,7 | 13,64 | 69,41 | 2,37 | 74,41 |
| Total en % | 30,42 | 90,7 | 13,64 | 69,41 | 2,37 | 74,43 |
4 Discussion
4.1 Structure du composé majoritaire de l'essence des racines de Uvaria sp.
Les déplacements chimiques des deux méthoxy sont très proches et apparaissent sous forme d'un seul pic à cette résolution du spectre RMN du proton. En effet, ceux-ci apparaissent sous forme d'un large singulet entre 3,6 et 3,7 ppm. Cependant, en se référant aux spectres RMN 13C et RMN COSY, on se rend bien compte que les carbones portant ces protons ont des déplacements chimiques distincts (56,25 et 62,2 ppm). Ces résultats ont donc permis d'identifier le produit majoritaire de l'essence des racines de Uvaria sp. comme étant le 1-hydroxy 2,5-diméthoxy-para-cymène (Fig. 1). Cette molécule a été également isolée de l'extrait éthéré des racines de Ageratina espinosara (Asteraceae) par Bohlmann et al. [6] en 1977 (Tableau 3). Cependant, c'est la première fois, à notre connaissance, qu'elle est identifiée dans le genre Uvaria.
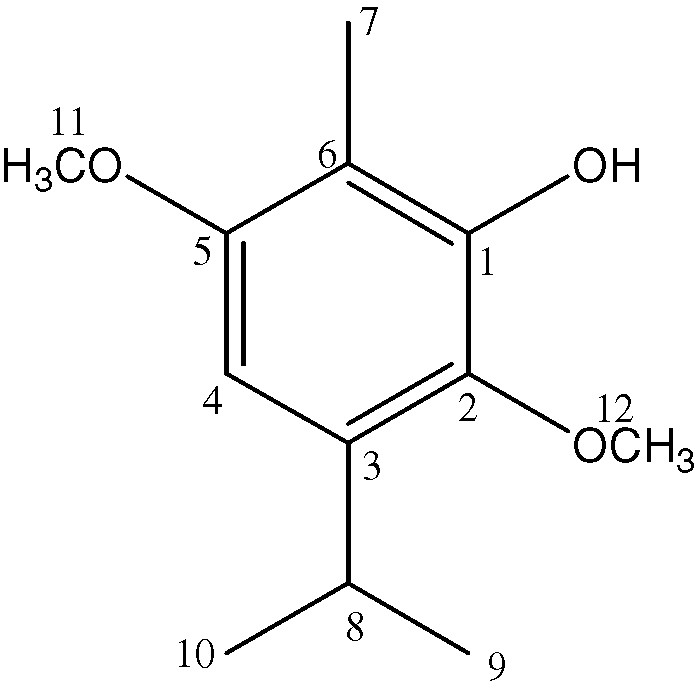
1-hydroxy 2,5-diméthoxy-para-cymène.
Comparaison des données RMN 1H du 1-hydroxy 2,5-diméthoparacymène (1) avec celles de la bibliographie (2) [6]
| H | 1 | 2 |
| 4 | 6,35 | 6,27 |
| 7 | 2,12 | 2,1 |
| 8 | 3,25 | 3,27 |
| 9 | 1,22 | 1,24 |
| 10 | 1,22 | 1,24 |
| 11 | 3,6 | 3,74 |
| 12 | 3,7 | 3,8 |
4.2 Compositions chimiques des huiles (Tableau 2)
4.2.1 Les racines
L'analyse de ces résultats révèle des similitudes et des particularités au niveau des essences des racines des trois Uvaria de Côte-d'Ivoire. En ce qui concerne les similitudes, on note une prédominance des monoterpènes oxygénés, quelle que soit l'espèce, avec un taux beaucoup plus important chez Uvaria sp., soit 77,39 % contre 44,05 % chez Uvaria chamae et 42,01 % chez Uvaria afzelii. De même, les pourcentages des monoterpènes hydrocarbonés sont assez proches dans les trois échantillons, soit 12,35 % chez Uvaria chamae, 17,38 % chez Uvaria afzelii et 15,09 % chez Uvaria sp. Quant aux composés identifiés, le camphène est le seul produit majoritaire commun aux trois espèces (7 % chez Uvaria chamae, 11,43 % chez Uvaria afzelii et 10,03 % Uvaria sp.). La plupart des produits majoritaires chez Uvaria chamae le sont également chez Uvaria afzelii, mais avec des taux différents. En effet, la teneur du 2,5-diméthoxy-para-cymène est environ deux fois plus élevée chez Uvaria chamae (28,55 %) que chez Uvaria afzelii (14,97 %). De même, le taux du benzoate de benzyle passe presque du double (30,42 %) chez Uvaria chamae au simple (13,64 %) chez Uvaria afzelii. Les pourcentages de l'acétate de bornyle et de l'α-épi-cadinol sont plus importants chez Uvaria afzelii (soit respectivement 13,67 % et 12,28 %) que chez Uvaria chamae (soit respectivement 5,04 % et 7,03 %).
S'agissant des particularités, Uvaria chamae se différencie des deux autres par un taux très élevé en dérivés benzéniques (30,42 %), soit environ deux fois plus important que celui de Uvaria afzelii (13,64 %) et environ 15 fois plus que celui de Uvaria sp. (2,37 %). Par ailleurs, Uvaria afzelii se distingue par une teneur en sesquiterpènes oxygénés plus importante (15,84 %), alors qu'elle est de moitié chez Uvaria chamae (7,73 %) et inexistante chez Uvaria sp. (tr). On constate également, pour cette espèce, un pourcentage en sesquiterpènes hydrocarbonés plus élevé (5,19 %) que chez les deux autres (autour de 1 %). Au niveau des produits identifiés, le thymol méthyl éther (6,64 %) est uniquement majoritaire chez de Uvaria chamae, pratiquement inexistant chez les deux autres espèces. En revanche, chez Uvaria afzelii et Uvaria sp., ce sont respectivement le 1,8-cinéole (5,56 %) et le 1-hydroxy 2,5-diméthoxy-para-cymène (72 %) qui dominent.
4.2.2 Les écorces
Les huiles des écorces des trois Uvaria renferment essentiellement du benzoate de benzyle, avec les teneurs de 90,7 % chez Uvaria chamae, 74,41 % chez Uvaria sp. et 69,41 % chez Uvaria afzelii. En dehors de cette similitude, les trois espèces pourraient se distinguer les unes des autres par leurs taux en terpènes. Par exemple, chez Uvaria afzelii, on note des taux plus élevés en 1,8-cinéole (6,03 %) et en α-épi-cadinol (4,78 %), alors que Uvaria sp. se différencie des autres par sa teneur en 1-hydroxy 2,5-diméthoxy-para-cymène (4,55 %) et la présence exclusive de l'α-muurolol (3,76 %). Quant à Uvaria chamae, le seul terpène dont la teneur dépasse l'unité, l'α-épi-cadinol (2,24 %) est environ deux fois moins important que l'espèce afzelii (4,78 %).
5 Conclusion
Cette étude a permis de trouver un caractère commun aux espèces Uvaria étudiée. Il s'agit du benzoate de benzyle, qui constitue la principale molécule des essences des écorces de ces Uvaria, avec de fortes teneurs (90,7 % chez Uvaria chamae, 74,41 % chez Uvaria sp. et 69,41 % chez Uvaria afzelii). Cependant, chaque espèce garde une particularité bien spécifique, car les molécules identifiées dans les racines permettent de les différencier. En effet, l'huile des racines de Uvaria sp. renferme en majorité le 1-hydroxy-2,5-diméthoxy-para-cymène, avec 72,01 %, tandis que celle de Uvaria chamae contient deux produits majeurs, qui sont le 2,5-diméthoxy-para-cymène (28,55 %) et le benzoate de benzyle (30,42 %). Quant à l'essence des racines de Uvaria afzelii, on y trouve en plus du 2,5-diméthoxy-para-cymène (14,97 %) et du benzoate de benzyle (13,64 %), de l'acétate de bornyle (13,67 %), de l'α-épi-cadinol (12,28 %) et du camphène (11,43 %). Ces trois derniers composés existent également dans Uvaria chamae, à des taux moins importants.
Il serait intéressant d'étendre cette étude à d'autres espèces Uvaria, afin de vérifier si le benzoate de benzyle peut être un facteur d'identification du genre.


