1 Introduction
Pour comprendre les mécanismes fondamentaux à l'origine des processus électrochimiques se déroulant à une interface métal–solution électrolytique, il est indispensable de définir au préalable la structure de la surface métallique à l'échelle nanométrique. Dans cette voie de recherche, l'étude des surfaces monocristallines d'or occupe une place prépondérante. En effet, l'or est incontestablement le plus intéressant d'entre les métaux nobles, car, au contact de certaines solutions électrolytiques aqueuses, il peut rester idéalement polarisé dans un grand domaine de potentiel, de l'ordre de 1 V. Cette caractéristique permet d'étudier d'une manière plus détaillée l'influence de la structure atomique superficielle sur les propriétés électrochimiques de l'interface or monocristallin/solution électrolytique.
Depuis une vingtaine d'année, l'emploi de la diffraction d'électrons lents (LEED), de la microscopie à effet tunnel (STM) et de la diffraction des rayons X sous incidence rasante (GIXD), sous vide ou en solution électrolytique, ont permis des progrès considérables dans le domaine de la connaissance des surfaces et des interfaces or monocristallin/solution électrolytique. L'étude, dans un premier temps, des deux plans de haute densité atomiques (100) et (111) a permis de mettre en évidence les processus de reconstruction superficielle [1,2] caractérisant ces deux faces. Les reconstructions de type (5 × 20) pour le plan (100) et (22 × √3) pour le plan (111) correspondent à des structures stables qui se forment sous l'effet de forces de contrainte superficielle induites par le phénomène de stress consécutif à la création de la surface. Dans le cas du plan (111), la reconstruction (22 × √3), qui a été décrite dans le cadre du modèle de Frenkel–Kontorova [3–6], résulte de forces de compression non uniformes, qui s'exercent dans la direction [1,1,0], et qui donnent naissance à une structure secondaire en chevrons, très caractéristique de ce plan cristallin de l'or.
Plusieurs études sous vide des faces vicinales du plan Au(111), composées soit de terrasses (111) et de bord de marches {100}, soit de terrasses (111) et de bord de marches {111} (Fig. 1 et Tableau 1), ont montré que les modèles de facettage thermique qui apparaissent sur ces faces dépendent essentiellement de la nature des interactions s'exerçant entre chaque type de marche et la reconstruction présente sur les terrasses (111) [7–9]. Dans le cas des faces vicinales à marches {100}, telles que Au(11,9,9) et Au(433), le facettage conduit à la formation de facettes d'orientation (111) et (755). La caractérisation par STM, par LEED et par GIXD de ce type de facettage révèle que, pour Au(11,9,9) et Au(433), les facettes (111) ont une largeur de l'ordre de 4 nm, et que le modèle de reconstruction présent sur ces facettes est différent de la reconstruction (22 × √3) observée sur une surface monocristalline Au(111) [10,11]. Cette reconstruction particulière se caractérise par la présence d'une ligne de faute d'empilement parallèle à la marche, c'est-à-dire dans une direction différente de celles caractérisant la reconstruction en chevron d'une électrode Au(111). Dans ce modèle de reconstruction, la zone comprise entre la ligne de faute d'empilement et le bord de la marche correspond à la zone reconstruite ; l'empilement atomique est de type hexagonal compact (hc). Cette reconstruction du bord des terrasses (111) impose une reconstruction du bord des marches {100}, c'est-à-dire la formation d'un bord de marches {111} qui correspond à une structure plus stable. Cette marche reconstruite (111) se situe à la jonction entre les facettes (111) et les facettes (755), dont les terrasses (111) ne sont pas reconstruites et dont les marches ont conservé leur structure (100). La formation des facettes (111) et (755) crée à la surfaces des électrodes une nouvelle morphologie avec une structure périodique en hill-and-valley, dont la périodicité est de 7 nm pour la face Au(11,9,9) et de 11,5 nm pour Au(433).

Diagramme schématique des faces vicinales du plan Au(111) situées sur la zone . Ces faces sont constituées de terrasses (111) d'une largeur de n rangées atomiques, avec des marches de type {100} ou {111}.
Caractéristiques des faces vicinales du plan Au(111) : angle θ de désorientation, nombre n de rangées atomiques et largeur L des terrasse (111) de chacune des faces
| θ (°) | n | L (nm) | θ (°) | n | L (nm) | ||
| Au(776) | 4.05 | 14 | 3.33 | ||||
| Au(9,9,11) | 5.57 | 10 | 2.4 | Au(554) | 5.76 | 10 | 2.33 |
| Au(334) | 8.05 | 7 | 1.7 | Au(775) | 8.47 | 7 | 1.58 |
| Au(557) | 9.45 | 6 | 1.4 | Au(332) | 10.00 | 6 | 1.33 |
L'étude électrochimique des deux faces vicinales Au(11,9,9) et Au(433) facettées avait permis de montrer que l'ensemble des facettes (111) et des facettes (755) présentes à leur surface se comportent électriquement au contact d'une solution électrolytique comme des condensateurs en parallèle [12]. On en avait déduit qu'il est possible de reproduire le comportement électrochimique de ces faces vicinales en utilisant des électrodes monocristallines Au(111) et Au(755) pour simuler les deux types de facettes. L'exploitation des courbes de capacité différentielle en fonction du potentiel C(E) obtenues avec les électrodes Au(111) et Au(755) avait alors permis de reconstituer des courbes C(E) théoriques identiques aux courbes C(E) expérimentales obtenues avec les faces Au(11,9,9) et Au(433) facettées. La structure atomique des facettes (111) et (755) étant homogène, chacune possède un seul travail de sortie électronique sous vide et, par conséquent, un seul potentiel de charge nulle (pcn) au contact d'une solution électrolytique. Les courbes C(E) permettent donc de déterminer le pcn, puis la densité de charge en fonction du potentiel (σ(E)) de chaque type de facette. À partir des courbes σ(E), il est alors possible de déterminer le potentiel pour lequel la valeur de la charge portée par l'ensemble des facettes Au(111) et Au(755) est la même, mais de signe opposé. Ce pseudo-pcn, pour lequel la somme des charges présentes à l'interface métal/solution s'annule, est un paramètre caractéristique de ces faces vicinales, qui ne peut être déterminé que par cette méthode.
Dans le présent article, nous traiterons d'un autre type de faces vicinales du plan Au(111) constitué de terrasses (111) avec des bords de marches d'orientation {111}. Les deux faces vicinales à marches {111} étudiées ici sont l'orientation Au(554), dont la surface avant facettage est constituée de terrasses (111) d'une largeur de dix rangées atomiques, et l'orientation Au(775), dont les terrasses (111) ont une largeur de sept rangées atomiques. Les travaux que nous avons entrepris précédemment sur ces faces vicinales ont montré que le facettage thermique de ces surfaces à marches {111} conduit à la formation de structures atomiques plus complexes que celles observées avec les surfaces à marches {100}. Des études sous vide par STM [8], par LEED et par GIXD [13] ont révélé l'existence de deux niveaux de structures périodiques en hill-and-valley. Le premier niveau, qui correspond à une structure périodique à grande échelle, est formé de très grandes facettes, d'orientations (776) et (332), dont la super-périodicité est de 180 nm pour la face Au(554) et de 260 nm pour la face Au(775). Le second niveau correspond aux deux répartitions périodiques caractérisant les structures atomiques des deux types de facettes (776) et (332). L'orientation Au(776) est constituée de terrasses (111) d'une largeur de quatorze rangées atomiques dont la structure est reconstruite, tandis que l'orientation Au(332) est constituée de terrasses (111) d'une largeur de six rangées atomiques, avec une structure non reconstruite [14].
Les structures atomiques sous vide des faces vicinales Au(554) et Au(775) étant bien définies, une étude en solution des propriétés électrochimiques de ces faces, similaire à celle réalisée précédemment avec les faces vicinales Au(11,9,9) et Au(433) [12], a donc été entreprise.
2 Techniques expérimentales
2.1 Préparation des électrodes
Les cylindres d'or monocristallins (Engelhard–CLAL Purcla THP 99,99%) obtenus par la méthode de Brigdman sont orientés aux rayons X à ±10' par la méthode de diffraction de Lauë. Les électrodes monocristallines coupées par électroérosion à fil sont des disques de 2 mm d'épaisseur et de 12 mm de diamètre. La surface de chaque électrode est polie mécaniquement avec des pâtes diamantées de granulométrie décroissante jusqu'à 0,25 μm. La couche superficielle de métal perturbée par le polissage mécanique est éliminée par polissage électrochimique. Cette étape de préparation, qui précède le recuit, permet d'obtenir la structure non facettée des faces vicinales Au(776), Au(554) et Au(775). Les échantillons monocristallins sont ensuite recuits sous vide à 700 °C pendant 1 h, et ce traitement thermique conduit à la formation de la structure facettée dans le cas des faces Au(554) et Au(775) [9].
Un nettoyage chimique des électrodes est effectué ensuite dans deux bains d'acide nitrique et d'acide chlorhydrique bouillants. Après chacun des traitements à l'acide, l'électrode est soigneusement rincée avec de l'eau ultrapure (Millipore-Synergy UV System), puis finalement immergée dans de l'eau ultrapure et transférée dans une boîte à gants.
2.2 Mesures électrochimiques
Pour limiter au maximum la contamination de la surface des électrodes, l'étude électrochimique est effectuée dans une boîte à gants sous une atmosphère d'argon pur. Les voltamogrammes I(E) et les courbes de capacité différentielle en fonction du potentiel C(E) sont obtenues à l'aide d'un appareillage de mesure comprenant : un potentiostat de type « Solartron 1284 » et deux amplificateurs à détection synchrone de type « EG&G-DSP Lock-in Amplifier 7220 ». La méthode de mesure potentiostatique consiste à imposer à l'électrode une variation linéaire du potentiel et de superposer une faible tension alternative. Les courbes C(E) sont obtenues à l'aide d'un système d'acquisition et de traitement automatique des valeurs en phase et en quadrature des réponses alternatives en courant et en potentiel fournies par les détections synchrones. La vitesse du balayage en potentiel est de 0,01 V s−1, l'amplitude de la tension sinusoïdale superposée est de 3 mV et la fréquence est de 5,63 Hz. Cette fréquence particulière a été choisie afin d'éviter les perturbations dues aux sous-harmoniques du 50 Hz de la tension d'alimentation de l'appareillage de mesure. Les potentiels électrochimiques sont mesurés par rapport à une électrode de référence au calomel saturée (e.c.s.).
Afin de réduire les effets de l'adsorption spécifique sur les mesures de capacité différentielle on utilise des solutions diluées d'un électrolyte (NaF) dont l'anion F– s'adsorbe faiblement. Les solutions aqueuses de NaF 0,01 M utilisées sont préparées avec du sel NaF « Merck-Suprapur » et de l'eau ultrapure (« Millipore-Synergy UV System »).
3 Résultats expérimentaux
3.1 Comportement électrochimique des surfaces facettées de Au(554) et de Au(775)
Pour toutes les surfaces étudiées l'exploitation des courbes courant–potentiel I(E) permet d'abord de déterminer le domaine de potentiel de couche double dans lequel sont effectuées les mesures de capacité différentielle. L'intervalle de potentiel utilisé pour cette étude est compris entre −0,6 V et +0,5 V/(e.c.s.). Au début de chaque expérience, lors de la première polarisation de l'électrode au contact de la solution, les courbes I(E) évoluent légèrement pendant deux ou trois cycles, avant d'atteindre leur forme définitive. Ce phénomène, dû à la désorption progressive des dernières molécules de contaminant sous l'effet des variations de la charge interfaciale, correspond à la dernière étape de décontamination de l'électrode. L'étude électrochimique étant effectuée dans une boîte à gants sous atmosphère d'argon pur, aucune pollution ne se produit ultérieurement pendant les mesures. Par conséquent, les courbes de courant I(E) et de capacité différentielle C(E) restent reproductibles pendant toute la durée de l'expérience.
Pour mettre en évidence le facettage des orientations Au(554) et Au(775), on a représenté sur le diagramme de la Fig. 2 les courbes C(E) de ces deux faces ainsi que celles des électrodes d'orientations Au(332) et Au(776), qui correspondent aux deux types de facettes formées. Pour chaque orientation, on a représenté les courbes C(E) obtenues dans les deux sens de balayage en potentiel. La faible différence entre les courbes C(E) obtenues dans les deux sens de balayage en potentiel montre que, pour toutes ces orientations, aucune transformation importante de l'interface, telle qu'une reconstruction atomique ou une forte adsorption ionique, ne se produit dans ce domaine de potentiel.

Courbes de capacité différentielle C(E) dans une solution de NaF 10 mM, 10 mV s−1, 5,63 Hz ; potentiels E mesurés par rapport à une électrode au calomel saturée (e.c.s.) : Au(332), (---) balayage vers les potentiels positifs, (—) balayage vers les potentiels négatifs ; Au(775), (- - -) balayage vers les potentiels positifs, (- - - -) balayage vers les potentiels négatifs ; Au(554), (–·–) balayage vers les potentiels positifs, (-·-·-·-) balayage vers les potentiels négatifs ; Au(776), (****) balayage vers les potentiels positifs, (⋯) balayage vers les potentiels négatifs.
Le diagramme de la Fig. 2 révèle également l'existence de deux points d'intersection des quatre courbes C(E) situés à −0,070 V/(e.c.s.) et à +0,390 V/(e.c.s.). L'existence de ces points d'intersection prouve que les orientation Au(554) et Au(775) sont bien composées de facettes Au(776) et Au(332). En effet, les orientations Au(776) et Au(332) ayant à ces potentiels la même valeur de capacité différentielle, les surfaces de Au(554) et de Au(775) étant elles-mêmes composées de facettes (776) et (332), elles doivent également avoir la même valeur de capacité à chacun de ces potentiels. Ce comportement électrochimique démontre donc que la structure facettée de Au(554) et de Au(775) observée sous vide est bien conservée au contact de la solution électrolytique.
Pour confirmer cette observation, le comportement électrochimique des faces Au(554) et Au(775) a également été simulé à partir de celui des faces Au(332) et Au(776). Au contact de la solution électrolytique, les facettes se comportent électriquement comme des condensateurs en parallèle et la capacité différentielle d'une surface facettée est donc égale à la somme des capacités différentielles des facettes qui la composent. La surface de Au(554) étant constituée de 71% de facettes (776) et de 29% de facettes (332), et celle de Au(775) de 25% de facettes (776) et de 75% de facettes (332), il est possible, à partir des courbes C(E) d'électrodes d'orientations Au(332) et Au(776), de reconstituer la courbe C(E) de chaque surface facettée. Le diagramme C(E) de la Fig. 3 montre que, pour les deux faces Au(554) et Au(775), il y a une bonne coïncidence entre la courbe des valeurs mesurées et celle des valeurs calculées. Ceci constitue, pour ces deux orientations, une seconde confirmation de l'existence de la structure facettée au contact de la solution.
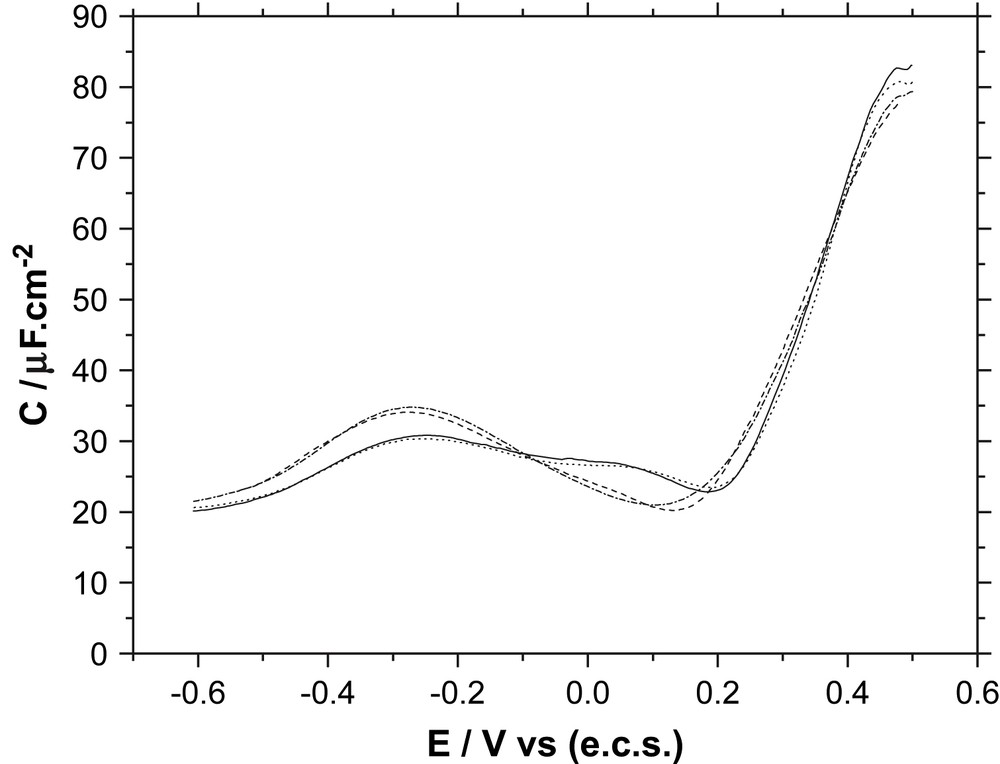
Courbes de capacité différentielle C(E) dans une solution de NaF 10 mM, 10 mV s−1, 5,63 Hz ; Au(554), (—) courbe mesurée, (….) courbe calculée [71% Au(776) + 29% Au(332)] ; Au(775), (- - - -) courbe mesurée, (_._._._) courbe calculée [25% Au(776) + 75% Au(332)].
3.2 Propriétés électrochimiques de Au(776)
La connaissance des propriétés électrochimiques des facettes Au(332) et Au(776), c'est-à-dire de la courbe de capacité différentielle C(E) et du potentiel de charge nulle (pcn) de chaque facette, devrait permettre de calculer la valeur de la charge interfaciale σ de chaque facette, puis d'accéder à la charge globale de la surface facettée.
Dans le cas des facettes Au(332), nous avons montré, dans des études précédentes [15,16], que cette orientation présente une structure électronique superficielle homogène (Fig. 4) c'est-à-dire qu'elle possède un seul type de dipôle électronique superficiel, auquel correspond un seul travail de sortie électronique sous vide et, par conséquent, un seul pcn en solution. Le tracé de la courbe C(E) et la détermination du pcn peut donc permettre d'accéder à la courbe de charge en fonction du potentiel (σ(E)) d'une électrode Au(332). Le calcul de la charge globale portée par l'ensemble des facettes Au(332) présentes sur une électrode facettée Au(554) ou Au(775) est donc possible.
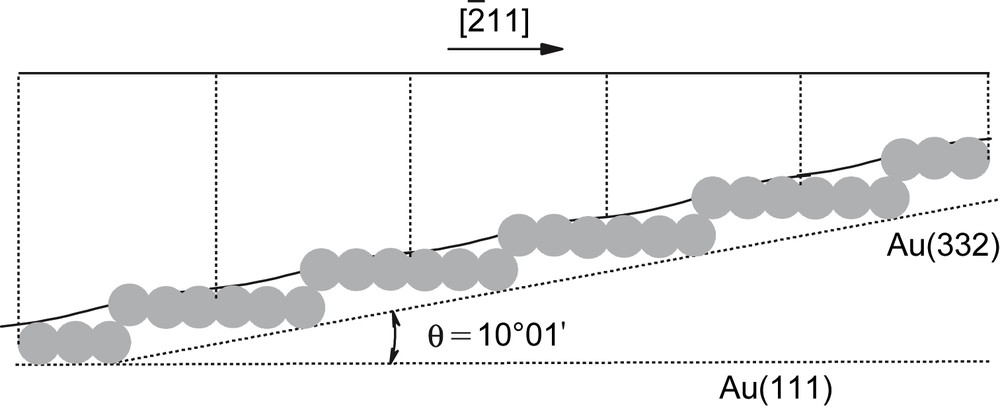
Vues schématiques du profil de la structure atomique d'une surface Au(332) et du profil de la répartition électronique superficielle sur les marches {111}.
En ce qui concerne les facettes Au(776), les études STM sous vide ont montré que cette orientation possède, comme Au(332), une structure atomique stable. En revanche, la stabilité atomique de sa surface n'implique pas, comme pour Au(332), l'homogénéité de son comportement électrochimique. En effet, sa structure atomique superficielle, constituée par une succession de grandes terrasses (111) d'une largeur de quatorze rangées atomiques et de marches monoatomiques, ne lui confère probablement pas une structure électronique superficielle homogène. Il est probable que la densité électronique au niveau d'une marche monoatomique et au milieu d'une terrasse n'est pas la même et que les dipôles formés sur chacun de ces secteurs de la surface sont différents. Cette répartition électronique entraîne certainement sous vide l'existence, localement, de deux valeurs du travail de sortie électronique et, au contact d'une solution électrolytique, la présence d'une densité de charge σ différente pour chaque secteur. Par conséquent, la valeur de la capacité différentielle de la couche double électrochimique formée sur les marches monoatomiques est probablement différente de celle présente sur les terrasses (111), ce qui implique que ces deux secteurs de la surface possèdent des pcn différents. Dans cette hypothèse, la capacité différentielle d'une face Au(776) devrait être égale à la somme de la capacité différentielle du secteur de la surface occupé par les terrasses (111) et de celle du secteur occupé par les marches monoatomiques {111}.
Or, la comparaison de la morphologie de la courbe C(E) de Au(776) et de celles des faces Au(554) et Au(775) facettées (Fig. 2) tend précisément à confirmer l'existence de deux types de structures à sa surface. Ce diagramme montre en effet que la capacité différentielle de la face Au(332) passe par un maximum vers −0,260 V/(e.c.s.) et que les courbes C(E) des orientations Au(554) et Au(775) facettées présentent également un maximum à ce même potentiel. L'amplitude de ce maximum de capacité différentielle étant proportionnelle au taux de facettes Au(332) présentes sur ces faces, sa valeur décroît lorsqu'on passe de Au(775) à Au(554). Or, la courbe C(E) de la face Au(776) révèle également à ce potentiel la présence d'un maximum de capacité différentielle. La structure atomique de Au(776) étant stable et ne présentant donc pas de facettes Au(332), la présence de ce maximum indiquerait qu'une fraction de sa surface présente cependant le même comportement électrochimique qu'une face Au(332). Cette observation confirmerait ainsi notre hypothèse précédente, c'est-à-dire que l'ensemble des marches de Au(776) aurait un comportement électrochimique différent de celui des terrasses (111), et que ce comportement électrochimique serait comparable à celui d'une surface Au(332).
Cependant, la comparaison des structures des faces Au(776) et Au(332) observées sous vide par STM ne permettent pas de confirmer directement cette dernière hypothèse. L'assimilation du comportement électrochimique des marches monoatomiques de Au(776) à celui d'une surface Au(332) nécessite d'admettre que la structure atomique de Au(776) a été modifiée au contact de la solution électrolytique. En effet, l'étude de Au(332) a montré que sa structure atomique très stable restait identique sous vide [14] et au contact d'une solution électrolytique [16]. Ceci signifie qu'au contact d'une solution électrolytique, sa surface est constituée de terrasses (111) non reconstruites d'une largeur de six rangées atomiques et de marches monoatomiques {111}. Or, l'étude STM sous vide de Au(776) montre que les terrasses (111) sont reconstruites. On observe sur les terrasses une succession de petits domaines correspondant aux deux types d'empilements atomiques, cubique à faces centrées (cfc) et hexagonale compacte (hc), séparés par des lignes de fautes d'empilements (Fig. 5). Dans les domaines cfc, les terrasses sont délimitées par des marches de type {111}, tandis que dans les domaines hc, l'empilement hc sur le substrat cfc conduit à la formation de marches {100}. On constate que cette structure mixte des bords de marches de Au(776) observée sous vide, constituée par une succession de marches {111} et {100}, ne correspond pas à la structure unique {111} des marches de Au(332). L'analogie du comportement électrochimique de l'ensemble des marches de Au(776) avec celui des marches de Au(332) impliquerait donc qu'en solution les marches de Au(776) ont également une structure unique de type {111}. Réciproquement l'existence en solution d'une structure {111} pour l'ensemble des marches de Au(776) impliquerait que les terrasses (111) ne sont pas reconstruites. Or, cette absence de reconstruction des terrasses (111) au contact de la solution est confirmée par les diagrammes C(E) de la Fig. 2. On remarque en effet que les courbes C(E) de Au(776) sont identiques dans les deux sens du balayage en potentiel, ce qui signifie qu'aucun processus réversible d'apparition et de disparition de la reconstruction des terrasses (111) ne se produit dans ce domaine de potentiel [16,17].

Images STM d'une surface Au(776) sous vide. Les différences de niveau des terrasses ont été soustraites afin de faire apparaître les lignes de reconstruction. (a) À grande échelle, les lignes de fautes d'empilement séparant les domaines cfc et hc traversent perpendiculairement les bords des marches. Cependant, à l'intérieur d'une terrasse, ces lignes sont en forme de « V ». (b) À l'approche du bord des marches, sous l'effet de la relaxation atomique, les domaines cfc s'élargissent, tandis que les domaines hc se rétrécissent.
L'existence d'une structure unique et stable constituée de terrasses non reconstruites (111)(1 × 1) et de marches monoatomiques {111} est donc l'hypothèse la plus vraisemblable pour décrire la face Au(776) au contact de la solution électrolytique (Fig. 6). Ceci revient à considérer que 40,4% d'une surface Au(776), correspondant au secteur des marches, a le même comportement électrochimique qu'une face Au(332) et que 59,6% de la surface, correspondant au secteur des terrasses, a le comportement électrochimique de la structure non reconstruite Au(111)(1 × 1). La capacité différentielle d'une électrode Au(776) est ainsi égale à la somme des capacités différentielles de ses secteurs Au(332) et Au(111)(1 × 1). Par conséquent, la courbe C(E) caractérisant le comportement électrochimique des terrasses Au(111)(1 × 1) peut être obtenue en défalquant la courbe C(E) de Au(332) de celle de Au(776) (Fig. 7).
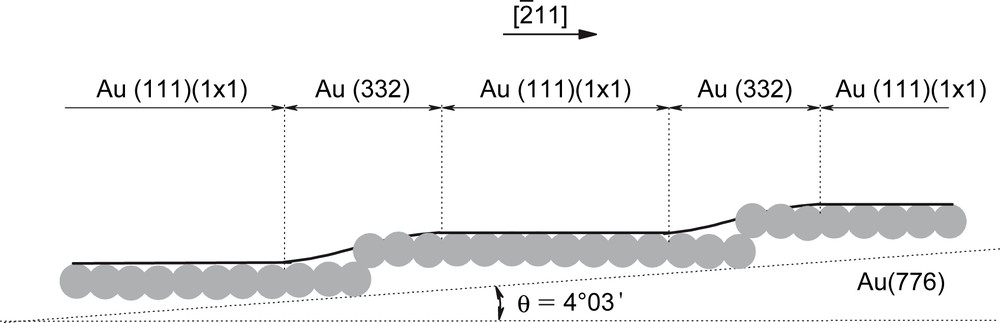
Vues schématiques du profil de la structure atomique d'une surface Au(776) et du profil de la répartition électronique superficielle. En solution électrolytique, chaque domaine Au(332) et Au(111)(1 × 1) de la surface Au(776) a un comportement électrochimique autonome.
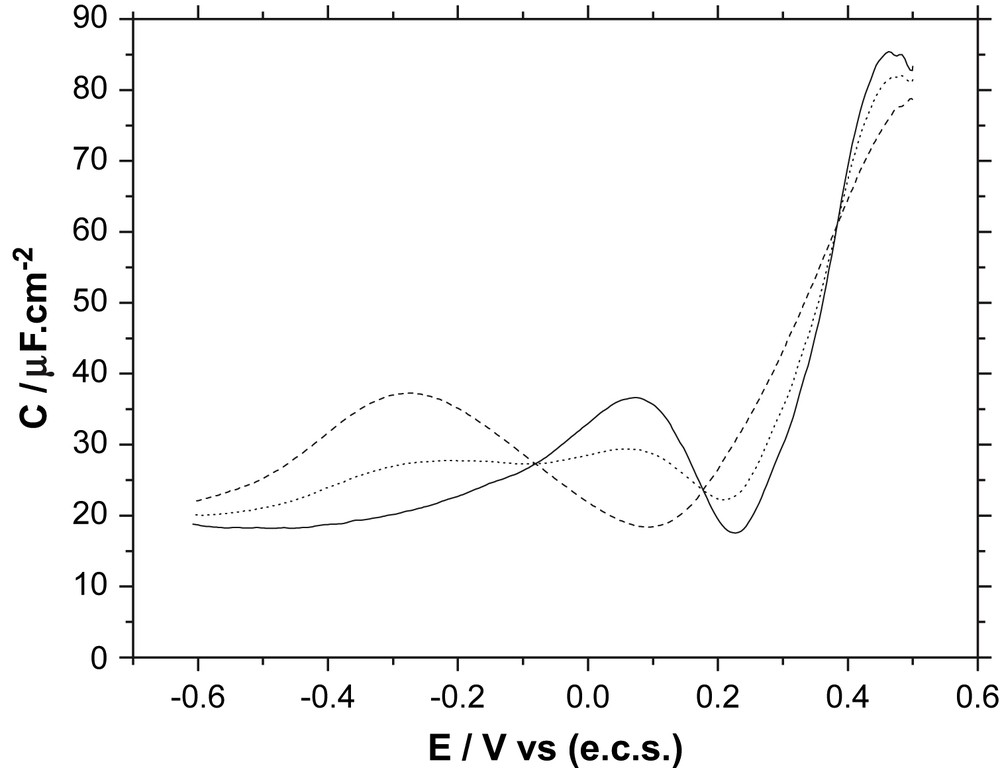
Courbes de capacité différentielle C(E) dans une solution de NaF 10 mM, 10 mV s−1, 5,63 Hz ; Au(776), (⋯) courbe mesurée ; Au(332), (- - -) courbe mesurée ; Au(111)(1 × 1), (—) courbe calculée [(100% Au(776) − 40,4% Au(332))/0,596].
3.2.1 Comparaison des propriétés électrochimiques des terrasses (111) de Au(776) avec celles d'une électrode monocristalline Au(111)
La représentation, sur un même diagramme (Fig. 8), de la courbe C(E) caractérisant les terrasses Au(111)(1 × 1) de Au(776) (Fig. 7) et des deux courbes C(E) d'une électrode monocristalline Au(111) correspondant aux deux sens du balayage en potentiel [16,17] montre que les trois courbes ont la même morphologie, mais que les minimums de capacité différentielle indiquant théoriquement les pcn sont situés à des potentiels différents. Pour les terrasses Au(111)(1 × 1), le minimum est situé à +0,225 V/(e.c.s.) et, pour l'électrode Au(111), le minimum est situé à +0,330 V/(e.c.s.) pour la courbe C(E) correspondant au balayage vers les potentiels positifs et à +0,280 V/(e.c.s.) pour celle correspondant au balayage vers les potentiels négatifs. Pour comprendre l'origine des écarts observés entre ces trois pcn, il est nécessaire de décrire la nature des forces d'interaction qui s'exercent à l'interface métal/solution dans tout le domaine de potentiel utilisé.
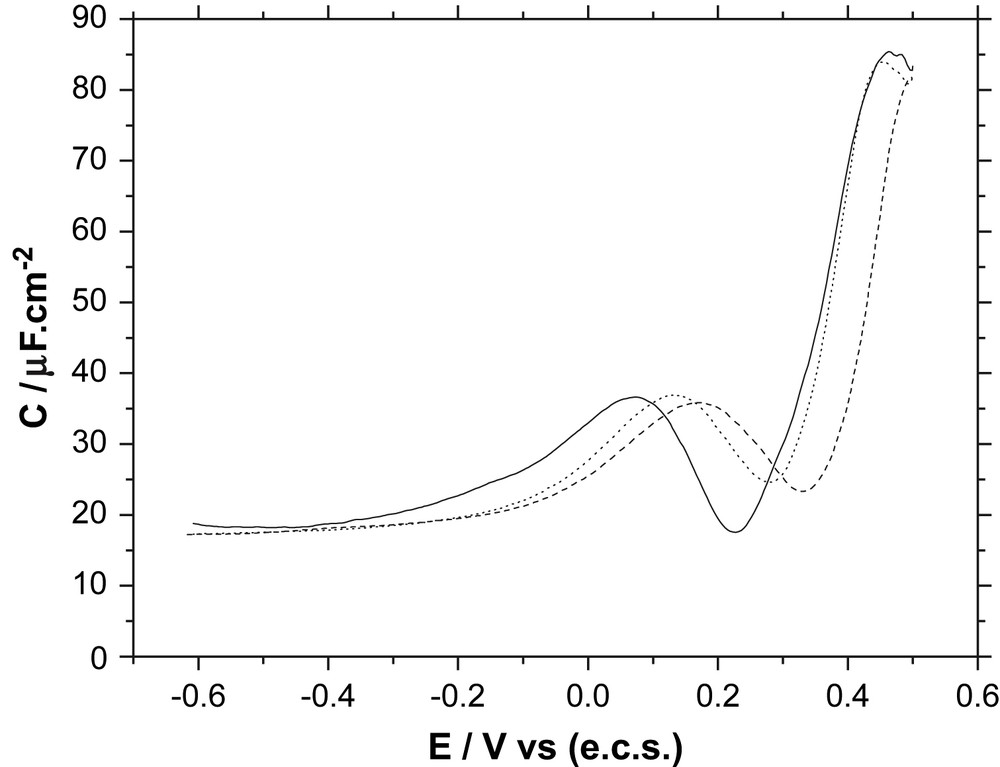
Courbes de capacité différentielle C(E) dans une solution de NaF 10 mM, 10 mV s−1, 5,63 Hz ; monocristal Au(111) reconstruit, (- - -) balayage vers les potentiels positifs ; monocristal Au(111) partiellement reconstruit (⋯), balayage vers les potentiels négatifs ; terrasses Au(111) non reconstruites de Au(776), (—) balayages vers les potentiels positifs et les potentiels négatif.
Dans le domaine des potentiels les plus négatifs ou l'électrode porte une forte charge σ négative l'excès d'électrons présents à la surface du métal crée un champ électrique de répulsion qui repousse le pôle hydroxyle des molécules d'eau. Dans ce domaine de potentiel l'interaction métal - solution est uniquement due au faible caractère hydrophile de l'or qui maintient le contact entre le métal et les molécules d'eau de la solution. La pression exercée par la solution électrolytique sur la surface donc très faible. Par conséquent dans le cas d'une électrode Au(111) la surface est alors essentiellement soumise aux forces tangentielles de compression induites par le stress et la reconstruction atomique (22 × √3) peut apparaître comme sous vide. Le pcn le plus positif, situé à +0,330 V/(e.c.s.), obtenu lors du balayage vers les potentiels positifs (Fig. 8), correspond donc à la structure atomique reconstruite (22 × √3).
Lors du balayage vers les potentiels positifs, l'interface métal–solution commence à se charger positivement après le pcn, c'est-à-dire après +0,330 V/(e.c.s.). Cette diminution de la densité électronique à la surface du métal crée un champ électrique d'attraction qui attire le pôle hydroxyle des molécules d'eau et accroît la force d'adsorption du solvant. Cette force d'attraction s'exerce également sur les ions de l'électrolyte et provoque progressivement une faible adsorption spécifique des anions F–. Dans ces conditions, la pression exercée par la solution électrolytique sur la surface du métal peut générer au niveau des lignes de faute d'empilement atomique des forces tangentielles antagonistes aux forces de compression induites par le stress et provoquer ainsi la disparition progressive de la reconstruction (22 × √3). Les domaines reconstruits ayant une densité atomique supérieure d'environ 4% à celle des domaines non reconstruits, la suppression de la reconstruction entraîne obligatoirement une extension de la surface. La réintégration dans le réseau cfc des atomes en excès situés dans les zones de faute d'empilement n'est donc possible que si un degré de liberté supplémentaire créé par un bord de marche permet l'extension de la surface. Or, à l'échelle nanométrique la surface d'une électrode Au(111) n'est jamais parfaite, et sa structure réelle est constituée d'un ensemble de grandes terrasses (111) disposées par étages et délimitées à leur périphérie par différent types de marches monoatomiques. Une telle structure peut permettre une extension des terrasses (111) et, dans ces conditions, la pression exercée par la solution peut alors se transformer en une force tangentielle de glissement qui permet de replacer dans leurs sites initiaux du réseau cfc les atomes situés sur les lignes de fautes d'empilement et dans les secteurs hc.
Les domaines non reconstruits ainsi formés sont localisés sur le pourtour des terrasses (111) et leur largeur dépend du rapport entre les forces crées par la pression de la solution et celles générées par le stress. La pression exercée par la solution électrolytique dépend de la valeur de la charge superficielle σ, c'est-à-dire du potentiel imposé. Plus le potentiel est positif par rapport au pcn, plus la surface des domaines non reconstruits s'accroît. Si, à la borne positive du domaine de polarisation, la pression est insuffisante pour annuler totalement les forces de compression dues au stress, la reconstruction (22 × √3) ne disparaît pas entièrement. Dans ces conditions, la surface de l'électrode présente une structure atomique mixte, c'est-à-dire composée de secteurs reconstruits et de secteurs non reconstruits. La capacité différentielle d'une telle structure mixte est égale à la somme de la capacité différentielle de chacun des secteurs. Chaque secteur étant caractérisé par sa propre courbe C(E), la forme globale de la courbe C(E) d'une structure mixte dépend de la proportion de chacun des secteurs, et le potentiel de son minimum de capacité différentielle est situé entre les pcn des secteurs reconstruits et non reconstruits.
Or, les caractéristiques de la courbe C(E) de l'électrode Au(111) correspondant au balayage vers les potentiels négatifs (Fig. 8) indiquent que la surface de l'électrode possède probablement ce type de structure superficielle mixte. En effet, le potentiel de son minimum de capacité différentielle situé à +0,280 V/(e.c.s.) occupe bien une position intermédiaire entre +0,330 V/(e.c.s.) correspondant au pcn de la surface reconstruite Au(111)(22 × √3) et +0,225 V/(e.c.s.), correspondant au pcn des terrasses non reconstruites (111)(1 × 1) de Au(776).
Cette structure superficielle mixte résulte donc d'un état d'équilibre entre les forces permanentes de contrainte dues au stress et les forces antagonistes variables générées par la pression de la solution. Par conséquent, le processus de formation de cette structure mixte est réversible, c'est-à-dire que la suppression de la pression de la solution provoque automatiquement la réapparition de la reconstruction (22 × √3) dans la région du bord des marches. Ainsi, lors du balayage en potentiel vers les potentiels négatifs, la pression exercée par la solution diminue avec la charge positive, et lorsque la charge à la surface du métal devient négative, les forces de contrainte dues au stress reconstruisent progressivement l'ensemble des terrasses (111). Cette réversibilité du processus de reconstruction atomique de la surface d'une électrode Au(111) au contact d'une solution électrolytique est donc à l'origine du phénomène d'hystérésis observé sur les courbes C(E) (Fig. 8). Dans une étude précédente du plan Au(111) effectuée par Kolb et al. [16] avec des solutions acides de HClO4 0,01 M qui permettent à la fois de déplacer la borne positive du domaine de potentiel jusqu'à +0,6 V/(e.c.s.) et d'utiliser des anions ClO4– qui s'adsorbent plus fortement que F–, un pcn situé à +0,230 V/(e.c.s.) a été atteint lors du balayage vers les potentiels négatifs. Ce résultat confirme donc que, lorsque la densité de charge positive est suffisamment grande et que l'adsorption ionique est plus forte, la pression exercée par la solution électrolytique sur la surface peut faire disparaître totalement la reconstruction (22 × √3).
Dans le cas de la face Au(776), l'identité des courbes C(E) (Fig. 2) correspondant aux deux sens du balayage en potentiel implique que la reconstruction des terrasses (111) disparaît lors de la première polarisation positive et qu'elle ne réapparaît plus dans le domaine des charges négatives. Cette différence majeure de comportement entre les terrasses (111) de Au(776) et la surface d'une électrode monocristalline Au(111) provient de la dimension des terrasses (111) présentes sur ces deux types de surface. Dans le cas de Au(776), les terrasses (111) d'une largeur de quatorze rangées atomiques sont trop petites pour permettre la formation complète de la structure en chevrons de la reconstruction (22 × √3), et un nouvel arrangement des lignes de fautes d'empilement en forme de V apparaît alors sur les terrasses (Fig. 5). Cette morphologie particulière, due à la relaxation atomique en bordure des marches qui réduit les domaines reconstruits hc, signifie que les forces de contrainte sur les petites terrasses de Au(776) sont plus faibles que celles qui s'exercent sur les grandes terrasses d'un monocristal Au(111). Ces forces de contrainte résiduelles, qui devraient provoquer la reconstruction des petites terrasses (111) dans le domaine des charges négatives, sont alors trop faibles, et la pression exercée par l'adsorption des molécules d'eau sur le métal crée des forces antagonistes suffisantes pour les annuler. Ceci explique que les terrasses de la face Au(776) conservent toujours la structure non reconstruite (111)(1 × 1) dans tous le domaine de polarisation et que les courbes C(E) de Au(776) sont identiques dans les deux sens du balayage en potentiel.
Cela confirme donc que la courbe C(E) des terrasses (111) obtenue à partir des courbes C(E) de Au(776) et de Au(332) (Fig. 7) est bien caractéristique du comportement électrochimique de la structure non reconstruite Au(111)(1 × 1).
3.3 Comparaison du comportement électrochimique des structures facettées et non facettées de Au(554) et de Au(775)
L'ensemble de ces observations montre que la présence de la reconstruction sur les terrasses (111) au contact d'une solution électrolytique dépend essentiellement de la largeur de celles-ci. Par conséquent, si cette reconstruction n'apparaît pas sur les terrasses (111) de Au(776), qui ont une largeur de 14 atomes, alors il est probable qu'elle n'existe pas non plus dans le cas des structures non facettées des faces vicinales Au(554) et Au(775), qui ont respectivement des terrasses (111) d'une largeur de dix et de sept atomes. Les terrasses (111) n'étant pas reconstruites, le bord des marches doit également avoir une structure {111}. Donc, par analogie avec Au(776), ces faces vicinales non facettées ont probablement aussi un comportement électrochimique assimilable à celui d'une surface composée de secteurs Au(332) et de secteurs Au(111)(1 × 1).
Les structures facettées des orientations Au(775) et Au(554) étant constituées de facettes Au(776) et Au(332), leur comportement électrochimique doit également être assimilable à celui d'une surface composée de domaines Au(332) et Au(111)(1 × 1). On en déduit que la structure facettée et la structure non facettée de ces deux faces vicinales doivent avoir le même comportement électrochimique. Or, le diagramme de la Fig. 9 montre précisément que les courbes C(E) correspondant aux deux types de structure, facettée et non facettée, de Au(554) et de Au(775) sont pratiquement identiques. Ces mesures confirment donc bien, d'une part, que l'ensemble des marches {111} des surfaces non facettées a un comportement électrochimique identique à celui des facettes Au(332) et, d'autre part, que les terrasses (111) des surfaces non facettées ont également le même comportement électrochimique que les terrasses (111)(1 × 1) des facettes Au(776).

Courbes de capacité différentielle C(E) dans une solution de NaF 10 mM, 10 mV s−1, 5,63 Hz ; Au(775), (—) surface facettée, (⋯) surface non facettée ; Au(554), (- - -) surface facettée, (–·–·–) surface non facettée.
3.4 Détermination de la charge interfaciale de la structure facettée de Au(554) et de Au(775)
La possibilité d'assimiler le comportement électrochimique des faces Au(775) et Au(554), facettées ou non facettées, à celui d'une association de secteurs Au(332) et Au(111)(1 × 1) constitue une étape importante dans cette voie de recherche, car elle donne la possibilité d'accéder à la fois à la charge locale et à la charge globale de l'interface métal/solution. En effet, les structures atomiques de Au(332) et de Au(111)(1 × 1) étant homogènes, chacun de ces domaines possède son propre pcn, et il est alors possible, à partir de leurs courbes C(E) respectives, de calculer la charge électrique superficielle de chaque domaine. Les taux d'occupation de chacun des domaines étant respectivement de 85% de Au(332) et de 15% de Au(111)(1 × 1) pour une surface Au(775) et de 58% de Au(332) et de 42% de Au(111)(1 × 1) pour une surface Au(554), il est possible de calculer la charge superficielle globale en fonction du potentiel σ(E) des faces Au(775) et Au(554). Lorsque, à un potentiel donné, les charges électriques des deux secteurs d'une face ont la même valeur et sont de signes opposés, la charge globale de la surface s'annule, et ce potentiel correspond alors au pseudo potentiel de charge nulle (pseudo-pcn) de la face étudiée.
Les diagrammes de la Fig. 10 pour l'orientation Au(775) et ceux de la Fig. 11 pour l'orientation Au(554) représentent trois types de courbes σ(E). Le premier type correspond aux courbes σ(E) des secteurs Au(332) et Au(111)(1 × 1), composant chacune des faces Au(775) et Au(554). Le second type correspond aux courbes théoriques de charge globale σ(E) des faces Au(775) et Au(554), obtenues en effectuant la somme des charges des secteurs Au(332) et Au(111)(1 × 1) de chacune des faces. Ces courbes théoriques de charge globale permettent de déterminer le pseudo-pcn de Au(775), qui est situé à +0,120 V/(e.c.s.), et celui de Au(554), qui est situé à +0,150 V/(e.c.s.). Enfin, le dernier type de courbe représenté sur les diagrammes (Figs. 10 et 11) est la courbe σ(E) expérimentale, qui est obtenue à partir de la courbe C(E) expérimentale et du pseudo-pcn de chacune des faces Au(775) et Au(554).

Détermination du pseudo-pcn de Au(775) à partir de la courbe de densité de charge σ(E) dans une solution de NaF 10 mM ; (- - -), 15% de terrasses Au(111)(1 × 1) ; (–·–·), 85% de Au(332) ; (⋯), Au(775) courbe calculée [15% Au(111)(1 × 1) + 85% Au(332)] ; (—), Au(775) courbe mesurée.

Détermination du pseudo-pcn de Au(775) à partir de la courbe de densité de charge σ(E) dans une solution de NaF 10 mM ; (- - -), 42% de terrasses Au(111)(1 × 1) ; (–·–), 58% de Au(332) ; (⋯), Au(554) courbe calculée [42% Au(111)(1 × 1) + 58% Au(332)] ; (—), Au(554) courbe mesurée.
La bonne coïncidence entre les courbes σ(E) théoriques et expérimentales, pour les deux faces vicinales Au(775) et Au(554), est l'ultime preuve que le comportement électrochimique de ces surfaces est bien assimilable à celui de l'association de deux secteurs d'orientations Au(332) et Au(111)(1 × 1).
4 Conclusion
Dans le domaine de potentiel où une électrode est idéalement polarisée, et en l'absence d'adsorption spécifique, la distance entre la surface du métal et les ions de l'électrolyte les plus proches est de l'ordre de quelques dixièmes de nanomètres. Cette proximité des ions de la couche double avec la surface peut former localement des nanocondensateurs électrochimiques avec des zones de la surface de dimension nanométrique, comme par exemple les zones des marches monoatomiques. Chaque nanocondensateur formé par chacune des marches {111} est autonome et, par conséquent, le comportement électrochimique de l'ensemble des marches {111} est indépendant de leur mode de répartition sur les terrasses (111) des faces vicinales. Cette autonomie des nanocondensateurs formés par les marches {111} explique la similitude du comportement électrochimique observé dans le cas des structures facettées ou non facettées des faces Au(554) et Au(775). En effet, que les zones des marches {111} soient juxtaposées, comme dans le cas des facettes Au(332) présentes sur les structures face tées, ou qu'elles soient séparées par des terrasses (111) de différentes largeurs, comme dans le cas des structures non facettées, la capacité différentielle globale de l'ensemble des marches {111} reste la même.
L'hypothèse de l'existence d'une hétérogénéité des propriétés électrochimiques des surfaces monocristallines à marches, que nous avions émise antérieurement lors de l'étude de faces vicinales de Au(111) à marches {100} [12] et qui nous avait conduit à évoquer pour la première fois la notion de pseudo-pcn pour caractériser ces surfaces, est donc confirmée par cette étude sur les faces vicinales à marches {111}.


