1 Introduction
Le PHPT [1–5] est obtenu à partir d'une solution de ThCl4 et de H3PO4 en considérant un rapport molaire . Le mélange est réalisé dans un pot en téflon hermétique, puis placé sur un banc de sable à 150 °C. Après formation initiale d'un gel, la précipitation conduit rapidement à un produit cristallisé (1 jour à 2 semaines). La structure cristalline du PDT (Th4(PO4)4P2O7, groupe d'espace Pcam, Z = 2) a pu être déterminée par des études couplées de diffraction des rayons X sur poudre et de RMN [1]. Les études de diffraction de rayons X n'ont pas permis jusqu'à présent de définir celle du PHPT. En revanche, elles ont montré que son diagramme de diffraction des RX n'était pas modifié entre la température ambiante et 900 °C, température à laquelle le PHPT se transforme en PDT de manière irréversible. Les expériences d'ATD et d'ATG montrent que si on ne dépasse pas cette température, le système réadsorbe en partie les molécules d'eau lors du refroidissement, molécules d'eau qu'il avait perdues lors de l'échauffement entre 160 et 200 °C (une ou deux molécules), puis vers 400 °C (perte de la dernière molécule d'eau). Au-dessus de cette température, il n'y a plus de perte de masse détectable, attestant que le produit est anhydre. À l'heure actuelle, il est difficile d'opter pour une formulation du type Th2(PO4)2HPO4,H2O plutôt que pour Th4(PO4)4P2O7,3H2O (présence ou non de groupements HPO4 et/ou de molécule H2O à côté de PO4 et/ou de P2O7). Devant cette difficulté, différentes expériences de RMN ont été conduites parallèlement à la diffraction des rayons X sur poudre. Dans cet article, nous présentons quelques résultats de RMN préliminaires obtenus en utilisant une acquisition simple en rotation à l'angle magique (une impulsion de 90° suivie de l'acquisition), et une acquisition REDOR, dans l'objectif d'apporter une réponse quant à la formulation des phases hydratées.
Les expériences ont été réalisées à l'aide d'un spectromètre Avance 300, en utilisant une sonde CPMAS à deux canaux. Au préalable, des mesures de temps de relaxation par une méthode de saturation ont permis d'évaluer le temps de relaxation spin réseau T1 du proton (de l'ordre de 0,2 s) et du phosphore (entre 50 et 100 s, suivant l'échantillon). Les résultats présentés ici concernent deux échantillons étudiés à température ambiante. L'échantillon noté E-120 correspond à du PHPT brut de synthèse à 120 °C avec séchage final sous air (en étuve) dans l'éthanol ; l'échantillon E-300 a été chauffé à 300 °C sous atmosphère inerte. Les échantillons sont refroidis jusqu'à température ambiante et les spectres enregistrés. Dans toutes les expériences, la durée d'une impulsion de 90° pour le proton est de 4 μs et de 3,57 μs (ν1 = 70 kHz) pour le phosphore. Les conditions de polarisation croisée ont été ajustées sur l'échantillon E-120. Pour le phosphore, les expériences MAS ont été réalisées à 10 kHz dans le cas d'une simple acquisition et des expériences CP, et à 13 kHz pour l'expérience REDOR. La reconstruction des spectres a été réalisée à l'aide du logiciel DMFIT [6] ; chaque raie a un profil du type x L + (1 – x) G, où L représente une forme lorentzienne et G une forme gaussienne.
2 Résultats et discussion
2.1 Spectres du proton
Les spectres du proton enregistrés en rotation à l'angle magique à la fréquence νr = 14 kHz sont reportés sur la Fig. 1. Ils montrent que la quantité de protons est plus élevée dans E-120, ce qui montre que le chauffage permet de différentier les échantillons par la quantité de molécules d'eau réabsorbées. De plus, le spectre de E-120 comporte des raies fines qui pourraient alors être attribuées à de l'eau faiblement liée, facile à éliminer lors du chauffage.
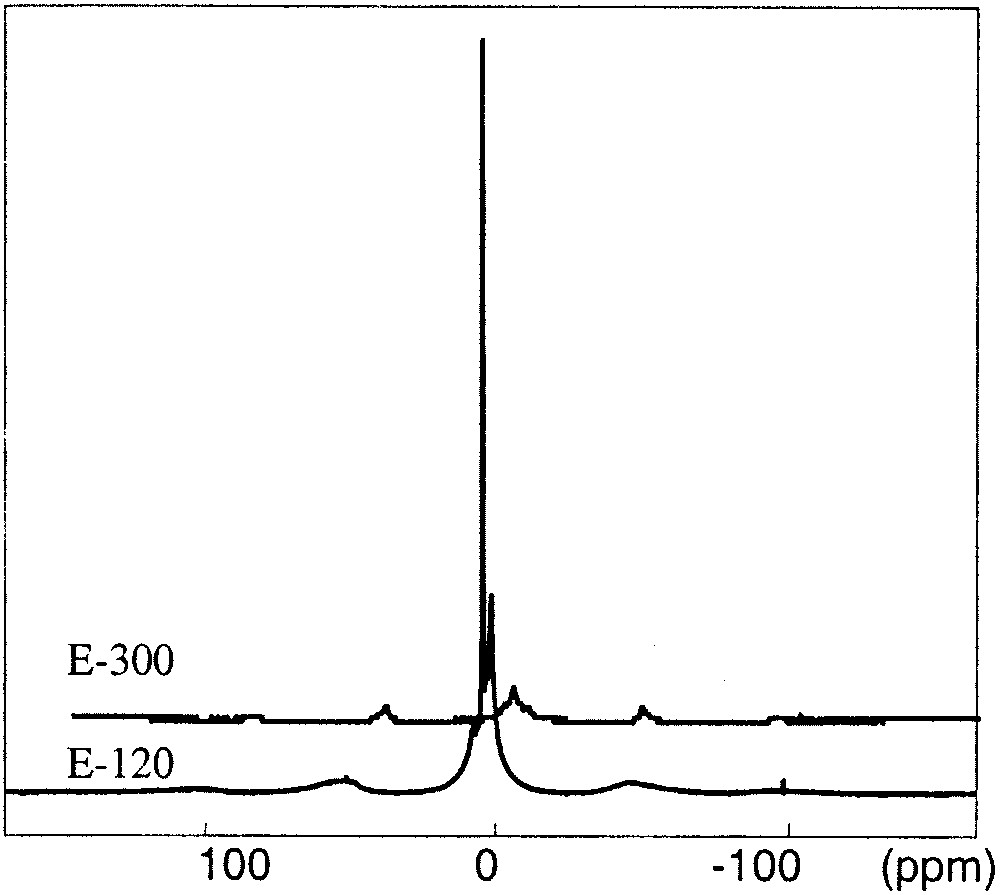
Spectres du proton pour les deux échantillons E-120 et E-300 en acquisition simple avec un délai de 2 s entre les transitoires. Le spectre de E-300 a été multiplié par 2. On observe clairement l'effet du traitement thermique.
2.2 Spectres du 31P
Les spectres du 31P obtenus au cours d'une acquisition simple (un pulse-acquisition) sont reportés sur la Fig. 2. Le délai entre chaque pulse est choisi suffisamment long pour obtenir des résultats quantitatifs. Pour chaque échantillon, le spectre comporte deux massifs : entre –4 et –11 ppm (α) et entre –16 et –21 ppm (β). La répartition est d'environ 33% pour le massif α et 66% pour le massif β pour les deux échantillons, ce qui correspond au rapport [P2O7]/[PO4] dans la formulation Th4(PO4)4P2O73 H2O. Il est important de noter que cette répartition est la même dans tous les échantillons que nous avons étudiés. Il est aussi important de noter que, dans le PDT, le massif α n'existe plus et que le massif β comporte alors cinq raies [1]. Enfin, dans l'échantillon E-300, le massif α se déplace vers le massif β.

Spectres du phosphore obtenus lors d'une simple acquisition avec un délai de 800 s entre deux transitoires. On distingue les deux régions associées aux massifs α (entre –4 et –11 ppm) et β (entre –17 et –21 ppm). Le massif α de E-300 se déplace vers le massif β (hauts champs). Les reconstructions des spectres conduisent à 33,3% pour α et à 66,6% pour β pour tous les échantillons. Les spectres sont normalisés, permettant ainsi de vérifier que les deux échantillons contiennent des quantités similaires de phosphore. Le spectre de E-300 est représenté en pointillés.
Pour attribuer l'origine des différents massifs, nous utilisons quelques résultats de la littérature. La position de la raie isotrope du 31P dans ThP2O7 cubique est à –26 ppm. Le spectre de Mg2P2O7 se situe dans le même domaine que celui du PDT. Pour Mg2P2O7H2O [7], les raies se trouvent déplacées entre –7 et –9 ppm, puis entre –4 et –10 ppm pour Mg2P2O73,5 H2O. Ainsi, les raies du P2O7 se situent entre –4 et –10 ppm et leur étalement se contracte en se déplaçant vers –10 ppm lorsque la quantité d'eau diminue. On observe le même comportement avec nos deux échantillons et nous pouvons proposer que les raies du massif α correspondent aux atomes de phosphore des groupements P2O7. Il est important de signaler que, quel que soit l'échantillon, les quantités de phosphore sont quasiment identiques et donc que le massif α représente la même quantité de phosphore pour chaque échantillon. Or, entre les échantillons E-120 et E-300, la quantité de protons est divisée par 8 au moins. Dans E-300, les entités ne peuvent pas être des HPO4, si elles l'avaient été dans E-120.
2.3 Polarisation croisée de 1H vers 31P
Afin d'obtenir des informations sur les voisinages protonés des phosphores, des expériences de polarisation croisée avec rotation à l'angle magique ont été réalisées à 10 kHz, avec des temps de contact τc de 100 μs, 250 μs, 500 μs, 1 ms, 5 ms et 10 ms. Dans E-120, l'intensité du massif β croît continûment jusqu'à τc = 10 ms, alors que le massif α croît jusqu'à 1 ms, puis décroît ensuite. Pour les deux autres échantillons, les intensités augmentent jusqu'à 10 ms et le transfert est moins efficace. Les résultats obtenus à 10 kHz et pour un temps de contact de 1 ms sont reportés sur la Fig. 3. L'échantillon E-120 est le plus sensible aux protons et les atomes de phosphore du massif α sont les plus proches des protons. Dans E-300, la répartition des protons et donc des molécules d'eau est plus homogène.

Spectres du phosphore en polarisation croisée 1H–31P obtenus dans les mêmes conditions pour les deux échantillons E-120 et E-300 (en pointillés). Le transfert de polarisation est plus efficace sur E-120 que dans E-300 ; pour les deux échantillons, il se fait préférentiellement sur le massif α.
2.4 Expériences REDOR (Rotational Echo Double Resonance), CP-REDOR [8,9]
Les expériences de polarisation croisée étant également sensibles à la dynamique de transfert, nous les avons complétées par des expériences REDOR afin d'évaluer les distances 31P–1H. Elles consistent en un écho sur le canal du phosphore et en l'application d'un train d'impulsions π sur le proton. Ces impulsions, synchronisées avec la rotation de l'échantillon, ont pour effet de recoupler l'interaction dipolaire hétéronucléaire avant d'observer le phosphore. Cette interaction, qui introduit un déphasage du signal RMN et qui est moyennée par la rotation à l'angle magique, permet d'accéder à la distance entre deux noyaux. Deux expériences sont alors réalisées : l'une avec le train d'impulsions sur le canal du proton et l'autre sans train d'impulsions. Quand ce train d'impulsions est présent, l'interaction en question réintroduit le déphasage dipolaire et réduit le signal de l'écho S(N) où N est le nombre de cycles d'impulsions dans le train. Une comparaison entre le signal S avec recouplage et S0 sans recouplage, pour différentes longueurs du train de pulses, permet la construction de la courbe REDOR. Cette courbe, d'équation :
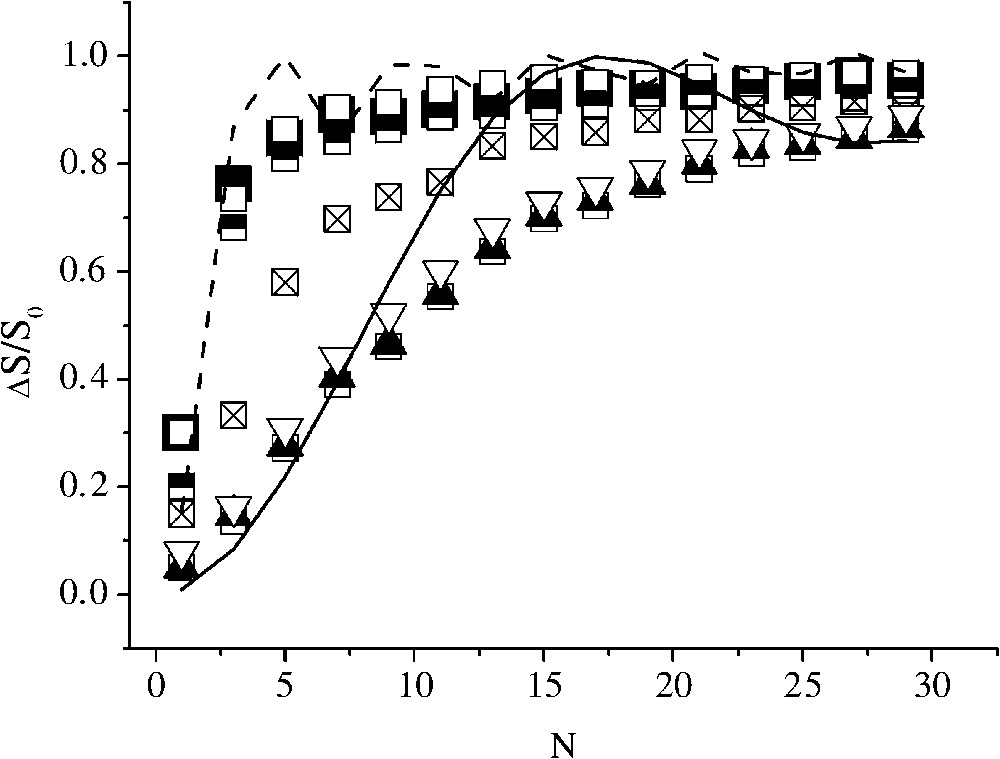
Échantillon E120 : expérience REDOR. Les carrés correspondent aux raies du massif α. Les phosphores des deux massifs ne voient pas de façon identique les protons. Les courbes encadrent les valeurs ωD = 48 000 Hz et 8000 Hz correspondant à des distances d(1H–31P) comprises entre 2,1 et 3,3 Å environ.

Échantillon E-300 : expériences REDOR. Les courbes en pointillés encadrent ωD/2π = 350 Hz et 700 Hz. Le déphasage REDOR n'est pas complet, mais le plateau à 0,2 permet de déduire qu'un peu plus de 20% des atomes de phosphore voient des protons.
Dans E-300, le déphasage REDOR (Fig. 5) n'étant pas complet, on ne peut donc pas avoir d'informations directes sur les distances, mais il donne le pourcentage de phosphores liés à des protons – nous remercions le referee anonyme pour cette remarque – à partir du plateau de saturation observé, soit de l'ordre de 20%, ce qui est cohérent avec les résultats de polarisation croisée. Cependant, ce résultat indique que les protons dans E-300 ne sont pas liés au phosphore car, bien qu'il y ait la même quantité d'atomes de phosphore que dans E-120, il y a bien moins de protons.
Les informations sur les distances sont obtenues à partir du signal CP-REDOR dans lequel les phosphores observés et avec lesquels nous étudions le signal REDOR sont ceux liés au protons. Comme cela peut être observé sur la Fig. 6, le signal REDOR est presque totalement déphasé. Comme précédemment, la pente à l'origine permet d'évaluer les distances P–H. Elles sont comprises entres 2,3 et 3,7 Å et sont donc un peu plus grandes que dans E-120 (entre 2,1 et 3,4). Ce résultat suggère alors fortement que l'on est en présence d'eau et non de HPO4, dans lequel les distances seraient identiques dans les deux composés et de l'ordre de 2,4 à 2,6 Å.
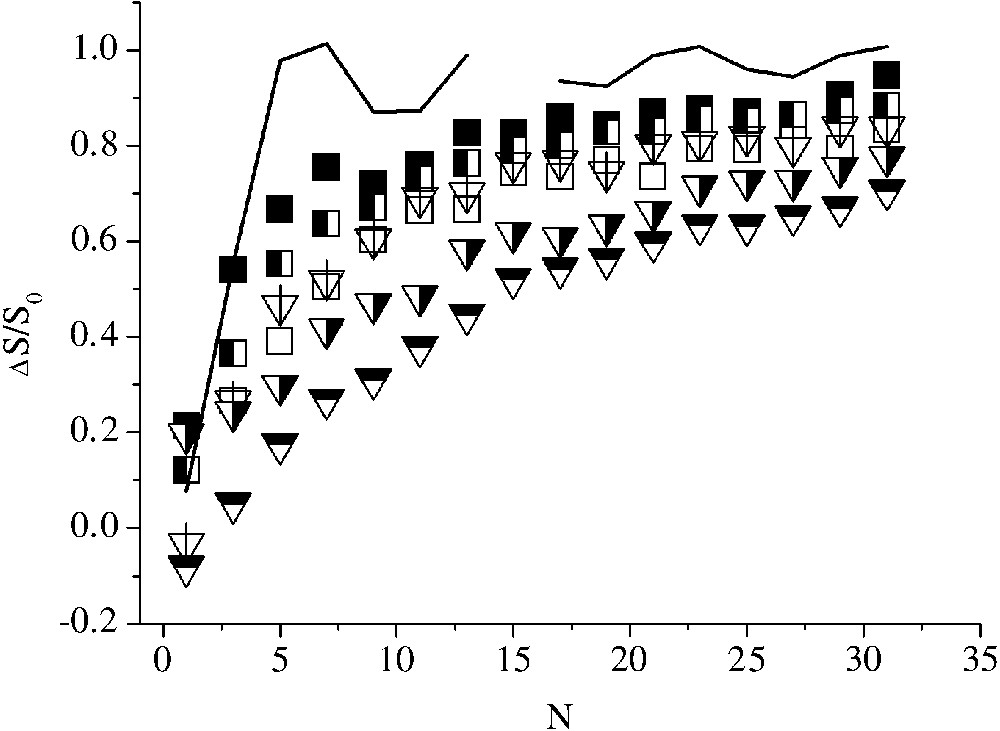
Échantillon E-300 : expériences CP-REDOR avec un temps de contact court de 143 μs pour éviter la diffusion de spin. Le déphasage CP-REDOR est presque complet. La courbe correspond à une interaction ωD/2π = 24 000 Hz, soit une distance limite de 2,33 Å.
En conclusion les résultats précédents suggèrent fortement qu'à partir d'un traitement à 300°C (E-300) la formulation pourrait être Th4(PO4)4P2O7x H2O pour le PHPT dans les différents échantillons. Pour l'échantillon E-120, la conclusion est incertaine, les distances trouvées pour le massif α restent proches de la somme des liaisons P–O et O–H. D'autres expériences RMN sont en cours pour confirmer ces résultats ainsi que des expériences Raman qui pourraient apporter des compléments d'informations à travers les fréquences caractéristiques des différentes entités.


