1 Introduction
Les oxydes des métaux de transition présentant plusieurs états d'oxydation ont fait l'objet de nombreuses études. Notamment, les phases de type pérovskites au cuivre supraconductrices à haute température critique ont été d'un grand intérêt, tant sur le plan de la recherche fondamentale que des applications technologiques. Les oxydes de structure du type pyrochlore connaissent aussi des applications intéressantes [1]. Le pyrochlore est un minéral naturel répondant à la formule (Na,Ca,U)2(Nb,Ta)2O6(OH,F) [JCPDS/13-254]. Il a été le premier composé d'une famille de formulation A2B2X6X′. Le système cristallin est cubique, de groupe d'espace Fdm et de paramètre de maille a ≈ 10 Å ; la maille comporte huit unités formulaires [2].
Lors de travaux antérieurs [3], un nouveau composé pyrochlore à base de cuivre, d'antimoine et de bismuth de formule (Bi1,524Cu0,476)[Sb1,524Cu0,476]O7+δ a été mis en évidence, avec un paramètre de maille a = 10,430(1) Å. Dans ce composé, le bismuth, de rayon ionique élevé, occupe le site A, de coordinence VIII, et l'antimoine, de rayon ionique faible, occupe le site B, de coordinence VI octaédrique, en accord avec les conditions de stabilité de la structure pyrochlore. Le cuivre est distribué entre les deux sites A et B en proportions égales, comme il a été déjà signalé dans les travaux de Champarnaud et al. [4]. La résistivité électrique du composé à température ambiante est de l'ordre de 105 Ω cm et la valeur du moment effectif μCu du cuivre, égale à 2,27 μB, nettement supérieure à celle observée habituellement pour Cu2+, à savoir 1,73 μB.
Dans ce travail, nous avons entrepris de synthétiser deux nouvelles solutions solides (Bi1,524–xCaxCu0,476)-[Sb1,524Cu0,476]O7+δ et (Bi1,524–xPbxCu0,476)[Sb1,524-Cu0,476]O7+δ et d'étudier leurs propriétés magnétiques et électriques.
2 Expérience
Les composés polycristallins ont été synthétisés par la méthode classique de réaction à l'état solide des oxydes Sb2O3 (99 %), Bi2O3 (99,9 %), CuO (99 %), CaO (99 %) et PbO (98 %) (Aldrich Chemical Company Ltd). Les précurseurs pesés selon les proportions stœchiométriques requises ont été intimement mélangés par un broyage minutieux dans un mortier en agate, jusqu'à l'obtention d'un mélange parfaitement homogène. Celui-ci subit un premier chauffage à 700 °C pendant 24 h, avant d'être de nouveau broyé. Les échantillons subissent ensuite deux cycles de chauffage–broyage à une température de 900 °C pendant 72 h. Les échantillons sont finalement broyés finement et compactés sous forme de pastilles de 13 mm de diamètres lesquelles sont soumises à un frittage à 1000 °C pendant 24 h.
La caractérisation des échantillons par diffraction des rayons X a été réalisée à l'aide d'un diffractomètre automatique à poudre de type X'pert opérant en géométrie focalisante de type Bragg-Brentano (θ/2θ) et utilisant la longueur d'onde κα du cuivre.
Les mesures électriques ont été effectuées par la méthode des quatre pointes à température ambiante. Les mesures de susceptibilité magnétique ont été réalisées à l'aide d'une balance de Faraday dans une gamme de température comprise entre 80 et 600 °K. La détermination du degré d'oxydation de l'antimoine dans les composés a été effectuée par spectrométrie Mössbauer de 121Sb.
3 Résultats et discussion
3.1 Diffraction des rayons X
La solution solide (Bi1,524–xCaxCu0,476)[Sb1,524Cu0,476]O7+δ existe dans le domaine 0 ≤ x ≤ 0,30. La Fig. 1 donne l'allure du diffractogramme du composé x = 0. Au-delà de cette fraction, on assiste à un mélange de phase. En effet, le diffractogramme de la composition x = 0,40 (Fig. 1) montre la présence de raies supplémentaires. Le Tableau 1 regroupe les positions 2θ, l'intensité relative et les indices de Miller des principales raies indexées dans une structure pyrochlore du composé à x = 0.
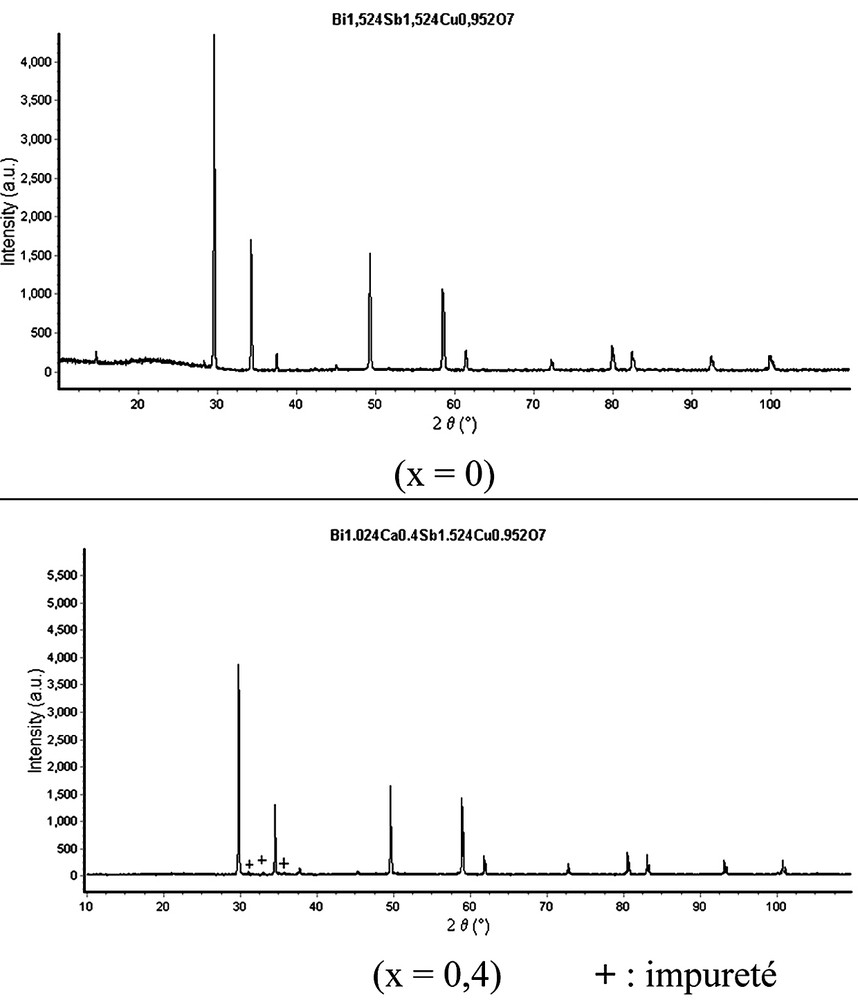
Diffractogrammes des rayons X des composés x = 0 et 0,40 de la solution solide (Bi1,524–xCaxCu0,476)[Sb1,524Cu0,476]O7+δ.
| N | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
| 2θ (°) | 14,64 | 28,47 | 29,72 | 34,35 | 37,64 | 45,17 | 49,43 | 58,80 | 61,60 | 72,42 | 80,06 | 82,71 | 92,64 | 99,64 |
| I/Imax | 3,11 | 1,76 | 100 | 33,43 | 5,12 | 1,58 | 41,37 | 40,25 | 8,85 | 4,00 | 7,32 | 5,98 | 2,88 | 2,89 |
| hkl | 111 | 311 | 222 | 400 | 331 | 511 | 440 | 622 | 444 | 800 | 662 | 840 | 844 | 10 22 |
Les phases obtenues pures cristallisent dans le système cubique avec le groupe d'espace Fdm. L'affinement du paramètre de maille révèle une diminution régulière de celui-ci, en accord avec la différence entre les rayons ioniques du bismuth (RVIII = 1,17 Å) et du calcium (RVIII = 1,12 Å) [5] (Fig. 2).
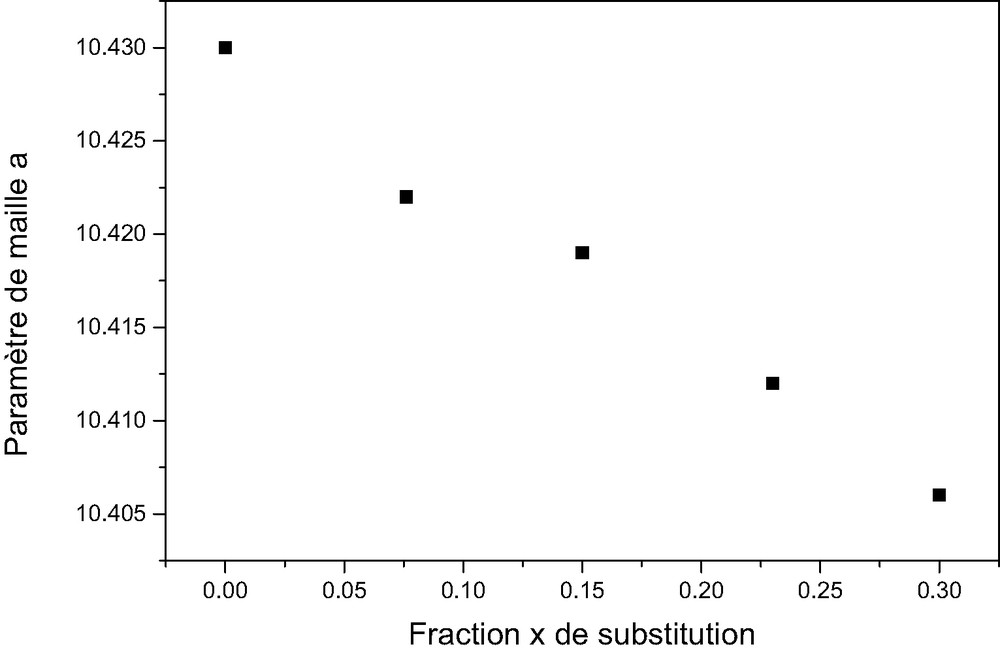
Variation du paramètre de maille a en fonction de la fraction x de substitution de la solution solide (Bi1,524–xCaxCu0,476)-[Sb1,524Cu0,476]O7+δ.
La solution solide au plomb (Bi1,524–xPbxCu0,476)[Sb1,524Cu0,476]O7+δ est formée jusqu'à x = 0,26. L'évolution du paramètre de maille a affiné en fonction du taux x de plomb semble être irrégulière, bien que le rayon ionique du plomb (RVIII = 1,29 Å) soit supérieur à celui du bismuth (Tableau 2).
| Fraction x | 0 | 0,1 | 0,15 | 0,20 | 0,23 | 0,26 |
| Paramètre a (Å) | 10,430(1) | 10,441(5) | 10,435(9) | 10,446(6) | 10,4357(9) | 10,435(1) |
L'évolution irrégulière du paramètre de maille a été déjà rencontrée dans des travaux où le plomb, un cation à paire d'électrons non liés inerte « E*Pb » substituant partiellement le bismuth un cation à paire d'électrons non engagés « E*Bi » [6], qui aurait pour conséquence deux effets contradictoires :
- ● la diminution de la distorsion ferait diminuer le paramètre a de maille ;
- ● la taille plus grande de l'ion Pb ferait augmenter le paramètre a.
Il y a probablement une compétition entre l'effet de taille et l'effet de la paire d'électrons non liée.
3.2 Spectrométrie Mössbauer de 121Sb
Les spectres Mössbauer de 121Sb obtenus à température ambiante, pour les trois composés x = 0 ; x(Ca) = 0,23 et x(Pb) = 0,26 (Fig. 3), se présentent sous la forme d'un singulet. Les analyses de ces spectres ont mis en évidence la présence d'un seul site d'antimoine dans la maille. Les valeurs du déplacement isomérique (δ), comprises entre 8,48 et 8,55 mm/s (Tableau 3) par rapport à InSb, sont en accord avec l'état d'oxydation +5 de l'ion Sb dans tous les échantillons, tandis que les valeurs observées pour l'éclatement quadripolaire (Δ) sont nulles, mettant en évidence une répartition sphérique des charges autour des noyaux Sb.
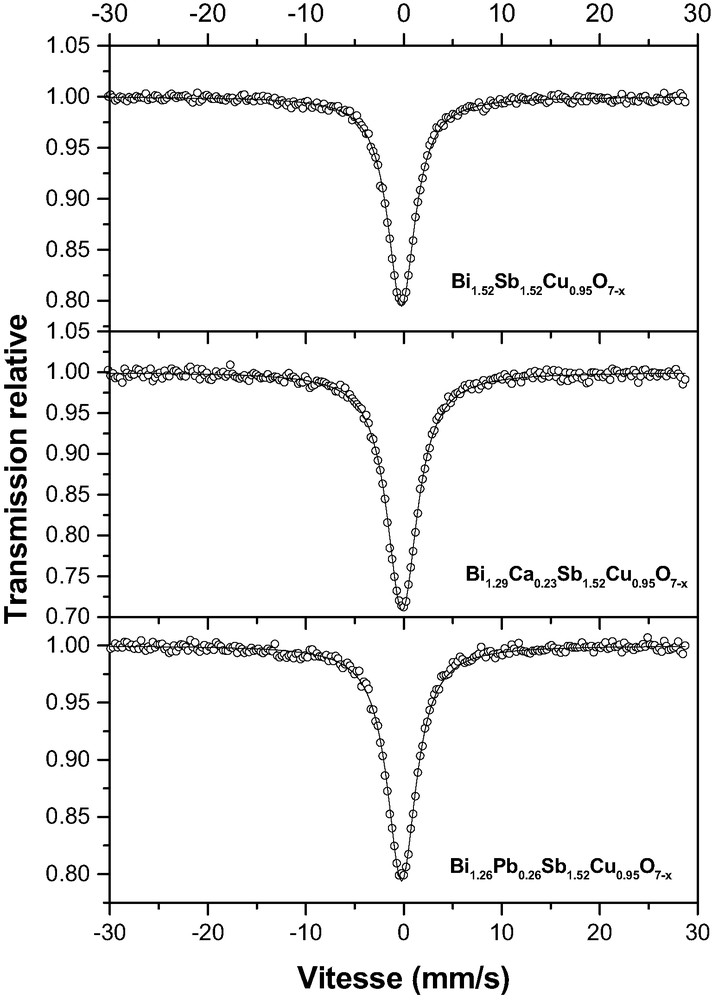
Spectres Mössbauer de 121Sb à 293 °K des composés x = 0 ; xCa = 0,23 et xPb = 0,26.
| Composés | δ (mm/s) | Δ (mm/s) | Γ (mm/s) | Attribution |
| Bi1,52Sb1,52Cu0,95O7 | +8,479 (7) | – | 1,57 (2) | SbV |
| Bi1,29Ca0.23Sb1,52Cu0,95O7 | +8,552 (9) | – | 1,66 (3) | SbV |
| Bi1,26Pb0.26Sb1,52Cu0,95O7 | +8,505 (9) | – | 1,74 (3) | SbV |
3.3 Susceptibilité magnétique
La Fig. 4 présente l'évolution des courbes (T) de la solution solide au calcium. Nous remarquons qu'il existe une diminution de la susceptibilité magnétique lorsque le taux de substitution x augmente. Le calcul de la valeur du moment effectif (MCu) de l'ion de cuivre dans le domaine paramagnétique (300–600 °K) (Tableau 4) a révélé aussi une décroissance de cette valeur de 2,38 à 1,49 μB, quand x croît de 0 à 0,30 respectivement.

Inverse de la susceptibilité magnétique molaire en fonction de la température de la solution solide (Bi1,524–xCaxCu0,476)-[Sb1,524Cu0,476]O7+δ.
| Fraction x | 0 | 0,15 | 0,30 |
| Moment effectif MCu (μβ) | 2,38 | 2,06 | 1,49 |
| Valeur de δ calculée | +0,329 | +0,181 | –0,1818 |
Ces résultats montrent que, pour les composés x = 0 et 0,15, ces valeurs sont plus élevées que la valeur théorique de l'ion Cu2+ (M = 1,73 μB), si on ne tient compte que du couplage entre les spins (, S = 1/2). Plusieurs hypothèses pourraient être avancées :
- ● soit cette augmentation de M est due au fait que ces composés contiennent un excès d'oxygène δ, qui engendre une oxydation partielle du Cu2+ en Cu3+, comme dans le cas de nombreux composés de type pyrochlore [7–10]. Mais, en tenant compte des valeurs du moment effectif habituellement observées pour les ions Cu3+ et Cu2+ (2,83 et 1,73 μB respectivement) et de celle de notre composé non substitué (x = 0 et MCu = 2,38 μB), l'estimation sur la charge de l'ion Cu dans ce composé a conduit à une charge +2,59 ; nous serions donc en présence d'une phase à valence mixte du cuivre, avec δ = 0,329. Cette dernière valeur nous semble élevée pour un composé synthétisé à l'air comme celui-ci. Il est à noter aussi que nous n'avons pas pu déterminer ce taux δ par un dosage de type iodométrique ou par une ATG en atmosphère réductrice à cause de la faible solubilité de ces produits en solution et de la volatilité du bismuth, respectivement ;
- ● soit les valeurs élevées de MCu dans x = 0 et 0,15 sont liées au schéma d'énergie des ions Cu2+ occupant ensemble avec les ions Bi3+ un site de symétrie cubique (coordinence VIII). Cette symétrie implique à ces ions Cu2+ la configuration eg4t2g5 donnant l'existence d'un trou dans la bande t2g, cela pouvait entraîner un couplage spin–orbite qui, par conséquent, pourrait faire augmenter la valeur du moment effectif de Cu2+ de ces phases ;
- ● soit dans le site cubique, la présence de l'ion Cu2+ beaucoup plus petit que l'ion Bi3+ entraîne un réarrangement des voisins du cuivre et par conséquent, peut conduire à une coordinence tétraédrique plus adaptée à la taille de cet ion. Avec cette symétrie, le moment magnétique effectif de l'ion Cu2+ peut varier d'une manière notable en fonction de la température et il peut atteindre une valeur élevée (2,25 μB à 300 °K) [11]. La légère courbure observée à basse température (< 300 °K) sur les courbes (T) de nos composés (encart de la Fig. 4) semble être en accord avec cette considération. Cependant, même si dans ces phases, 50 % des ions cuivre avaient cette coordinence, cela ne pourrait pas faire augmenter la valeur du moment effectif total, observé pour l'ensemble des deux types de sites de cuivre dans la structure, jusqu'à 2,38 μB.
De plus, l'observation d'une diminution importante de MCu dans les phases substituées au calcium laisse penser que le taux d'oxygène est réduit lorsqu'on substitue un ion trivalent (Bi3+) par un ion divalent (Ca2+). Cela pourrait éventuellement entraîner une réduction de la charge du cuivre, notamment pour le composé x = 0,30, dont le MCu a une valeur particulièrement faible (1,49 μB). Cependant, nous n'avons pas pu vérifier ces réductions du taux d'oxygène et de la charge du cuivre par les méthodes de dosage habituelles, comme nous l'avons indiqué plus haut.
Dans la solution solide (Bi1,524–xPbxCu0,476)-[Sb1,524Cu0,476]O7+δ, la variation du moment effectif du cuivre avec la substitution du bismuth par le plomb est moins marquée qu'avec la substitution par le calcium ci-dessus. La Fig. 5 donne l'allure de la courbe de l'inverse de la susceptibilité magnétique molaire en fonction de la température pour x = 0 et x = 0,26 ; la valeur de MCu décroît de 2,38 à 2,11 μB, respectivement. Cela nous laisse penser que le taux d'oxygène est moins affecté par la substitution au plomb que par celle au calcium. Cet effet est probablement dû à l'oxydation d'une partie du Pb2+ en Pb4+ (RPbVI = 0,775 Å) occupant le site B, tandis qu'une partie du cuivre passerait en site A. L'occupation du site B par le plomb a été déjà observée dans quelques composés de type pyrochlore, de formule Ln2Pb2O7 (Ln = La–Gd) [12] et Eu2B2O7 (B = Ti, Ru et Pb) [13,14] et se rencontre aussi dans des composés au plomb en coordinence VI, de formule A2PbO4 (A = Ca [15], Sr [16] et Cd [17]). Par ailleurs, le plomb peut aussi occuper le site A : on peut donner l'exemple de Pb2B2O7–x (x ≈ 1, B = Ru, Re et Ir) [18]. Cela nous laisse penser que le plomb serait distribué dans les deux sites du composé selon la formule (Bi3+1,524–xPb2+x–yCu2+0,476+y)(Sb5+1,524Cu2+0,476–yPb4+y)O2-7+δ.
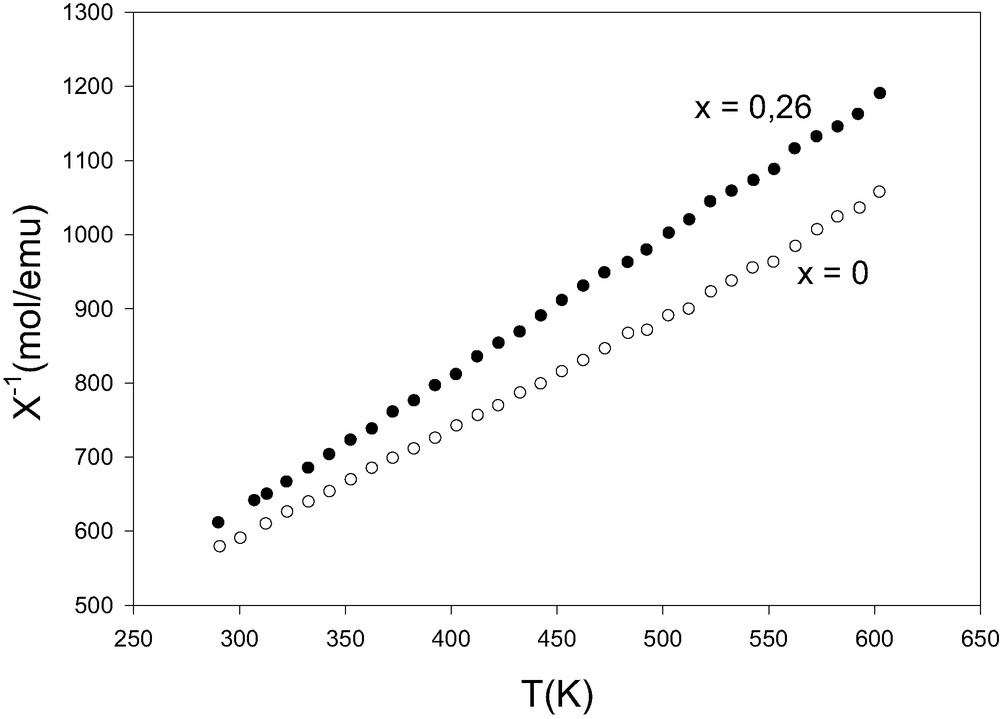
Inverse de la susceptibilité magnétique en fonction de la température de la solution solide (Bi1,524–x PbxCu0,476)[Sb1,524Cu0,476]O7+δ ; x = 0 et x = 0,26.
Les mesures électriques effectuées sur tous les échantillons à température ambiante par la méthode des quatre pointes donne une résistivité de l'ordre de 105 Ω cm.
4 Conclusion
Dans ce travail, deux solutions solides de type pyrochlore ont été synthétisées. La solution solide (Bi1,524–xCaxCu0,476)[Sb1,524Cu0,476]O7+δ avec 0 ≤ x ≤ 0,30 est caractérisée par une diminution régulière du paramètre a de la maille cubique et du moment effectif du cuivre en fonction de la fraction x de substitution. En revanche, pour la solution solide (Bi1,524–xPbxCu0,476)[Sb1,524Cu0,476]O7+δ avec 0 ≤ x ≤ 0,26, l'évolution du paramètre de maille n'est pas régulière ; elle est corrélée à la présence des « paires d'électrons non liées ». La variation du moment effectif du cuivre MCu = f(x) est moins forte que dans le cas de la substitution au calcium. La spectrométrie Mössbauer de 121Sb a confirmé le degré d'oxydation +5 de l'antimoine dans ces deux solutions solides. Ces résultats et les mesures de susceptibilité magnétique laissent penser que la substitution du bismuth par le calcium a une influence sur le comportement magnétique du cuivre.
Remerciements
Les auteurs remercient J. Olivier-Fourcade et J.-C. Dumas de l'équipe Mössbauer du laboratoire des agrégats moléculaires et matériaux inorganiques, université Montpellier-2, France, pour l'étude en spectroscopie Mössbauer de 121Sb.


