1 Introduction
Des solutions alternatives aux procédés existants de traitement de l'eau sont développées en prévision d'une plus sévère réglementation concernant la protection de l'environnement. Récemment, de nouvelles technologies sont apparues pour traiter les eaux polluées sous le vocable d'Advanced Oxidation Technologies (AOTs) [1–8]. Parmi ces AOTs, la photocatalyse hétérogène sur le dioxyde de titane se révèle comme une solution potentielle pour l'élimination de composés organiques [9–12]. Le principe de la méthode repose sur la production de radicaux lorsque le photocatalyseur, semi-conducteur, est irradié par des photons d'énergie égale ou supérieure à l'énergie de sa bande interdite [13,14]. Les radicaux formés, très réactifs, tels que HO2 et OH, induisent alors des réactions d'oxydation de molécules organiques par hydroxylation ou des réactions de décarboxylation [15,16].
Ce travail fait suite aux résultats relatifs à la photodégradation du β-naphtol, choisi comme molécule de référence [17]. Notre étude a pour objectif de vérifier l'efficacité de la photocatalyse hétérogène sur le TiO2 pour la dégradation et la minéralisation du β-naphtol en CO2 et H2O. Nous avons étudié l'influence de la température et l'effet des ions Cl−, SO42−, HCO3−, NO3−, Fe3+, Cu2+, Cr3+, de l'éthanol et du peroxyde d'hydrogène sur la vitesse initiale de disparition du β-naphtol.
2 Partie expérimentale
2.1 Réactifs
Le β-naphtol est un produit Fluka (pureté > 99%) utilisé sans purification préalable. Les sels utilisés (chlorure de sodium, sulfate de sodium, hydrogénocarbonate de sodium et nitrate de sodium), ainsi que l'acétonitrile, l'éthanol et le peroxyde d'hydrogène sont des produits Prolabo. Les chlorures de fer (FeCl3·6 H2O), de cuivre (CuCl2·2 H2O) et de chrome (CrCl3·6 H2O) sont fournis par Aldrich. L'hydroxyde de baryum Ba(OH)2·8 H2O, pur à 99%, provient de la société Janssen.
Le photocatalyseur est le TiO2 Degussa P-25. Sa structure cristalline est constituée d'anatase (80%) et de rutile (20%). Il présente une surface spécifique de 50 m2/g et une densité de 3,85 g/cm3. Il est non poreux et le diamètre moyen des grains élémentaires est de 30 nm. La largeur de la bande interdite de l'anatase est d'environ 3,2 eV, ce qui correspond à une longueur d'onde d'absorption maximale de 390 nm.
2.2 Photoréacteur
Les études expérimentales sont effectuées dans un réacteur photochimique à immersion en pyrex, semi-ouvert et d'une capacité de 2 l. Il présente plusieurs ouvertures permettant des mesures de la température et du pH, ainsi que l'admission de l'oxygène au cours de la réaction.
La source d'irradiation est une lampe à vapeur de mercure haute pression (HPK-125 W Philips), dont le spectre d'émission présente un maximum à 365,5 nm. La double enveloppe centrale en pyrex qui entoure la lampe laisse passer les radiations dont les longueurs d'onde sont supérieures à 290 nm.
2.3 Méthodes d'analyse
La dégradation photocatalytique du β-naphtol est suivie par chromatographie liquide à haute performance (HPLC) à l'aide d'un chromatographe Shimadzu, couplé à un détecteur UV à longueur d'onde variable (fixée à 280 nm pour la détection du substrat) et d'une pompe isocratique Jasco 880-PU. Une colonne Spherisorb ODS-2 greffée en C-18 (octadécylsilane), fournie par la société Boyer, de longueur 25 cm, de diamètre intérieur 4,6 mm, est utilisée pour la séparation. Le débit d'éluant est maintenu à 0,4 ml/min. La phase mobile est un mélange eau bidistillée/acétonitrile (20%/80%) en volume. Les échantillons prélevés après irradiation sont filtrés à laide de filtres Millipore (taille des pores : 0,45 μm de diamètre), afin d'éliminer les particules solides de TiO2.
La quantité de gaz carbonique dégagée au cours du processus de photominéralisation du β-naphtol est déterminée par une méthode conductimétrique, selon le protocole opératoire préconisé par Chemseddine et al. [18]. Cette technique consiste à entraîner le CO2 formé, par un courant d'oxygène, dans un flacon contenant une solution de 500 ml d'hydroxyde de baryum à 10−2 mol/l. Une cellule conductimétrique, plongeant dans cette solution, permet la mesure de la conductivité à l'aide d'un conductimètre Orion, muni d'une cellule caractérisée par une constante K = 1 cm−1. Avant l'irradiation, un barbotage sous courant d'oxygène est effectué dans le photoréacteur pendant quelques minutes pour évacuer le CO2 résiduel.
2.4 Mode opératoire
Un litre d'une solution de titre connu en β-naphtol (5 × 10−4 mol/l) est introduit dans le photoréacteur, en présence de 1 g/l de TiO2. Cette valeur correspond à la quantité nécessaire à l'absorption totale des photons potentiellement absorbables par le solide [17,19]. La suspension est d'abord agitée pendant 60 min à l'obscurité. Cette période est nécessaire pour atteindre l'équilibre d'adsorption du polluant sur la surface de catalyseur. Ensuite, nous procédons à l'irradiation du mélange réactionnel. Le pH initial de la solution est de 6.
3 Résultats et discussion
3.1 Cinétique de disparition du β-naphtol
Nous avons, dans un premier temps réalisé, la photodégradation du β-naphtol en présence de TiO2 en suspension. Les résultats obtenus sont traduits par les courbes de la Fig. 1. Trois remarques sont à faire :
- • sous irradiation et en l'absence du photocatalyseur, une diminution de la concentration du β-naphtol de l'ordre de 4% est observée (Fig. 1). La photolyse directe est donc négligeable. Le pyrex élimine, en effet, les photons susceptibles d'exciter directement le β-naphtol, dont la longueur d'onde d'absorption maximale se situe à 280 nm ;
- • en présence du dioxyde de titane et à l'obscurité, on note une disparition du β-naphtol dès les premières minutes d'agitation. La concentration tend ensuite à rester constante (4,5 × 10−4 mol/l) après 30 min. Ce phénomène, déjà observé [20–22], est attribué à l'adsorption du β-naphtol sur la surface de TiO2. Cette étape est cruciale pour le déroulement de la réaction de photodégradation ;
- • en présence simultanée de TiO2 et d'UV, l'irradiation du mélange conduit à une destruction totale du β-naphtol dans la solution au bout de 180 min. Ces résultats confirment la nature photocatalytique de la réaction. Les particules de TiO2 sont à l'origine de cette activation. Elles vont absorber les radiations UV pour donner naissance à des espèces très réactives qui conduiront à la dégradation du β-naphtol en solution.

Cinétique de disparition du β-naphtol en présence de TiO2/UV/O2 (photocatalyse) et en absence de catalyseur (photolyse).
Pendant les 60 premières minutes d'irradiation, au cours desquelles 80% du β-naphtol est dégradé, la réaction admet un ordre apparent égal à 1 (Fig. 2), et la cinétique suit l'expression suivante :
| (1) |
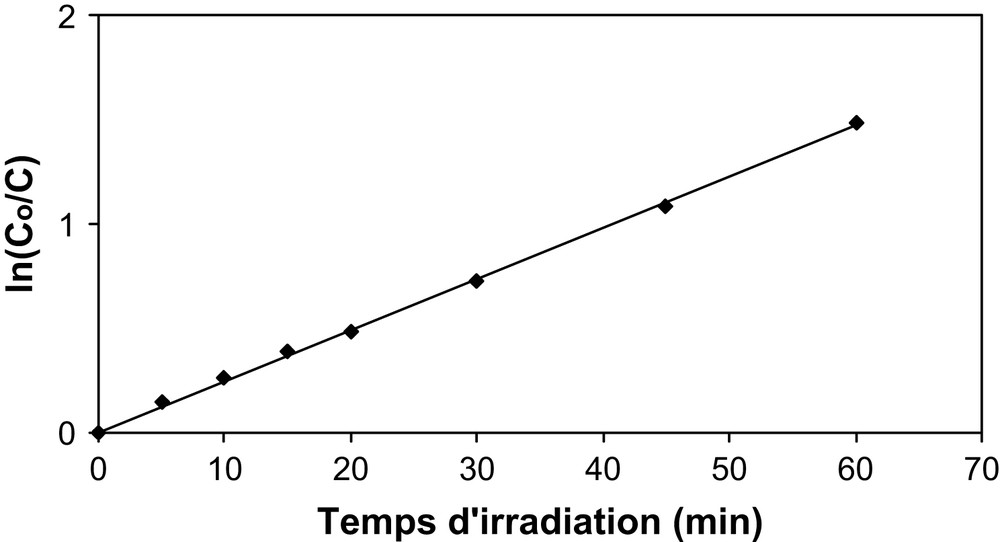
Variation de ln(Co/C) en fonction du temps.
Pour des temps d'irradiation supérieurs à 60 min, nous observons une diminution de la vitesse, qui peut s'expliquer par la concurrence d'adsorption, à la surface de TiO2, entre le polluant et les intermédiaires de dégradation.
En dérivant la relation liant la concentration en β-naphtol au temps d'irradiation, nous obtenons une expression semblable à celle du mécanisme de Langmuir–Hinshelwood (L–H) [19,23–25], où k est la constante de vitesse de la réaction photocatalytique et K la constante d'adsorption du β-naphtol sur le dioxyde de titane :
| (2) |
| (3) |
À faible concentration de β-naphtol, la constante de vitesse apparente déterminée est :
3.2 Minéralisation du carbone
Afin de vérifier la photominéralisation totale du β-naphtol en CO2 et H2O, nous avons suivi la formation du CO2 en fonction du temps. D'après la Fig. 3, on constate que le nombre de moles de CO2 dégagé augmente et atteint un palier au bout de 270 min d'irradiation. La conversion totale du β-naphtol (5 × 10−4 mol/l) aboutit à 5 × 10−3 mol de CO2. La minéralisation de ce polluant est décrite selon l'équation suivante :
| (4) |

Cinétique de formation de CO2 lors de la photominéralisation du β-naphtol.
3.3 Influence de la température
Pour évaluer l'importance de la température dans le domaine étudié, l'irradiation du β-naphtol a été réalisée entre 20 °C et 45 °C. Quelle que soit la température, nous observons une dégradation du polluant (Fig. 4). La vitesse initiale de disparition du β-naphtol augmente légèrement avec l'augmentation de la température.
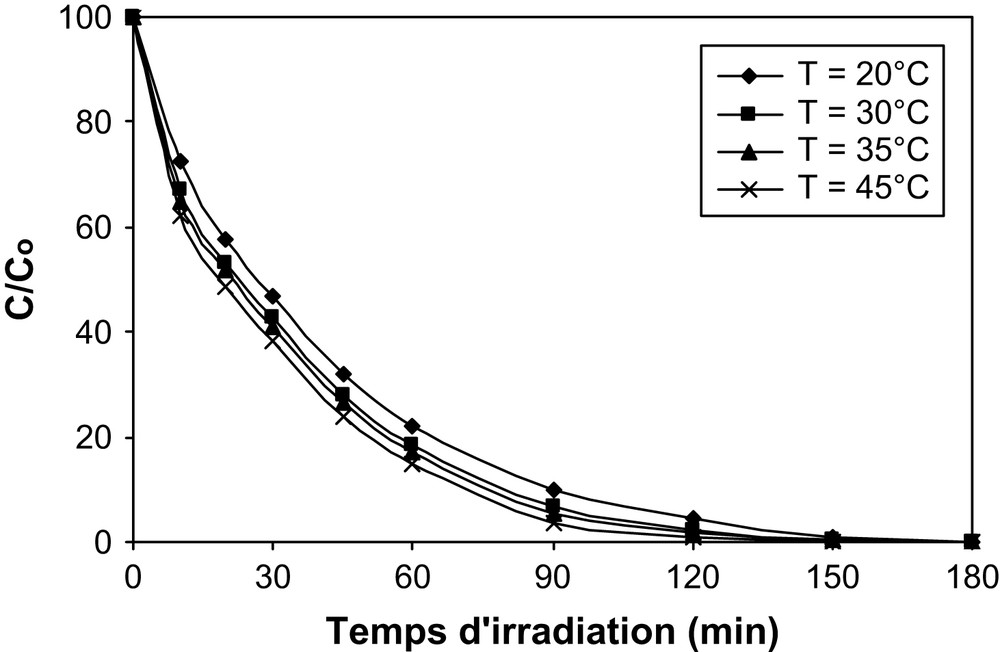
Influence de la température sur la photodégradation du β-naphtol.
La loi d'Arrhenius est définie de la façon suivante :
| (5) |
L'équation (5) donne :
| (6) |
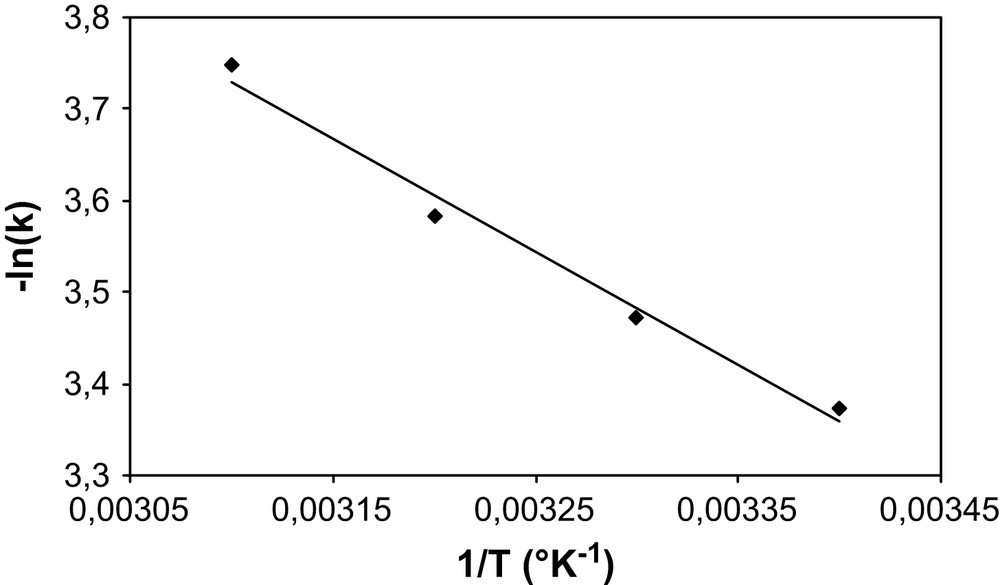
Graphe d'Arrhenius de la constante de vitesse de disparition du β-naphtol.
Cette valeur montre que les étapes d'activation thermique sont négligeables et que, dans le domaine de température étudié, la variation de température influence peu le processus. Le système photocatalytique ne requiert pas de chaleur, car il s'agit d'un processus d'activation photonique. La valeur de cette énergie d'activation est du même ordre de grandeur que celle du 4-chlorophénol [26], du 4-nitrophénol [27] et du phénol [28].
3.4 Influence d'ions en solution
3.4.1 Effets des anions chlorure, sulfate, nitrate et hydrogénocarbonate
Les analyses physicochimiques des eaux ont souvent révélé la présence des ions Cl−, SO42−, NO3− et HCO3−, avec des teneurs dépendant de la nature de l'effluent, ainsi que du site où sont effectués les prélèvements [29].
Pour évaluer l'influence de ces anions, une solution de β-naphtol a été illuminée en présence de sels de sodium dans des conditions opératoires analogues à celles établies précédemment. La concentration varie de 5 × 10−3 mol/l à 10−1 mol/l pour chaque ion.
Les Figs. 6–9 montrent l'effet des ions chlorure, sulfate, hydrogénocarbonate et nitrate sur la photominéralisation du β-naphtol.
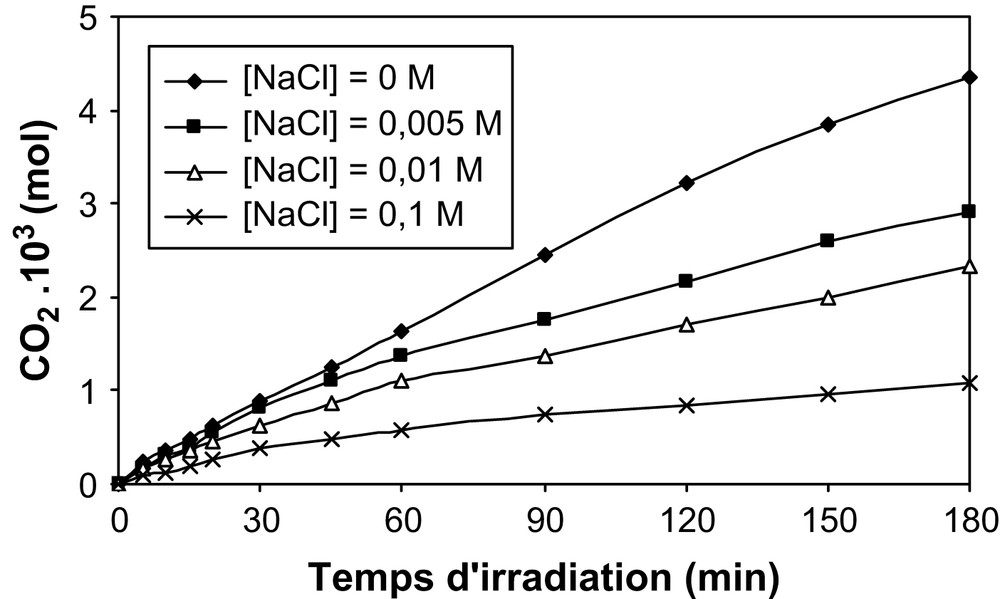
Influence de la concentration en NaCl sur la cinétique de minéralisation du β-naphtol.

Influence de la concentration en Na2SO4 sur la cinétique de minéralisation du β-naphtol.
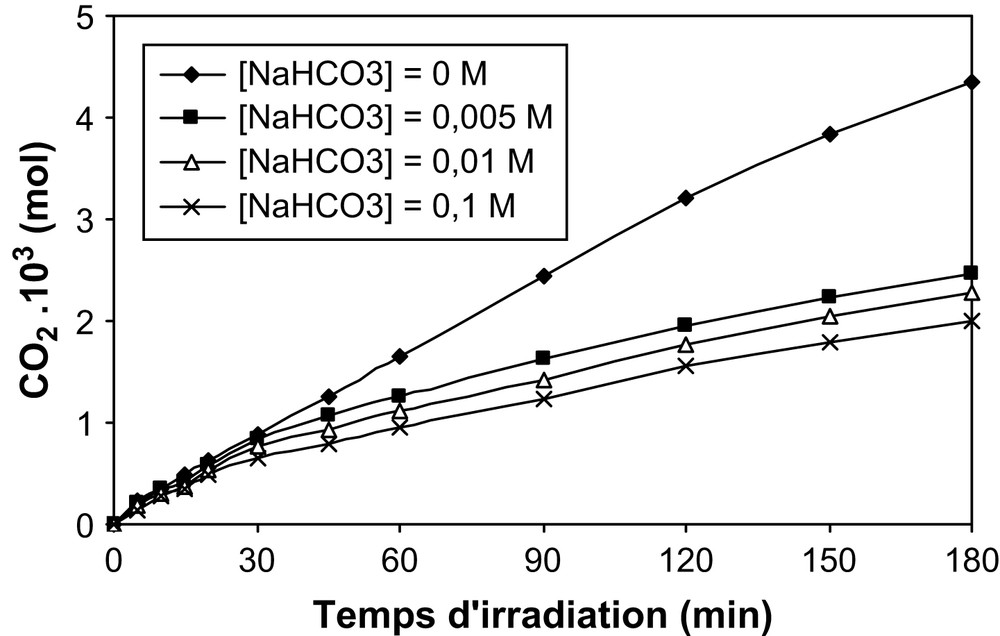
Influence de la concentration en NaHCO3 sur la cinétique de minéralisation du β-naphtol.
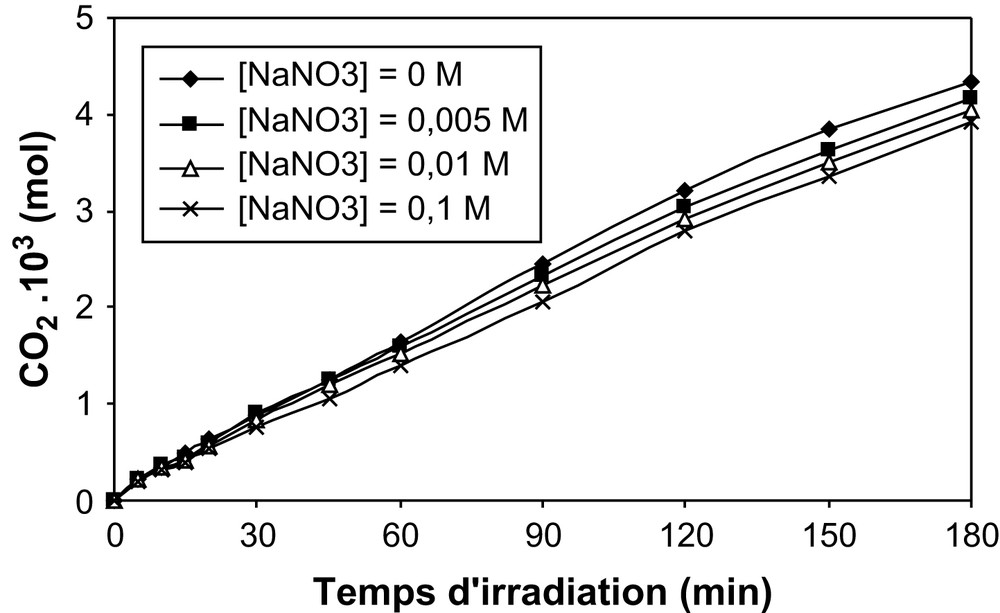
Influence de la concentration en NaNO3 sur la cinétique de minéralisation du β-naphtol.
Il en ressort que la présence des ions précités (chlorures, sulfates et hydrogénocarbonates) inhibe la cinétique de photodégradation du polluant. L'effet inhibiteur croît dans le sens HCO3−, SO42− et Cl− lorsque la concentration de ces ions augmente.
En revanche, les ions nitrate n'ont pratiquement pas d'effet notable sur l'activité photocatalytique, mesurée par la quantité de CO2 formé après 3 h d'irradiation. Ces résultats sont en accord avec ceux trouvés lors de la dégradation des chlorophénols et d'autres polluants organiques [30].
Cependant, selon la nature de l'anion, la minéralisation en CO2 du β-naphtol est de l'ordre de 21%, 28%, 40% et 80% pour une même concentration de 10−1 mol/l, respectivement en présence des ions Cl−, SO42−, HCO3− et NO3−.
L'effet inhibiteur de ces trois premiers ions est peut-être dû à l'adsorption sur les sites actifs du photocatalyseur et/ou à leur compétition avec le polluant pour réagir avec les radicaux générés. Ainsi, pour les chlorures qui inhibent fortement la cinétique de minéralisation, il a été rapporté que ces ions piégent des espèces radicalaires oxydantes, autres que les radicaux hydroxyle [31] :
| (7) |
| (8) |
| (9) |
En revanche, la cinétique de minéralisation est très peu sensible à la concentration en ions nitrate, puisque, selon Lucas Vaz et al. [33], ces ions génèrent des radicaux OH en présence de la lumière solaire selon l'équation suivante :
| (10) |
Les espèces OH ainsi photogénérées réagissent avec le polluant conduisant à sa minéralisation. C'est la raison pour laquelle l'ajustement des pH a été souvent réalisé par addition d'acide nitrique.
3.4.2 Cas des cations métalliques
La présence des cations métalliques est courante dans les eaux naturelles et dans les rejets industriels. Ces ions affectent sensiblement la vitesse et l'efficacité des réactions photocatalytiques. Ainsi, une variation de la vitesse de photodégradation a été observée pour les hydrocarbures aromatiques, les acides benzoïques, les composés phénoliques et d'autres composés organiques en présence d'ions métalliques, essentiellement Cu2+, Fe3+ et Ag+ [34–36].
L'activité catalytique, exprimée en vitesse initiale de formation de CO2, est représentée sur la Fig. 10 en fonction du rapport R = [cation]o/[β-naphtol]o relativement aux trois différents ions (Fe3+, Cu2+ et Cr3+).
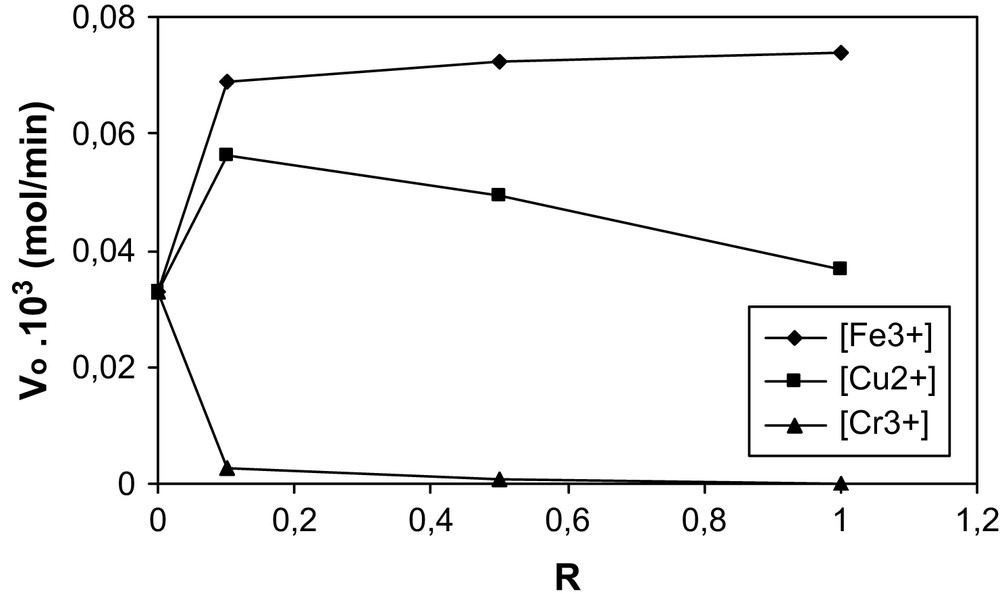
Influence des cations Fe3+, Cu2+ et Cr3+ sur la cinétique de formation de CO2 lors de la photooxydation du β-naphtol.
Pour les ions Cu2+, La vitesse de photominéralisation semble augmenter, pour atteindre un maximum pour R = 0,1, puis diminue au-delà. L'augmentation de la vitesse Vo pourrait être attribuée à un effet catalytique du cation Cu2+ [37]. Pour des concentrations en Cu2+ élevées, deux hypothèses peuvent être avancées. L'inhibition serait attribuée à l'adsorption des ions chlorure et/ou leur interaction avec les radicaux hydroxyle [35]. Selon San et al. [38], il est également probable que les Cu2+ réagiraient avec les photoélectrons, pour conduire à Cu+, lequel interagit avec les OH.
Ce résultat est en accord avec Yang et al. [39], qui ont montré que la photodégradation du phénol par TiO2 en suspension est accélérée par la présence d'ions Cu2+ jusqu'à une concentration de 1 mmol ; au-delà, la cinétique de dégradation est fortement diminuée.
Pour les ions Fe3+, l'augmentation de la vitesse de photodégradation est attribuée à la capacité que possède cet ion à capturer les électrons formés à la surface du catalyseur, inhibant ainsi la recombinaison trou/électron.
Il a été montré que les cations métalliques Fe3+ sont capables d'augmenter la vitesse d'oxydation photocatalytique par des réactions homogènes de type Photo-Fenton, qui produisent également des radicaux hydroxyle OH [40].
| (11) |
3.5 Addition d'éthanol et d'eau oxygénée
Pour mettre en évidence le rôle des radicaux hydroxyle (OH) dans la dégradation du β-naphtol, nous avons réalisé des tests photocatalytiques en présence, d'une part, d'éthanol, composé connu par sa grande affinité vis-à-vis des OH, et, d'autre part, en présence d'eau oxygénée, considérée comme une source génératrice de ces radicaux [41].
3.5.1 Influence de l'éthanol
La Fig. 11 traduit l'évolution de la vitesse initiale de formation de CO2 en fonction d'une quantité d'éthanol représentée en pourcentage volumique. Une chute de 55% de l'activité photocatalytique est observée pour une solution contenant 2% d'éthanol. Au-delà de cette quantité, la vitesse initiale Vo demeure pratiquement constante.

Influence de la teneur en éthanol sur la cinétique de formation de CO2 lors de la photooxydation du β-naphtol.
En tenant compte de la réactivité de l'éthanol avec les radicaux OH, nous pouvons considérer que la disparition du β-naphtol se produit selon un autre chemin réactionnel, faisant intervenir les trous h+ photogénérés à la surface de TiO2. Ceci a été bien observé pour les chlorophénols et les chlorobenzènes [42]. Il est probable qu'un taux de recouvrement maximum de ce substrat est atteint pour une certaine quantité d'éthanol. En conséquence, son augmentation n'a plus d'effet sur la vitesse initiale de minéralisation du β-naphtol.
3.5.2 Influence de l'eau oxygénée H2O2
L'oxydation de composés organiques en solution aqueuse par photolyse du peroxyde d'hydrogène (H2O2/UV) a fait l'objet d'un certain nombre de travaux au cours des dernières années [43].
Certaines études [44] ont montré que la concentration du peroxyde d'hydrogène reste pratiquement constante lors de la minéralisation de l'acide malique. Il y aurait une étape de régénération de cet oxydant, avec formation des acides oxalique et malonique, accompagnée de radicaux hydroperoxyle (HO2), source d'eau oxygénée selon la réaction :
| (12) |
L'influence de la concentration du peroxyde d'hydrogène sur l'activité photocatalytique du TiO2 dans la minéralisation du β-naphtol est étudiée en faisant varier le rapport R = [H2O2]o/[β-naphtol]o, avec [β-naphtol]o = 5 × 10−4 mol/l et [TiO2] = 1 g/l.
La Fig. 12 illustre l'évolution de la cinétique de dégradation du β-naphtol. L'addition de H2O2 en photocatalyse hétérogène accélère la vitesse initiale de disparition du β-naphtol, qui atteint un maximum, pour diminuer lorsque la quantité de H2O2 augmente.
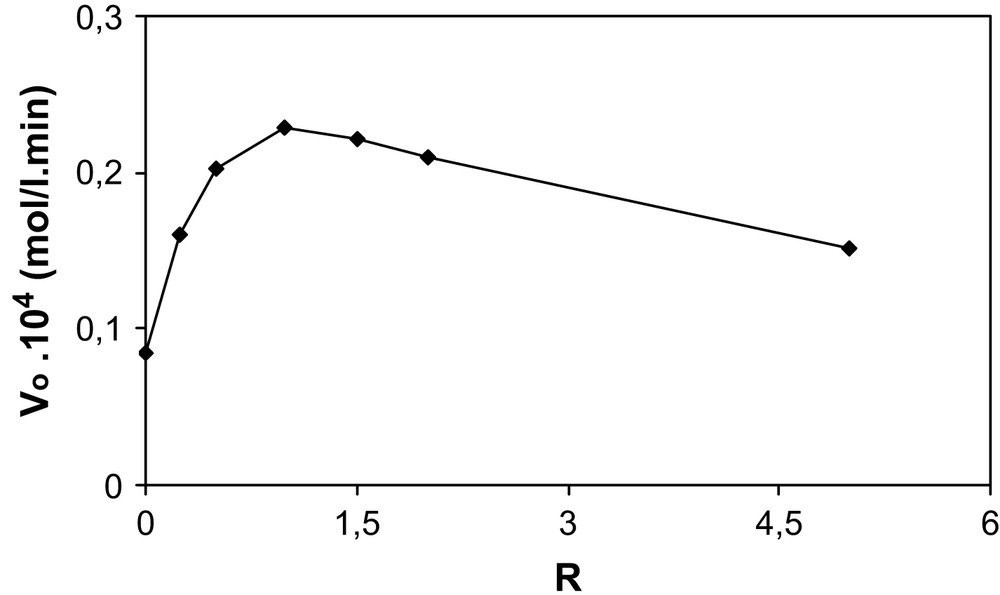
Influence de H2O2 sur la vitesse initiale de disparition du β-naphtol.
Cet accroissement de vitesse peut être attribué à une augmentation de la concentration des radicaux OH à la surface de TiO2.
En revanche, lorsque le rapport molaire R dépasse 1, cette vitesse initiale diminue, la concentration en O2 devenant importante.
Pour de grandes concentrations en peroxyde d'hydrogène, les réactions suivantes se produisent [45,46] :
| (13) |
| (14) |
À partir de ces deux réactions, on voit bien qu'une grande concentration en H2O2 exerce un effet négatif sur la cinétique de photodégradation. En effet, ces deux réactions consomment les radicaux hydroxyle (OH) et hydroperoxyle (HO2) nécessaires à la photodégradation des molécules organiques.
On peut conclure que l'ajout d'un accepteur d'électron permet de réduire le phénomène de recombinaison trou/électron. L'oxydant inorganique le plus étudié pour son effet positif sur la cinétique de photodégradation est le peroxyde d'hydrogène.
4 Conclusions
L'ensemble de ces résultats montre que :
- • la photocatalyse hétérogène est une technique adaptée pour dégrader et minéraliser complètement, à température ambiante, le β-naphtol. L'efficacité du système d'oxydation TiO2/UV/O2 a été mise en évidence ;
- • l'adsorption du micropolluant sur le TiO2 est une étape préalable à sa dégradation ;
- • la cinétique de disparition de ce polluant suit une réaction d'ordre 1 pour les 60 premières minutes d'irradiation. La vitesse initiale semble suivre une cinétique décrite par le modèle de Langmuir–Hinshelwood ;
- • la minéralisation totale du carbone nécessite un temps d'irradiation plus élevé que la disparition totale du polluant ;
- • la vitesse initiale de disparition du β-naphtol est peu affectée par la température ;
- • la présence des anions Cl−, SO42− et HCO3− conduit à une inhibition partielle de la minéralisation du β-naphtol. Ce résultat serait attribué soit à une compétition de réaction du β-naphtol et de l'ion vis-à-vis des radicaux hydroxyle ou autre espèce oxydante, soit à une concurrence d'adsorption du polluant et de ces ions ;
- • l'addition des cations Fe3+ et Cu2+ augmente la cinétique de photominéralisation du polluant, alors que le chrome inhibe totalement la réaction ;
- • le rôle important joué par les OH est confirmé par les résultats obtenus, lorsque la réaction a été réalisée en présence de l'eau oxygénée (source de OH). L'effet inhibiteur de l'éthanol, qui a une certaine affinité vis-à-vis des OH, confirme cette hypothèse.


