1 Introduction
La famille des hétéropolytungstates, incorporant un élément non métallique comme l’arsenic(III), l’antimoine(III) ou le bismuth(III), a fait l’objet de nombreuses études depuis la préparation de [AsW9O33]9– [1]. Ce composé dérive de la structure de Keggin [SiW12O40]4– ; il est formé de trois groupes W3O13 assemblés autour de l’hétéroatome. L’entité AsW9O33 peut jouer le rôle de brique et être assemblée avec divers autres groupes pour construire des espèces plus complexes. Citons par exemple [H2AsW18O60]7– [2], formé de AsW9O33 et de H2W9O33, qui partagent six atomes d’oxygène (X = As, Sb, Bi). Citons [As2W21O69(H2O)]6– [3] formé de deux groupes AsW9O33 assemblés par trois atomes de tungstène. Citons [HnX2W22O76][10–n]– [4–6], formé de deux groupes XW9O33 assemblés par quatre atomes de tungstène (X = Sb, Bi). Citons enfin [As12Ce16(H2O)36W148O524]76– [7], composé dans lequel des fragments AsW9O33 sont assemblés à des fragments W5O18. Cette liste n’est pas exhaustive.
Les composés [Sb2W22O72(OH)4]10– [4], [Bi2W22O70(OH)6]8– [5] et [Bi2W22O74(OH)2]12– [6] ont été préparés et leurs structures déterminées par diffraction des rayons X. Dans ces trois polyanions possédant le même assemblage X2W22O76, deux atomes de tungstène, symétriques par rapport au centre de symétrie du polyanion, sont situés à la périphérie du composé, étant liés au squelette X2W20 par trois atomes d’oxygène. Aussi bien dans le cas de l’antimoine que dans celui du bismuth, cette situation particulière explique la substitution de cet atome de tungstène dit externe par un cation métallique de la première série des métaux de transition. On peut citer comme exemple [Sb2W20M2O70(H2O)6]10– avec M = Mn2+,Fe3+,Co2+,Ni2+, [Bi2W20M2O70(H2O)6]10– avec M = Fe2+, Co2+, Ni2+, Zn2+ [1–3]. La disposition et les longueurs de liaison tungstène–oxygène suggèrent qu’un atome d’antimoine puisse aussi se fixer à cet endroit. Une synthèse tentée avec les proportions correspondantes d’antimoine et de tungstène (W/Sb = 5 en atomes) conduit à des cristaux aciculaires (composés 1 et 2). L’étude cristallographique amène à la conclusion que l’un des deux atomes de tungstène externe manque, le squelette métallique étant ainsi Sb2W21. La synthèse effectuée dans les mêmes conditions avec du nitrate de bismuth pentahydraté conduit au composé 3 isomorphe du composé 1, comme la résolution de structure le montre. Par ailleurs, un essai de synthèse du composé lacunaire SbW17 en présence de lithium conduit en réalité au composé 4, dont le squelette est Sb2W22 ; ceci permet de comparer le comportement du facteur de température de l’atome de tungstène externe en fonction du taux d’occupation, discussion sur laquelle se fonde la conclusion de l’existence d’un composé de squelette Sb2W21. Enfin, un essai de synthèse du composé à squelette SbW17Ni, dans lequel la substitution de certains atomes d’oxygène par du fluor avait été tentée, donne naissance entre autres choses au composé 5 vert pâle, dans lequel les deux sites externes sont occupés statistiquement par du tungstène et du nickel en proportion 1/1 en atomes, ce qui correspond à un squelette Sb2W21Ni.
2 Synthèses
2.1 Composé 1
42,0 mmol de Na2WO4·2 H2O sont dissoutes dans 100 cm3 d’eau. 4,2 mmol de Sb2O3 sont dissoutes dans 2 cm3 de HCl concentré (W/Sb en atomes = 5). La seconde solution est ajoutée goutte à goutte, sous agitation, à la précédente. À chaque addition apparaît un précipité blanc, qui se redissout rapidement. Le pH, égal à 9,9 en fin d’addition, est amené à 4 avec de l’acide acétique pur. Au bout de quelques jours, des cristaux aciculaires se forment. On trouve également des cristaux prismatiques correspondant à [H2W12O42]10–. Une séparation manuelle parfaite des cristaux s’avère infructueuse. De ce fait, les résultats analytiques sont peu utilisables.
2.2 Composé 2
La même synthèse réalisée avec HCl concentré au lieu de CH3COOH pur conduit au composé 2.
2.3 Composé 3
Une synthèse similaire pratiquée en remplaçant Sb2O3 par Bi(NO3)3·5 H2O (W/Bi en atomes = 5,3) et en acidifiant avec HCl concentré conduit au composé 3.
2.4 Composé 4
56,3 mmol de Na2WO4·2 H2O sont dissoutes dans 50 cm3 d’eau. 1,8 mmol de Sb2O3 sont dissoutes dans 2 cm3 de HCl concentré (W/Sb en atomes = 15,6). Cette solution est ajoutée goutte à goutte à la précédente, sous agitation. Le pH est ensuite amené à 4,7 avec HCl concentré. 3,6 mmol de LiCl sont dissoutes dans 5 cm3 d’eau, puis ajoutées à la solution précédente. Le pH est abaissé à 3,5 avec CH3COOH pur. Des cristaux aciculaires se forment au bout de quelques jours en même temps que des cristaux prismatiques de [H2W12O42]10–. Le même problème analytique se pose.
2.5 Composé 5
Un essai de substitution des groupes OH par F dans [SbW17NiO56(OH)3(H2O)]8– n’a pas donné le composé espéré, dans lequel des atomes de fluor auraient remplacé des atomes d’oxygène. 50,5 mmol de Na2WO4·2 H2O et 8,9 mmol de NaF sont dissoutes dans 50 cm3 d’eau. 1,5 mmol de Sb2O3 sont dissoutes dans 2 cm3 de HCl concentré (W/Sb en atomes = 14,8). Après mélange de ces deux solutions, le pH est amené à 6 avec HCl concentré. 2,97 mmol de NiCl2·6 H2O sont dissoutes dans 5 cm3 d’eau (W/Ni en atomes = 17,0). Après mélange, le pH est amené à 5,10 avec CH3COOH pur. La solution est jaune–vert. Au bout de quelques jours, à côté de cristaux de [H2W12O42]10–, il se forme des cristaux vert pâle aciculaires.
3 Études cristallographiques
Les cristaux ont été montés sur un diffractomètre Nonius-CAD4. Les données ont été enregistrées à température ambiante avec le rayonnement du molybdène. Les paramètres, déterminés par moindres carrés à partir de 25 réflexions, sont rassemblés dans le Tableau 1, ainsi que les principales caractéristiques de résolution de structure. Les atomes de tungstène et d’antimoine ont été localisés par méthode directe (SHELXS). L’absorption a été corrigée par la méthode DIFABS. La matrice des équations normales a été inversée en un seul bloc. Dans l’affinement final, les atomes de tungstène et d’antimoine ont été traités avec un facteur de température anisotrope, les autres atomes avec un facteur de température isotrope. Les calculs ont été effectués avec la chaîne CRYSTALS [8].
Données cristallographiques concernant les composés Na8[H6Sb2W21O73]·16,5 H2O (1), Na8[H6Sb2W21O73]·19 H2O (2), Na8[H6Bi2W21O73]·16,5 H2O (3), Li2Na6[H6Sb2W22O76]·14,5 H2O (4) et Na5[H7Sb2NiW21O73(H2O)3]·20 H2O (5)
| Composé 1 | Composé 2 | Composé 3 | Composé 4 | Composé 5 | |
| a | 12,382(6) | 13,083(2) | 12,354(7) | 34,01(2) | 12,879(3) |
| b | 13,062(7) | 13,393(4) | 13,066(7) | 26,04(1) | 25,169(4) |
| c | 17,031(2) | 17,115(3) | 16,956(9) | 12,97(2) | 16,082(3) |
| α | 108,78(3) | 110,02(2) | 108,86(4) | — | — |
| β | 95,51(2) | 99,46(1) | 95,59(5) | 92,3(1) | 94,95(2) |
| γ | 106,56(4) | 112,05(2) | 106,36(5) | — | — |
| V | 2445(2) | 2609(1) | 2435(3) | 11483(19) | 5194(1) |
| Groupe d’espace | P | P | P | C2/c | P21/n |
| Nombre de réflexions enregistrées | 7647 | 12 580 | 8076 | 10 094 | 8142 |
| Nombre de réflexions utilisées | 5088 | 9107 | 7594 | 6229 | 5544 |
| R | 5,39 | 6,21 | 9,63 | 7,65 | 6,96 |
| Rw | 6,02 | 7,22 | 11,28 | 9,38 | 7,90 |
4 Discussion
Les cinq composés sont centrosymétriques ; l’unité asymétrique du type XW11 correspond à un demi polyanion. Les onze atomes de tungstène se répartissent entre un groupe XW9 de type βB et les deux atomes qui assurent la liaison entre deux groupes SbW9 reliés par le centre de symétrie. Dans le groupe XW9, l’un des trois atomes de tungstène du groupe tourné de 60° n’est lié qu’à trois atomes d’oxygène du polyanion, en position faciale sur l’octaèdre WO6 entourant cet atome de tungstène externe ; l’octaèdre est complété par trois atomes d’oxygène terminaux.
La résolution de la structure du composé 1 conduit à quatre atomes de sodium pour un groupe SbW11O38. Un affinement effectué avec des facteurs de température isotropes donne R = 8,21 et Rw = 9,10 si le taux d’occupation de l’atome de tungstène externe est fixé à 0,5 ; son facteur de température est égal à 0,032, alors que la moyenne des facteurs des dix autres atomes de tungstène est égale à 0,029. Si le taux d’occupation est fixé à 1,0, R monte à 9,80 et Rw à 10,79 ; le facteur de température passe à 0,088 pour une moyenne des dix autres facteurs égale à 0,027. Cette comparaison suggère que le site de cet atome externe est occupé à 50%. De la même façon, les trois atomes d’oxygène terminaux liés à cet atome externe ont des facteurs de température isotropes égaux à 0,034 0,037 0,054 pour une occupation 0,5 de leurs sites alors que ces valeurs sont 0,131 0,165 0,192 pour une occupation 1. La moyenne des facteurs de température pour les 35 autres atomes d’oxygène du demi-polyanion est égale à 0,039. On en conclut que ces trois sites sont également occupés à 50% (Fig. 1). La présence de quatre atomes de sodium par unité asymétrique conduit à la formule Na8[H6Sb2W21O73]·16,5 H2O. Les études cristallographiques complètes faites sur deux cristaux tirés de deux synthèses indépendantes a donné le même résultat.
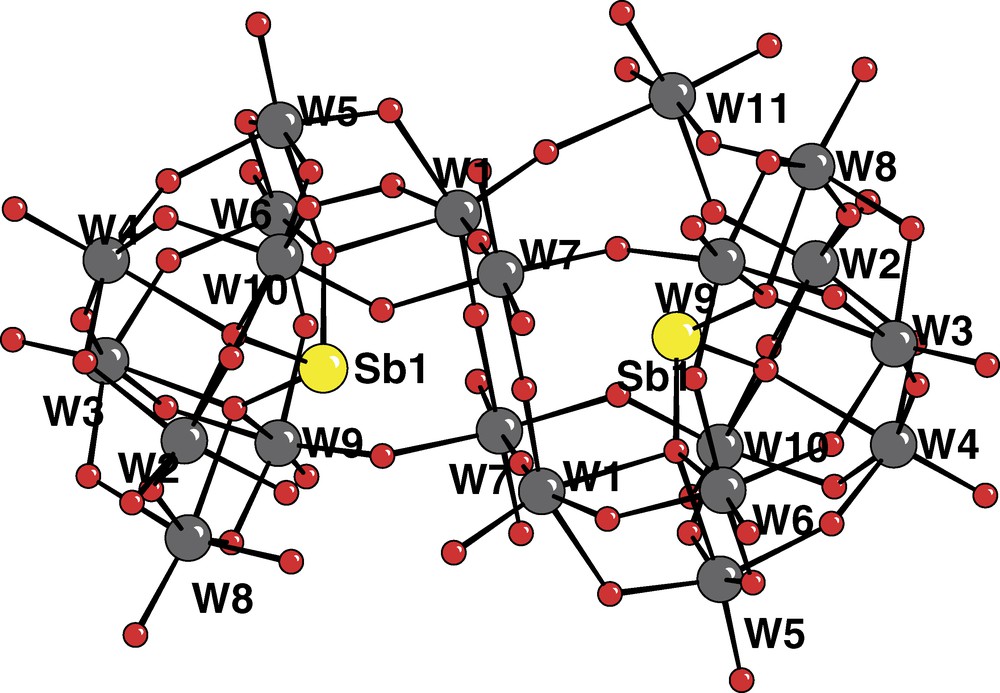
Représentation de l’assemblage lacunaire Sb2W21O73. Le grand cercle gris clair schématise l’antimoine et les grands cercles gris foncé le tungstène.
Le composé 3 qui contient du bismuth(III) au lieu d’antimoine(III), est isomorphe du composé 1. Les caractéristiques d’affinement décrites ci-dessus se retrouvent intégralement pour ce composé 3. Il est bon de noter que les paramètres cristallographiques ne sont ni ceux de Na8[Bi2W22O70(OH)6]·31 H2O, dont la maille est monoclinique (C2/c) : a = 33,892(5), b = 26,013(5), c = 12,990(7) Å, β = 92,03(3)° [2], ni ceux de Na12[Bi2W22O74(H2O)2]·44 H2O dont la maille est monoclinique (P21/n) : a = 12,993(5), b = 25,389(5), c = 16,279(3) Å, β = 98,36(3)° [3].
L’étude de la structure du composé 4 conforte cette interprétation. La maille monoclinique renferme quatre molécules, dont le squelette correspond à celui du composé Sb2W22. Il est identique à ceux de [H4Sb2W22O76]10–, de [H2Bi2W22O76]12– et de [H6Bi2W22O76]8– rappelés ci-dessus [1–3]. Si les onze atomes de tungstène du motif asymétrique Sb2W11O38 sont mis en occupation 1, le facteur de température isotrope de l’atome de tungstène externe est égal à 0,044, alors que le facteur moyen des dix autres atomes de tungstène est égal à 0,025 avec R = 8,34 et Rw = 9,99. Si maintenant le site de l’atome externe est affecté d’un taux d’occupation 0,5, R monte à 9,18 et Rw à 10,91 tandis que le facteur de température est égal à 0,001 avec une moyenne de 0,027 pour les dix autres atomes métalliques. Les facteurs de température des trois atomes d’oxygène terminaux liés à cet atome externe varient de la même façon, étant 0,044, 0,066, 0,070 en occupation 1 et –0,004, 0,008, 0,016 en occupation 0,5 avec une moyenne de 0,035 pour les autres atomes d’oxygène du polyanion. Ces sites sont donc totalement occupés. Cette relation particulière entre les valeurs des facteurs de température isotropes et les taux d’occupation, comparées à celles trouvées pour le composé 1, établit la validité des taux d’occupation égaux à 0,5 dans 1 et 3. L’étude structurale de 4 révèle quatre sites cationiques par groupe SbW11O38 dont deux sont occupés statistiquement par du lithium et du sodium dans le rapport 1:1 (voir synthèse). En effet, si le taux d’occupation 1 en sodium est affecté aux quatre sites cationiques, les facteurs de température isotropes sont 0,049, 0,051, 0,093 et 0,096 (R = 8,36). Si deux sites sont partagés à raison de 50% par le sodium et 50% par le lithium, les facteurs isotropes sont 0,048, 0,051, 0,043 et 0,045 (R = 8,34). Si ces deux sites sont occupés à 100% par le lithium, les facteurs isotropes sont 0,048, 0,050, –0,035, –0,032 (R = 8,43). La formule du composé 4 s’écrit Li2Na6[H6Sb2W22O76]·14,5 H2O.
Le composé 2 possède une maille qui diffère légèrement de celle du composé 1. Il est également du type Sb2W21. Une occupation 0,5 du site de l’atome de tungstène externe conduit à R = 6,97 et Rw = 7,88 ; le facteur de température isotrope est de 0,017 pour une moyenne de 0,017 avec les dix autres atomes de tungstène. Si l’occupation est 1,0, on trouve R = 8,41 et Rw = 9,47, avec un facteur de température de 0,062. Cette différence est significative et amène à choisir une occupation 0,5 pour ce site externe. Comme pour les précédents composés, il y a quatre sites cationiques par motif asymétrique, d’où la formule Na8[H6Sb2W21O73]·19 H2O (Fig. 1). Dans le cristal, les sites cristallographiques de deux atomes de tungstène externes de deux hétéropolyanions voisins sont distants de 3,48 Å. Ils sont reliés par un centre de symétrie. Les trois atomes d’oxygène externes auxquels chacun de ces atomes de tungstène est chimiquement lié sont liés deux à deux par le centre de symétrie. L’un de ces trois sites oxygène est distant de son symétrique de 1,38 Å. Cette distance, trop courte pour être un contact oxygène–oxygène, s’explique par une occupation statistique de 0,5, ce qui constitue un nouvel argument en faveur de la structure lacunaire Sb2W21. Trois synthèses successives et trois études cristallographiques complètes indépendantes ont conduit au même résultat.
Les cristaux vert clair du composé 5 sont caractérisés par une maille monoclinique qui contient quatre polyanions, dont le squelette est du type Sb2W22. Le première remarque est que les paramètres cristallographiques ne correspondent pas à ceux de Na10[Bi2Ni2W20O70(H2O)6], qui sont a = 12,565(9), b = 26,499(6), c = 12,767(5)Å, β = 92,26(5)°, P21/n [2]. L’examen par spectrométrie d’absorption UV–visible d’une solution aqueuse obtenue par redissolution de quelques cristaux vert pâle montre un spectre caractéristique de NiII avec deux bandes à 700 et 766 nm. La résolution de structure et l’examen du site occupé par l’atome de tungstène externe donnent les résultats suivants. S’il est totalement occupé par du tungstène, R = 7,90 et Rw = 9,09, avec un facteur isotrope de 0,076, alors que le facteur moyen des dix autres atomes de tungstène est égal à 0,027. Si le site est totalement occupé par du nickel, R = 7,65 et Rw = 8,69 avec un facteur isotrope égal à -0,008. Si maintenant le site est occupé statistiquement par 50% de tungstène et 50% de nickel, R = 7,04 et Rw = 7,98, avec un facteur isotrope de 0,030. 2,5 cations sodium sont trouvés par motif asymétrique. La formule s’écrit Na5[H7Sb2NiW20O73(H2O)3]·20 H2O. Soulignons que la maille observée pour ce composé 5 correspond à celle décrite par Krebs et al. [3] pour Na10[Bi2Ni2W20O70(H2O)6]·41 H2O.
On pourrait penser que la composition Sb2W21 résulte d’une solution solide Sb2W22–Sb2W20. En fait, toutes les tentatives faites pour obtenir le composé doublement lacunaire de squelette Sb2W20 ont échoué. Elles aboutissent invariablement à Sb2W21. On peut de plus comprendre que les formes et donc les volumes occupés par les polyanions Sb2W20 et Sb2W22 sont suffisamment différents pour empêcher une solution solide de proportion 50:50.
5 Conclusion
Cette étude cristallographique de cinq composés de formule Na8[H6Sb2W21O73]·16,5 H2O, Na8[H6Sb2W21O73]·19 H2O, Na8[H6Bi2W21O73]·16,5 H2O, Li2Na6[H6Sb2W22O76]·14,5 H2O et Na5[H7Sb2NiW21O73(H2O)3]·20 H2O amène à la conclusion que le polyanion lacunaire répondant à l’assemblage X2W21O73, avec X = Sb,Bi, existe. Il dérive de l’assemblage X2W22O76 par perte de l’un des deux atomes de tungstène externes.


