1 Abridged English version
The ancientness of a forest refers to the time that has passed since forest was established and is independent of past and current management. “Ancient” (ancien in French) and “recent” (récent) refer to the differences between a forest area that has been continuously wooded from a given date and a forest that was established on agricultural land after this date. This reference date is often related to the first countrywide detailed mapping of land use in the country. In France, the reference map layer that separates ancient forests from recent forests is the “État-Major” map, dating from the middle of the 19th century. No detailed analysis of the share of ancient forest is available yet, as the reference map data are still being digitised. The only available estimate for France is based on Cassini's map, which is basically insufficiently accurate for this purpose (scale, precision of forest limits, deforestation occurred after this date). A recent analysis states the share of ancient forest at 29 % of the French forested area.
Because of the variable ability of species to recolonize deforested areas, ancientness results in significant differences in biodiversity between the two forest types. The presence today of some forest species of plants and fungi and of some coleoptera depends on ancientness. Similarly, deforestation for agriculture impacts soil parameters. In the short term, transformation into arable land leads to a loss of 50 to 75 % of microbial biomass, a reduction in the quantity of mineralisable nitrogen and an increase in net nitrification. In the long term, the shallow horizons of recent forest will contain less carbon, more nitrogen and phosphorus, and have a higher C:N ratio than ancient forest. The ecological consequences of deforestation are highly persistent, as their effects are still noticeable more than 2000 years after deforestation.
Based on the French history and on scientific knowledge about the ecological impact of ancientness, we propose to use the term “ancient millennial forest” (forêt ancienne millénaire), which is already known, to describe a forest that has not been deforested since the last glaciation. We propose two new terms “ancient Gallo-Roman forest” (forêt ancienne gallo-romaine) and “ancient medieval forest” (forêt ancienne médiévale) to describe an area that has been continuously wooded since Roman time and since the middle age, respectively.“Maturity” is another ecological quality that refers to the stage of natural developmental of a forest stand. High maturity is evidenced by specific attributes: many large or old living trees, a high volume of coarse woody debris in different states of decomposition and many types of tree microhabitats on living trees. These features are commonly found in forest stands that have surpassed the first half of their natural life cycle. In regularly managed forests that are usually harvested no later than after the first third of the natural cycle, these features are often very rare. Less than 3 % of the French even-age forest is older than the harvesting age (Indicator 4.3, MCPFE).
A large proportion of biodiversity depends on maturity attributes: more than 25 % of forest species depend on dead wood and microhabitats in living trees. Removing woody material from the ecosystem through intensive harvest may also lead to imbalanced biogeochemical cycles and distinctively lower above- and belowground carbon stocks.
Maturity is not the only attribute that has to be studied to assess the level of naturalness of a forest: an old stand of pioneer stage of forest succession has totally different biodiversity than a stand dominated by shade-tolerant species and all phases of the silvigenesis. Dynamics is a quality of the ecosystem that reveals the causes, mechanisms, and processes responsible for spontaneous and/or anthropic changes in composition. This quality depends to a great extent on climate, and on the conditions at the site concerned and includes three aspects: succession, silvigenetic cycle and disturbance. Forests at the higher maturity stage with vegetation at its natural dynamic equilibrium are called “old-growth forest” (forêts subnaturelles in French). There is no available data over the French area that could be considered as old-growth forest.
The quality of ancientness and maturity are defined at different scales. The impact of human activity on ancientness is distinct, as it involves a change in land use, whereas for maturity, this impact is more differentiated and progressive, as the ecosystem remains the forest. Ancientness is related to a location, a parcel of land, whereas maturity describes the trees, the forest stand. The time scale for maturity relates to the natural lifespan of the dominant tree species (i.e. for decades to millennia), whereas the time scale of ancientness is absolute, and may range from decades to several millennia. A forest can be ancient with a high maturity's degree (for example, old growth forest), ancient with a low degree of maturity (for example, cultivated ancient forest) or recent with a high maturity's degree (for example, an old birch forest).
Ancientness and maturity have some process and mechanisms in common. In both cases, the removal of all, or part, of the woody material leads to changes in biochemical cycles and soil parameters. The limited ability of the species to recolonize the land after a disturbance that removes the resources can explain the differences in biodiversity between ancient and recent forests, but also between stands with high and low degrees of maturity.
To better understand and evaluate the value of a forest ecosystem, all its qualities need to be taken into account, starting with ancientness, maturity, and stand dynamic profile.
2 Introduction
Dans les régions tempérées, la forêt devrait naturellement recouvrir la plus grande partie du territoire depuis le début de l’Holocène [1]. Or, l’homme a modifié la répartition, la naturalité et la dynamique des écosystèmes en fonction de ses besoins pour l’agriculture, l’élevage ou l’urbanisation. Le fonctionnement naturel des forêts lui-même est modifié par une extraction de biomasse, un raccourcissement souvent drastique du cycle de vie des peuplements, une modification de la composition dendrologique, etc. En France métropolitaine, 30 % du territoire est actuellement boisé et 79 % des forêts présentent une structure régulière et sont âgées de moins de 100 ans [2]. Ces changements ont des conséquences évidentes sur l’écosystème, en termes de structure, de biodiversité et de fonctionnement [3].
Différentes qualités de l’écosystème permettent de comprendre le fonctionnement général de l’écosystème forestier et d’évaluer son état de conservation. Parmi celles-ci, l’ancienneté et la maturité sont souvent confondues car, dans la langue française non appliquée à l’écosystème forestier, ces deux termes sont particulièrement proches, tous deux étant liés à des notions de durée, de temporalité. Appliqués à la forêt, l’écologie forestière a montré ces dernières années qu’ils sont bien distincts :
- • l’ancienneté de l’état boisé fait référence au temps de présence d’un écosystème forestier sans interruption (continuité temporelle d’un sol boisé) ;
- • la maturité du peuplement vivant traduit l’avancement du développement biologique du peuplement d’arbres qui composent la strate arborescente dominante.
La traduction française des termes employés dans la littérature internationale varie parfois en fonction des sources et manque de précision (dans la littérature internationale, ces deux concepts, également nouveaux, montrent la même hésitation terminologique). Pour mieux comprendre le rôle écologique de chacune de ces qualités et leurs synergies, mais également faciliter le dialogue entre les gestionnaires forestiers et les écologues, il nous apparaît aujourd’hui important de définir et distinguer ces deux qualités et de proposer un vocabulaire clair, non ambigu et fondé sur les concepts de ces deux qualités. Une troisième qualité de l’écosystème, la dynamique, sera définie pour permettre de décrire l’évolution naturelle d’un peuplement, ainsi que l’état de forêt subnaturelle.
Outre, la terminologie et les différences de point de vue, cette réflexion sémantique suscite de nombreuses questions nouvelles de recherches. Comment définir ancienneté et maturité de façon scientifique ? Ces qualités écologiques sont-elles construites de façon assez précise au vu des connaissances actuelles, ou peut-on proposer des améliorations ? Quelles sont les composantes, synergies et limites de chacune de ces qualités des écosystèmes, leurs répercussions fonctionnelles et en termes de biodiversité ? Quelle est la part aujourd’hui de forêts, en France et dans le monde, concernées par un degré élevé d’ancienneté et de maturité ? Quels sont les enjeux liés à ces deux qualités, par exemple pour la conservation de la biodiversité, la compréhension de la productivité de l’écosystème ou l’adaptation aux changements climatiques ? Cet article est structuré en réponse à ces différentes questions.
2.1 État de l’art sur les qualités de maturité et d’ancienneté, terminologie associée
2.1.1 Ancienneté
L’ancienneté d’une forêt est la durée sans interruption de l’état boisé en un lieu. Cette qualité est indépendante de la gestion forestière passée et actuelle ayant modifié le peuplement [4]. Elle implique que le fonctionnement forestier, du peuplement comme du sol, n’a pas été interrompu durant cette période, par exemple par un défrichement et une mise en culture (labour), ces actions ayant un fort impact à long terme sur le fonctionnement de l’écosystème forestier. Ce terme correspond au terme anglo-saxon ancientness [5–9].
Aujourd’hui, cette continuité de l’état boisé est évaluée le plus souvent de façon binaire (ancien/récent), grâce aux documents d’archives disponibles (cartes de Cassini, d’État-Major, documents d’aménagement…). Les qualificatifs « ancien » et « récent » sont attribués respectivement pour distinguer une zone boisée en continu depuis une date clé [7] ou bien une forêt qui s’est constituée depuis cette date. Cette approche binaire est une simplification. Le choix de cette date est particulièrement important et doit être établi de façon raisonnée, fondé à la fois sur l’histoire et l’écologie de la région.
En France, c’est le minimum forestier du milieu du XIXe siècle qui sert généralement de référence [4,10–12] pour séparer les forêts anciennes des forêts récentes. Deux raisons justifient cette date [13] :
- • c’est la période historique où la surface boisée était à son minimum sur la plus grande partie du territoire français. Les forêts présentes à cette date ont donc une forte probabilité d’avoir persisté sur une période plus longue que seules les archives historiques ou l’archéologie peuvent confirmer ;
- • les archives et les cartes, notamment les cartes d’État-Major, permettent une spatialisation précise des boisements de l’époque.
Les recherches prenant cette date comme référence montrent des résultats très significatifs, notamment en ce qui concerne la preuve d’impact de l’ancienneté sur la diversité floristique [4,7].
Il n’existe pas, à l’heure actuelle, de chiffre estimant la surface française de forêt ancienne à partir des minutes des feuilles de la carte de l’État-Major (1:40 000). Le travail de digitalisation à l’échelle nationale (et les statistiques qui en découlent) est en cours [12]. Or, ces dernières sont celles qui doivent faire référence pour déterminer si une forêt est ancienne, car :
- • elles couvrent l’ensemble du territoire, Corse comprise ;
- • elles sont les plus proches de la date du minimum forestier, autour de 1850, et ;
- • elles sont beaucoup plus précises que les cartes de Cassini [12].
Le seul ordre de grandeur disponible, au niveau national, résulte aujourd’hui de l’étude des cartes de Cassini : 29 % des forêts du territoire français de l’époque (hors Corse et comté de Savoie) sont anciennes [11].
Dans les autres pays européens, le caractère ancien d’une forêt est déterminé à partir du document le plus ancien disponible à l’échelle nationale. Cette information diffère en date et précision pour chaque pays, ce qui explique que la date utilisée pour délimiter une forêt ancienne soit 1600 en Angleterre et au Pays de Galles, 1750 en Écosse [6], 1775 en Belgique (carte de Ferraris) [7,14], et 1850 en Hollande [15]. Ceci amène à 23 % de forêts anciennes au Royaume-Uni [6] et 16 % dans les Flandres belges [7].
Les surfaces forestières considérées comme anciennes varient donc sensiblement d’un pays à l’autre et en fonction du seuil d’ancienneté choisi, mais concernent entre 15 et 30 % des forêts dans les pays étudiés.
2.1.2 Maturité du peuplement
La maturité d’un peuplement est le degré d’avancement du développement biologique des arbres qui le composent. Le gradient de maturité suit donc les étapes clés du processus de leur développement (germination, installation, grossissement, vieillissement, sénescence, puis mort). Dans les peuplements en évolution naturelle, au fur et à mesure du développement biologique des arbres qui composent le peuplement, on observe que :
- • l’âge des arbres augmente ; c’est un indicateur simple du développement biologique ou de l’espérance de vie du peuplement vivant (dépendant de la longévité variable des essences qui le composent) ;
- • les arbres grossissent : leur diamètre est un indicateur indirect du développement biologique, même si l’accroissement en diamètre de l’essence dépend de la fertilité de la station forestière et du degré de concurrence pour la lumière avec les arbres voisins. Notons que la croissance est bien différente du développement, mais elle peut en permettre une approximation ;
- • les arbres portent de plus en plus de dendro-microhabitats (en particulier les cavités et les fentes) sur le tronc et les branches, car certaines parties de l’arbre se nécrosent, à cause de paramètres biotiques (par exemple, insectes, champignons, pics) ou abiotiques (par exemple, chutes de blocs ou d’arbres voisins, foudre). Certains dendro-microhabitats apparaissent préférentiellement sur des arbres de gros diamètres, de façon variable suivant les essences : les sporophores de champignons saproxyliques et les fentes chez le hêtre, et les fentes, cavités vides, puis cavités à terreau chez le sapin [16]. Ces dendro-microhabitats peuvent être considérés comme indicateurs de développement biologique du peuplement.
À l’échelle du peuplement, on observe également une augmentation de la quantité et de la diversité du bois mort. La présence de très gros arbres, d’une diversité de certains dendro-microhabitats abondants et d’une grande quantité de bois mort sous plusieurs formes sont ainsi des attributs structurels directement liés à l’augmentation de la maturité du peuplement.
Des relations non linéaires existent entre ces attributs et l’âge du peuplement ; et un seuil d’abondance des attributs de maturité est observé dans des peuplements en évolution naturelle ayant dépassé la moitié de la longévité de l’essence [17–19]. En forêt exploitée, ces relations ne sont pas toujours vérifiées, car l’application d’un diamètre d’exploitabilité souvent très faible par rapport au potentiel de croissance de l’essence et le martelage visant à préserver la qualité technologique des bois réduisent l’occurrence de l’ensemble des attributs [20,21]. A contrario, des pratiques d’élagage et de taillis particulières peuvent provoquer l’apparition de nombreux dendro-microhabitats sur des arbres encore jeunes [22].
En France, 3 % de la surface des futaies régulières peut être considérée comme ayant dépassé l’âge d’exploitabilité [23]. L’institut forestier national (IFN) stipule que ce chiffre est à considérer avec beaucoup de précautions, car les protocoles d’évaluation sont encore en cours d’amélioration, les âges seuils par essence ont été fixés à dire d’expert sur des critères d’exploitation (et non écologiques) et aucune caractéristique stationnelle n’a été prise en compte pour l’évaluation (indicateur 4.3.1, [23]). Notons d’ailleurs que les essences représentant la plus grande proportion de peuplements à maturité élevée sont le bouleau, le tremble et les aulnes, considérés comme « âgés » à partir de seulement 50 et 70 ans. Par conséquent, le protocole d’inventaire des peuplements ayant dépassé la moitié de leur longévité gagnerait donc à être affiné et ce chiffre de 3 % est à considérer comme un maximum [23]. Ce chiffre n’est basé que sur les futaies régulières étudiées par l’IFN, il gagnerait à être affiné par l’étude d’autres modes de gestion, notamment les futaies irrégulières.
Si les chiffres concernant les peuplements à maturité relativement élevée sont aujourd’hui peu précis et incertains, ceux concernant les forêts à faible maturité sont bien connus : 79 % des peuplements en France métropolitaine ont moins de 100 ans [2].
Aujourd’hui, les peuplements les plus âgés se trouvent en haute montagne et les arbres les plus vieux se développent en général sur des falaises. Les plus vieux arbres connus en France, des genévriers de Phénicie qui auraient environ 1500 ans, se trouvent dans les parois des gorges de l’Ardèche [24]. Dans des peuplements plus courants, notre expérience révèle que les sapinières de plus de 300 ans, les pineraies Laricio de Corse de plus de 400 ans, les hêtraies de plus de 250 ans et les chênaies de 350 ans sont très rares, mais sans doute à considérer comme les peuplements de France ayant la plus grande maturité.
2.1.3 Ancienneté et maturité : deux qualités définies à différentes échelles et non exclusives
L’ancienneté et la maturité se définissent sur des échelles bien différentes d’un point de vue fonctionnel, spatial et temporel :
- • lorsqu’on considère le gradient de maturité, il n’y a pas de modification de l’usage des sols, seul le peuplement des arbres est modifié dans l’écosystème. Tandis que l’ancienneté est induite par une rupture dans la présence du boisement, un changement plus profond est induit à la fois sur le peuplement (déboisement) et le sol (mise en culture) ;
- • la maturité est une qualité du peuplement, tandis que l’ancienneté qualifie, en général, un(e) site/endroit/localité (grand(e) ou petit(e)) ;
- • le pas de temps pertinent pour l’ancienneté se définit sur plusieurs siècles, voire même plusieurs millénaires. La maturité est décrite à l’échelle du cycle de vie de l’essence dominante, qui peut varier de quelques décennies à quelques siècles.
Ces qualités ne s’excluent pas mutuellement. Une forêt est dite ancienne quelle que soit l’exploitation actuelle ou passée. Ainsi, une forêt ancienne peut être constituée de peuplements à n’importe quel degré de maturité.
À l’inverse, une forêt ayant dépassé la moitié de sa longévité est ancienne, sauf dans quelques rares cas, comme certaines essences à croissance rapide. Un peuplement à maturité relativement élevée peut ainsi être récent dans quelques cas, par exemple, au sein d’une forêt alluviale à bois tendres ou d’un accru de bouleau verruqueux. Dans le cas général, toutefois, une forêt à maturité élevée est la plupart du temps ancienne.
2.1.4 Mise au point sémantique des qualificatifs associés à l’ancienneté et à la maturité
La langue française présente de nombreuses subtilités et parfois des synonymes purs. Avec l’émergence de la notion de naturalité, des qualités d‘ancienneté, de maturité, etc., les termes pour qualifier les différents degrés de ces qualités se sont multipliés. Afin d’être utilisés dans la littérature scientifique, les termes employés gagneraient cependant à être précisément définis. Nous proposons une synthèse (Tableau 1) de l’ensemble des termes couramment utilisés pour qualifier différents degrés d’ancienneté et de maturité et nous leur associons une définition basée sur la littérature nationale et internationale.
Définitions des termes employés dans la littérature pour caractériser les forêts du domaine tempéré.
| Terme | Définition/sous cas | Termes anglais équivalents | Degré d’ancienneté | Degré de maturité | Références |
| Forêt primaire | Espace boisé continu de grande taille (100 km2 minimum), constitué depuis la dernière glaciation par colonisation spontanée de terrains nus, et qui n’a subi aucune exploitation par prélèvement de bois, pâturage ou chasse ayant perturbé la structure et la composition naturelle de manière significative. L’intégrité des écosystèmes constitutifs n’a été altérée, ni dans leur fonctionnement, ni dans leur biodiversité | Primary forest, Virgin forest, Natural forest | Ancienneté de 8000 ans (millénaire) | Élevé | [6,7,30,85,103] |
| Forêt secondaire | Toute forêt non primaire : espace ayant été déboisé, forêt exploitée, pâturée ou chassée de façon plus ou moins intensive, mais non marginale | Secondary forest | Variable | Variable | [6,30,88] |
| Forêt subnaturelle | Forêt secondaire jamais exploitée ou de façon marginale, se développant depuis une longue période sans perturbation anthropique importante et ayant les caractéristiques fonctionnelles et structurelles qui en découlent. La durée d’abandon nécessaire varie selon les caractéristiques originelles des peuplements : d’une centaine d’années pour des dryades en futaie jardinée jusqu’à 500 ans au moins pour des pionnières en monoculture équienne | Old-growth forest | Ancienneté de plusieurs siècles (suivant le contexte) | Élevé | [4,31–33,35,40,103–108] |
| Forêt ancienne | Espace présentant une continuité de l’état boisé depuis une date fixée, qui correspond classiquement au minimum forestier du milieu du XIXe siècle en France. Cet espace a pu être défriché, puis reboisé, avant le minimum forestier Aucune caractéristique d’exploitation ou de non-exploitation, de maturité des peuplements ou d’avancement dans la succession écologique, n’est liée à cette définition |
Ancient forest | Ancienneté de 200 ans | Variable | [4–7,48,62–64,103,109,110] |
| Forêt ancienne médiévale | Espace boisé en continu depuis au moins le moyen âge | Ancien forest | Ancienneté de 600 ans | Variable | Termes définis pour la première fois dans cet article |
| Forêt ancienne gallo-romaine | Espace boisé en continu depuis au moins l’époque gallo-romaine | Ancien forest | Ancienneté de 2000 ans | Variable | |
| Forêt ancienne millénaire | Forêt ancienne n’ayant jamais été déboisée et formée par colonisation d’un sol nu par la forêt depuis la dernière glaciation (la composition dendrologique ayant pu évoluer) | Ancien forest | Ancienneté de 8000 ans | Variable | [13] |
| Forêt récente | Par opposition à une forêt ancienne : forêt boisée à partir d’un sol non forestier et postérieure à une date donnée (le minimum forestier en France) | Recent forest | Ancienneté inférieure à 150 ans | Variable | [4,6,48,63] |
Plusieurs applications des qualités d’ancienneté et de maturité sont possibles. Elles servent notamment à évaluer le degré de naturalité d’un peuplement. Pour nous permettre de bien décrire et comprendre le développement naturel d’un peuplement, il nous est nécessaire de prendre en compte une troisième qualité clé de l’écosystème : la dynamique.
2.2 Une troisième qualité pour définir l’évolution d’un peuplement : la dynamique
2.2.1 Définition
La dynamique est une qualité intrinsèque d’un écosystème qui met en relation les causes, les mécanismes et les processus provoquant des changements de composition, de structure et de maturité, qu’ils soient d’origine spontanée, anthropique ou mixte. La dynamique fait appel à de nombreuses relations fonctionnelles entre les espèces (dissémination, compétition…), avec les perturbations (tempêtes, incendies) et est également sous dépendance des conditions stationnelles.
Champs de travail important depuis longtemps en écologie (par exemple, [25]), les théories écologiques sur la dynamique comprennent plusieurs concepts complémentaires : la succession linéaire, le cycle sylvigénétique et les perturbations.
La succession linéaire est « l’évolution au cours du temps de la composition des espèces et de la physionomie de la végétation sur un même site où le climat reste constant » [26]. Pour la décrire, on parle classiquement de stades de succession (pionnier, transitoire et terminal). Le premier stade est souvent constitué d’essences pionnières héliophiles, à fort pouvoir de dispersion, à forte croissance juvénile mais à faible longévité, comme les bouleaux, les saules ou encore le peuplier tremble. Ces essences sont remplacées par des nomades (appelées parfois post-pionnières : érables, frêne commun, etc.) au stade transitoire. Le stade terminal est dominé par des essences dryades, longévives et tolérant l’ombre (hêtre, sapin pectiné, etc.) ou parfois par des nomades lorsqu’un blocage stationnel local arrête la succession (c’est le cas, par exemple, des forêts sur éboulis instables) [27].
Une fois le dernier stade de succession installé, l’écosystème reste dynamique (« équilibre dynamique ») et est alors dominé par des processus de dynamique cyclique interne au stade terminal ou cycle sylvigénétique. Cette notion redonne toute sa profondeur dynamique à la notion de climax [25], qui a trop souvent été vue de façon fixiste. Tout équilibre n’est que temporaire dans l’écosystème forestier et peut être modifié par des conditions extérieures, comme par exemple un changement climatique, ou bien, le plus souvent, une perturbation. Des facteurs internes peuvent également intervenir, comme par exemple des changements génétiques (dérives, mutations, hybridations…). Durant cette phase d’équilibre dynamique, les dryades se maintiennent dans un cycle de vie du peuplement forestier qui a une durée moyenne, selon les écosystèmes, de 100 à plus de 500 ans. Le cycle est souvent décomposé en cinq phases de durées variables [28], dites de régénération, de croissance, de maturation, de vieillissement et d’écroulement.
Les perturbations naturelles sont, avec la sénescence naturelle des arbres, le moteur de la dynamique rythmant la vie de l’écosystème. En climat tempéré, les forêts sont façonnées par les tempêtes et la mortalité naturelle individuelle, il en résulte en une mosaïque fine où les différents stades de développement sont présents, et qui est caractéristique des forêts naturelles (surface moyenne des taches de quelques centaines à quelques milliers de mètres carrés) [29].
2.2.2 Évolution naturelle d’un peuplement : vers l’état subnaturel
À chaque stade de la succession linéaire, les peuplements se développent le long d’un gradient de maturité (Fig. 1). L’état le plus avancé du développement naturel est un peuplement :
- • dominé par des essences dryades ;
- • présentant une mosaïque de degrés de maturité et ;
- • faisant partie d’une forêt ancienne (Fig. 1).

Les gradients d’ancienneté, de maturité et de dynamique dans le cas d’une forêt tempérée en évolution naturelle.
Il est nommé subnaturel par Greslier et al. [30]. Dans la littérature internationale, ces peuplements sont nommés par le terme d’old-growth forests [31–35].
En plus des valeurs écologiques que comportent tous les peuplements à maturité élevée, les forêts subnaturelles présentent une biodiversité animale comme végétale plus élevée que les peuplements ayant simplement dépassé l’âge d’exploitabilité [35]. Les peuplements subnaturels ont un rôle à jouer face au changement climatique, car ils représentent des stocks importants de carbone [36]. Contrairement à ce qui a été généralement admis depuis des décennies [37], une forêt subnaturelle continue à stocker du carbone, notamment dans le sol. Les arbres âgés continuent leur croissance et leur photosynthèse et, de ce fait, stockent encore du carbone en quantité non négligeable [38,39]. Les peuplements subnaturels sont également sources de diversité des essences et de diversité génétique intraspécifique (par l’absence de sélection anthropique), ce qui pourrait permettre aux peuplements et aux essences de s’adapter plus facilement aux changements [35].
Malgré leur importance écologique, ces écosystèmes forestiers subnaturels sont rares dans le monde et en particulier en France. Les chiffres estimant la surface des old-growth forests aux États-Unis varient selon les régions, mais sur l’ensemble du pays, le chiffre de 4 % peut être retenu [34,35]. En Roumanie, Giurgiu et al. [40] estimaient, en 2001, une surface totale d’environ 250 000 ha de forêts vierges et subnaturelles, soit 4 % de la surface boisée du pays. En France, ce type de forêt n’est étudié que depuis très récemment, et peu de données chiffrées sont actuellement disponibles sur l’ensemble du territoire. Le chiffre de 30 000 ha (soit moins de 0,2 % de la surface forestière française), a été évalué « à la louche » à des fins pratiques [23,41,42] et n’est scientifiquement plus recevable aujourd’hui. L’étude des vieilles forêts des Pyrénées, dont les résultats ne sont pas encore publiés, aboutit à une valeur de 7000 ha de forêts subnaturelles dans les Pyrénées de Midi-Pyrénées, soit 2 % de la surface du territoire. Ces forêts sont essentiellement situées aux étages montagnards supérieur et subalpin.
Comme cela a été mis en évidence par l’IGN [2], certaines essences pionnières sont peu longévives et les peuplements sont considérés comme « âgés » après 70 ans de reconquête forestière. Or, il faut bien plus longtemps aux espèces et aux paramètres édaphiques pour retrouver les caractéristiques de milieux forestiers peu perturbés que l’on peut trouver dans les forêts subnaturelles. Ainsi, les peuplements à maturité élevée d’essences pionnières ne peuvent être apparentés, en termes d’état de conservation, à des écosystèmes subnaturels. La dynamique forestière doit donc être prise en compte pour évaluer correctement le développement biologique et écologique d’un peuplement.
De manière générale, c’est en prenant en compte toutes les qualités et toutes les composantes d’un écosystème forestier que l’évaluation de son état de conservation est la plus pertinente. Toutefois, ancienneté, maturité et complétude de la dynamique forestière sont les trois qualités les plus décisives aujourd’hui en Europe pour distinguer les forêts subnaturelles des forêts à degré de naturalité plus faible.
Les conséquences écologiques de la dynamique étant étudiées et admises par tous depuis longtemps [25,26,43–45], nous ne les détaillerons pas davantage dans les parties suivantes.
2.3 Conséquences des variations d’ancienneté et de maturité sur l’écosystème forestier
2.3.1 Conséquences pédologiques de la rupture de l’état boisé
Le défrichement et l’utilisation des sols pour le pâturage ou l’agriculture modifient les équilibres chimiques et microbiens des sols. À court terme, le labour provoque des pertes de 50 à 75 % de la biomasse microbienne du sol, réduit la quantité d’azote potentiellement minéralisable et augmente la nitrification nette [46]. À long terme, les horizons de surface d’un sol forestier issu d’un sol préalablement agricole présentent, en comparaison avec un sol anciennement boisé, une plus faible quantité de carbone, une quantité d’azote et de phosphore plus importante et un rapport C/N des horizons de surface plus faible [47–49]. Ces impacts sur les sols sont encore visibles 2000 ans après un retour à l’usage forestier [50]. Une mise en culture à l’époque gallo-romaine d’une forêt dite ancienne aujourd’hui (boisée depuis 1850) a un impact significatif sur la fertilité, les concentrations de magnésium et sodium et provoque une augmentation significative de la concentration de phosphore et d’azote et une diminution significative du rapport C/N [51].
Toutefois, les conséquences de l’usage des sols sur le pH ne sont pas toujours significatives et les résultats sont parfois contradictoires. Le pH est légèrement plus élevé dans les horizons de surface (jusqu’à 15 cm de profondeur) dans les sols autrefois en culture [46]. A contrario, Bossuyt et al. [52] montrent qu’après 50 ans d’abandon de l’agriculture, il n’y a plus de différence significative entre les pH des horizons Ah et Bt (au sens du référentiel CPCS de 1967) et les mêmes horizons en forêt ancienne. Ils montrent néanmoins que 125 ans sont nécessaires à un horizon E pour revenir à un pH semblable à celui d’une forêt ancienne. Dambrine et al. montrent un effet de l’occupation romaine encore significatif sur le pH actuel des horizons minéraux de surface (0 à 10 cm) du sol [51].
2.3.2 Conséquence pédologique d’une réduction de la maturité
Sans intervention humaine, les arbres vivent longtemps (plusieurs siècles pour la majorité des espèces), présentent une longue phase de vieillissement et de sénescence, puis meurent et se décomposent. L’intégralité de la matière organique et des minéraux qu’ils contiennent retourne dans le sol : les cycles des éléments minéraux sont bouclés, hors événements particuliers (lessivage excessif, par exemple). Par l’exploitation sylvicole, l’homme exporte tout ou partie de ces minéraux à l’extérieur de l’écosystème forestier et influence significativement les flux d’azote et de carbone [53,54]. La biomasse ligneuse est en effet un réservoir important d’éléments chimiques tels que le carbone : 60 % de la masse de carbone de l’écosystème est contenue dans les arbres vivants [53]. Les fortes valeurs prises par les attributs de maturité qui caractérisent les peuplements à maturité élevée, et en particulier le volume de très gros bois vivant sur pied et l’abondance de bois mort en décomposition, déterminent le fonctionnement plus ou moins naturel de l’écosystème. Ces variables influencent également le taux de décomposition de la matière organique du fait d’un microclimat plus humide et tamponné, mais également car la présence des espèces de décomposeurs du bois mort en dépend [54]. L’exploitation sylvicole, en particulier les coupes rases, induisent également une perte indirecte de nutriment en augmentant la décomposition de la litière et le lessivage des nutriments [55].
2.3.3 Conséquences des variations de l’ancienneté sur la biodiversité
La conversion d’une forêt vers un usage agricole du sol élimine la grande majorité des espèces de faune, de flore et de fonge forestières présentes et modifie les banques de graines dans le sol. Ces éliminations et modifications sont d’autant plus importantes que le sol a été labouré [4] et que la durée de l’exploitation agricole a été longue. Lors du retour du couvert forestier, la recolonisation du milieu par les espèces spécialistes de la forêt n’est pas assurée : des différences notoires de composition spécifique existent, pour les herbacées et les arthropodes, entre les forêts récentes et les forêts anciennes [56]. Il y a une différence de composition spécifique dans le tapis herbacé entre des forêts anciennes et celui des forêts récentes, et ce, quel que soit le mode de gestion actuel (y compris avec un régime de taillis) [4]. Les espèces significativement plus présentes en forêt ancienne qu’en forêt récente sont nombreuses et servent d’espèces indicatrices d’ancienneté. En forêt feuillue, 34,5 % des espèces herbacées forestières d’une région de Belgique sont significativement plus présentes en forêt ancienne [57], et cette proportion peut dépasser 50 % en forêt feuillue sur le sol riche [47]. Les traits biologiques des communautés de plantes diffèrent entre les forêts récentes et anciennes. La végétation des forêts récentes est significativement plus héliophile et plus compétitive que celle des forêts anciennes [48]. Les forêts anciennes sont dominées par des hémicryptophytes et des géophytes (53 % des espèces de forêts anciennes), alors que les forêts récentes le sont par les phanérophytes et les chamaephytes (62 % des espèces) [48]. Les lichens sont également impactés par l’ancienneté [58,59].
Les modifications des sols entraînées par la mise en culture ont également des conséquences indirectes sur la biodiversité qu’ils portent. Par exemple, l’ajout de nutriments par l’agriculture modifie les relations de compétition entre les espèces herbacées : les espèces résistantes au stress sont remplacées par des espèces plus compétitives [60,61]. La modification de la forme d’humus influe également sur la biodiversité, non seulement sur la forme biologique dominante, mais également sur la richesse spécifique croissante, depuis le Mor jusqu’à l’Eumull [62].
En ce qui concerne la faune, certaines espèces forestières de carabes sont significativement plus présentes en forêt ancienne qu’en forêt récente (4 espèces/22 observées, [63]) [64]. Le caractère « relique » (pratiquement absentes des forêts récentes) est mis en évidence pour deux espèces (Carabus glabratus et Abax parallelus) [63,65].
Au début du XIXe siècle, l’impact de la mise en culture sur la biodiversité a été démontré pour des forêts ayant une ancienneté supérieure à 150 ans, notamment via l’impact des mises en culture de l’époque gallo-romaine [51]. Six pour cent (2/33) des espèces végétales étudiées par Vanwalleghem et al. [66] sont significativement influencées par l’utilisation des sols par les Gallo-Romains. Les cortèges de champignons terricoles, notamment les ectomycorhizes, sont aujourd’hui différents en fonction de l’usage des sols à cette époque [50].
Pour résumer, les usages passés des sols forestiers ont donc une double influence (Fig. 2) :
- • sur les composantes biotiques : diminution immédiate de la présence de certains taxons forestiers, modification des compositions des assemblages et des compétitions interspécifiques. Cela se prolonge dans le temps du fait de la capacité limitée de dispersion de certaines espèces ;
- • sur l’équilibre et la composition chimique des sols, ayant elle-même une influence sur la composition spécifique. La résilience est également faible.
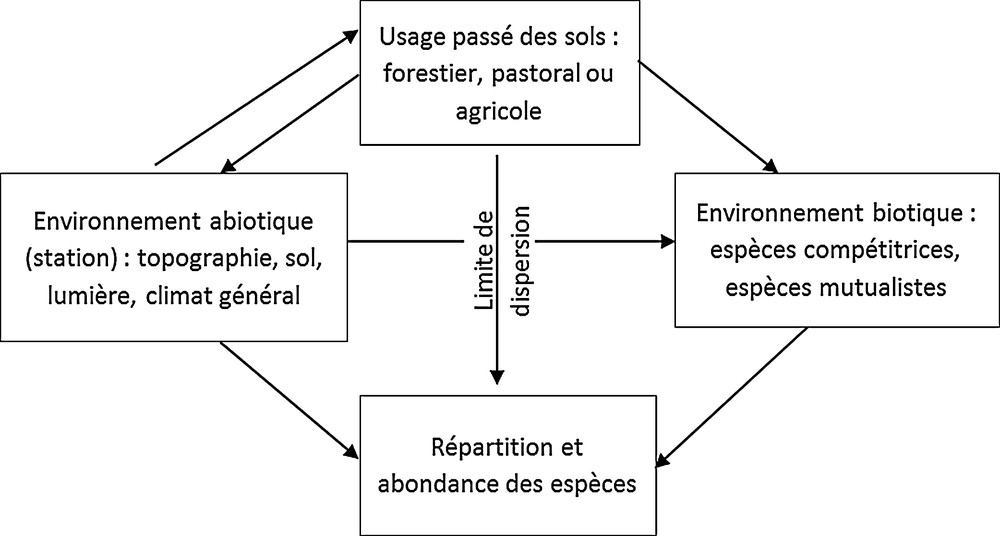
Les conséquences de l’usage passé des sols sur la biodiversité (d’après [101], modifié). Les flèches symbolisent une action ou une influence d’un facteur sur l’autre.
La littérature démontre un impact des mises en culture sur les sols et la biodiversité même pour des forêts avec une ancienneté plus grande, remontant avant le XVIIIe siècle ou même à l’époque gallo-romaine.
2.3.4 Conséquences de la faible maturité des forêts tempérées sur la biodiversité
Les espèces végétales et animales présentes en forêt évoluent avec la maturité. La diversité spécifique, et en particulier celle des espèces rares, de lichens [67], de mollusques et d’oiseaux [68] est significativement et positivement corrélée à l’âge du peuplement [69]. La diversité des attributs qui caractérise les écosystèmes forestiers à maturité élevée (diversité du bois mort, des diamètres, des dendro-microhabitats, complexité de la stratification, etc.) est source de diversité spécifique [70]. On estime que plus de 25 % des espèces forestières sont, par exemple, liées au bois mort et aux microhabitats portés par les arbres vivants [71–73]. Ces espèces sont pour la plupart saproxyliques et dépendantes de l’abondance et de la diversité du bois mort. Parmi elles, se trouvent principalement des coléoptères [74,75], des champignons [76] et de petits mammifères [77]. De nombreuses espèces ne sont présentes que dans les arbres âgés, présentant des diamètres importants ou des microhabitats particuliers [78–80].
2.3.5 Similitudes des processus à l’origine des différences pédologiques et écologiques
Les forêts à maturité et/ou ancienneté élevée se distinguent des autres par deux aspects : leur composition en espèces et leurs caractéristiques édaphiques. Ce n’est pas un hasard si l’ancienneté et la maturité ont des influences sur les mêmes paramètres, ces deux qualités sont liées aux mêmes causes et aux mêmes processus généraux : la modification des cycles des nutriments et la capacité de recolonisation des espèces.
Que ce soit par l’exploitation sylvicole, l’utilisation agro-pastorale ou le passage de la forêt à l’agriculture, l’homme exporte la biomasse et la nécromasse de l’écosystème, en plus ou moins grande proportion. Avec le pâturage et la mise en culture, il effectue également des apports. Par ce biais, il modifie le retour des minéraux au sol et l’équilibre chimique de ce dernier. Les différences chimiques constatées entre les forêts anciennes et les forêts récentes, d’une part, et entre les peuplements exploités et les peuplements non exploités, d’autre part, sont causées par le même processus : l’exportation, voire l’apport, de matière.
Les différences de biodiversité observées entre forêts anciennes et récentes d’une part, et peuplements à maturité élevée et jeunes d’autre part, sont liées au même processus d’extinction/recolonisation. Lorsque l’homme exploite la forêt, ou bien qu’il la transforme en système agricole, il réduit ou détruit la ressource pour les espèces forestières. Certaines d’entre elles disparaissent quasi immédiatement, tandis que d’autres disparaîtront plus tard : c’est ce que l’on appelle la dette d’extinction [81]. Inversement, lors du retour à l’état boisé, ou à une maturité élevée, certaines espèces recoloniseront rapidement les espaces, tandis que d’autres ne les recoloniseront que bien plus tardivement [82]. Ce processus de recolonisation est dépendant de facteurs abiotiques (exigences d’habitat des espèces) et de facteurs biotiques (mobilité des espèces) [49,83] et la part relative de ces facteurs reste pour l’instant mal connue.
Les études portant sur les capacités de dispersion et la biologie des espèces permettront à la fois d’étudier les processus d’extinction/recolonisation liés à l’ancienneté et la maturité de façon transversale, mais également de mieux comprendre et utiliser le caractère indicateur de ces espèces.
Le Tableau 2 dresse le bilan des différences et similitudes des qualités d’ancienneté et de maturité.
Différences et similitudes des qualités d’ancienneté et de maturité de l’écosystème forestier.
| Ancienneté | Maturité | ||
| Échelle | Échelle temporelle | Jusqu’au début de l’Holocène | Longévité de l’essence en peuplement |
| Échelle spatiale | Forêt | Peuplement | |
| Influence de l’activité humaine | Usage passé forestier vs défrichement et usage agricole des sols (plus ou moins ancien) | Absence d’exploitation vs gestion sylvicole récente et réductrice de la nécromasse ligneuse, des dendro-microhabitats et TGB | |
| Impacts | Biodiversité concernée | Flore herbacée, champignons ectomycorhizien; mollusques, coléoptères | Cavicoles, saproxyliques, organismes de milieu tamponné |
| Biodiversité potentiellement concernée (études en cours) | Coléoptères, faune du sol, autres groupes de champignons | Organismes liés à des houppiers à structures complexes | |
| Caractéristiques édaphiques | Cycle du carbone, de l’azote et du phosphore | Cycle du carbone et influence sur les stocks de matière organique | |
| État de conservation | Surface de la forêt française concernée | 29 % (d’après les cartes de Cassini) | 3 % de peuplement ayant dépassé l’âge d’exploitabilité |
| Prise en compte dans les méthodes d’évaluation de la biodiversité | IBP ; état de conservation Natura 2000 ; évaluation de la naturalité | IBP ; évaluation de la naturalité | |
| Outils de protection | Aucun spécifique aux forêts anciennes aujourd’hui ; mais conservation de l’état boisé par les documents d’aménagement forestier | RBI ; îlots de sénescence | |
| Valeur éthique | Écosystèmes témoins de naturalité élevée, valeur de mémoire |
2.4 Proposition de structuration des concepts et leurs limites
2.4.1 Certaines époques clés pour structurer l’ancienneté
À l’heure actuelle, deux termes sont couramment utilisés pour caractériser le gradient d’ancienneté d’une forêt (Fig. 3) : récente, ancienne (comme défini précédemment). Plusieurs milliers d’années séparent la moitié du XIXe siècle de la dernière glaciation. Or comme nous l’avons déjà vu, l’utilisation agricole de ces espaces durant cette période a une influence notable sur les sols et la biodiversité.

Le gradient d’ancienneté dans le contexte français, depuis la dernière glaciation (d’après [13,102], modifié).
Il apparaît donc nécessaire d’introduire, au moins théoriquement pour l’instant, d’autres seuils d’ancienneté. Ces seuils, pour être pertinents, doivent être définis à partir de l’histoire humaine et des forêts (phases de défrichement et déprise). L’histoire des forêts de l’Europe est par exemple marquée par trois époques de forte pression anthropique : l’époque romaine, le moyen âge et le début de l’ère industrielle (1830–1870). Ces seuils doivent également être réfléchis par rapport à la résilience aux impacts de ces mises en culture, tant du point de vue des sols que de la vitesse de recolonisation des espèces.
Au vu des connaissances actuelles sur l’évolution de la surface boisée en France, nous proposons quatre seuils d’ancienneté notables (Fig. 3) :
- • une ancienneté supérieure à 8000 ans. Une forêt qui serait boisée depuis la fin de l’emprise des glaces, le début de l’Holocène, est appelée forêt ancienne millénaire, comme déjà proposé par Emberger et al. [13]. Ce seuil conduit probablement à une surface extrêmement faible en France. Les extrapolations des paramètres de résilience connus (sol, dispersion des espèces) montrent que les processus à l’œuvre, qui expliquent par exemple la recolonisation des espèces forestières après la dernière glaciation, sont d’une autre nature que ceux évoqués. Des auteurs, dans d’autres contextes, montrent l’importance de la non-interruption par la glaciation, reliant ainsi de fait l’ancienneté telle qu’elle est généralement comprise (temps court) avec la question de l’évolution et de la spéciation sur le temps très long [84] ;
- • une ancienneté supérieure à 2000 ans. Un espace boisé en continu depuis l’époque gallo romaine, période durant laquelle la forêt a subi une forte pression et dont la mise en culture a encore des répercussions visibles aujourd’hui [50,51,66]. Nous proposons de qualifier ces boisements de « forêts anciennes gallo-romaines ». Il semble, au vu des données disponibles, que les processus dirigeant l’ancienneté soient extrapolables jusqu’à cette période. L’archéologie forestière à ce jour conduit à penser que leur surface est faible dans les grands massifs de plaine en France, mais aucune étude exhaustive n’existe ;
- • une ancienneté supérieure à 600 ans. Un espace boisé en continu depuis la fin du moyen âge (XIIe–XIIIe siècle). L’impact de cette ancienneté n’a toutefois pas été à ce jour documenté et distingué des autres. Mais, puisque les changements d’usage des sols à l’époque gallo-romaine ont encore des impacts visibles aujourd’hui, ce mimimum, plus récent, devrait avoir des conséquences sur les sols davantage visibles. Nous proposons d’appeler ces espaces « forêts anciennes médiévales » ;
- • une ancienneté supérieure à 150 ans. Une forêt boisée en continu depuis le dernier minimum forestier du milieu du XIXe siècle est qualifiée, comme c’est déjà le cas, de forêt ancienne.
Notons que ces différents termes peuvent se superposer : une forêt ancienne gallo-romaine est, de fait, également médiévale et ancienne. Il conviendra d’employer le qualificatif associé à l’époque correspondant à la preuve la plus ancienne de la continuité de l’état boisé.
2.4.2 Limites de la pertinence du concept d’ancienneté
À l’heure actuelle, les degrés d’ancienneté des forêts dites anciennes ne sont pas distingués, qu’elles soient boisées depuis plusieurs millénaires ou seulement depuis 1850. Ceci est en grande partie lié à la difficulté de caractériser avec précision l’usage passé des terres, par manque d’outils ou par nécessité de recours à des moyens coûteux, comme par exemple des recherches archéologiques ou par Lidar (télédétection par laser des microtopographies témoignant des usages passés) [85]. Ces différences d’historique pourtant regroupées sous le terme de forêt ancienne pourraient expliquer la non-significativité de certains résultats, ou bien la contradiction entre certaines études. Il est donc souhaitable de préciser l’ancienneté plus en détail, là où les données sont disponibles pour le faire. C’est la raison pour laquelle nous proposons ces seuils d’ancienneté. Étant donné le coût élevé des études pour déterminer l’ancienneté (Lidar, recherche archéologique), la précision de ce gradient est pour l’instant surtout utile et accessible aux scientifiques.
Le seuil du millénaire est très théorique et, avec les moyens d’études actuels, difficile à prouver. Le seuil d’ancienneté médiévale (600 ans) est proposé ici alors qu’il n’existe pas à notre connaissance d’étude scientifique prouvant son influence spécifique et distincte sur la biodiversité ou les paramètres édaphiques. Plus on remonte dans le temps, plus l’importance de la capacité de dispersion versus les caractéristiques chimiques des sols pour expliquer la répartition des espèces se complexifient et donc, plus il est difficile de mesurer avec précision l’influence de ces seuils sur l’écosystème.
Une forte variabilité spatiale des espèces indicatrices d’ancienneté apparaît dans la littérature. Selon les régions du monde, le cortège floristique des forêts anciennes peut changer [7]. Les espèces indicatrices d’ancienneté varient également entre les régions biogéographiques d’un même pays [48]. Il est envisageable que la distinction de ces seuils d’ancienneté et de leurs conséquences conduira à des listes d’espèces indicatrices plus fiables et plus stables.
Dans d’autres contextes comme celui de l’île de la Gomera, qui n’a pas été sous l’emprise des glaces durant la dernière glaciation européenne, la continuité de l’état boisé a une influence sur une échelle de temps beaucoup plus longue. Nogué et al. [84] montrent son importance sur l’évolution (spéciation) et l’adaptation des espèces. Dans des contextes de continuité forestière plus longue, ces paramètres ont une influence visible sur la répartition des espèces et rendent l’interprétation de l’ancienneté plus complexe.
À cette échelle de temps, la continuité est un facteur explicatif de la répartition de certaines espèces, qui doit être considéré, entre autres, en lien avec l’évolution du génome de celles-ci et du climat. La capacité de dispersion ne peut, à elle seule, expliquer la répartition de l’espèce, comme classiquement dans l’ancienneté. Certaines espèces, comme la Jacinthe des bois (Hyacinthoides non-scripta) ont une capacité de dispersion estimée, suivant les conditions locales, entre quelques mètres et quelques centaines de mètres par siècle et sont caractéristiques des forêts anciennes. Or, la Jacinthe des bois se trouve aujourd’hui dans le Nord de la France, zone impossible à atteindre en 8000 ou même 12 000 ans, depuis les refuges glaciaires du Sud de l’Europe. Notons que la compétition entre espèces, les conditions stationnelles et climatiques ou des évènements exceptionnels (coupes rases, tempêtes, inondations…) sont également des facteurs particulièrement importants qui peuvent expliquer des variations dans les vitesses de recolonisation [61].
Il semble que les processus à l’œuvre soient alors différents (évolution, spéciation, compétition, climat) et que l’ancienneté telle qu’elle est généralement définie montre ici toutes ses limites.
2.4.3 Synthèse des structurations du gradient de maturité existantes
À l’échelle de l’arbre, l’appréciation du développement biologique nécessite une lecture de l’architecture des arbres [86], ce qui permet d’identifier quatre stades de développement fondés sur des « unités architecturales » (Fig. 4 ; [87]). Le premier est celui de l’arbre jeune : à ce stade, chaque espèce se caractérise par un ordre de ramification limité (par exemple, 3 pour le noyer royal et le frêne commun, 4 pour les chênes, le châtaignier et le merisier). Les branches sont fines et ont une durée de vie brève car elles sont amenées à disparaître par élagage naturel. Elles forment donc un houppier transitoire dont la forme conique est typique. L’arbre jeune ne fleurit pas, ou peu. Avec la mise en place des branches maîtresses permanentes réitérant l’unité architecturale, la forme du houppier des feuillus passe progressivement de conique à sphérique. Les branches, constituées de fourches successives, se terminent par des axes caractéristiques : ils sont rectilignes, de grande taille (50 cm à 1 m de longueur), abondamment ramifiés et fertiles. Ils confèrent au houppier un aspect régulier et compact. L’arbre est alors au stade adulte. Chez les conifères, c’est à ce moment que la cime s’arrondit. Le stade mature est atteint lorsque l’arbre arrive à son volume définitif. À ce stade, les branches continuent à se développer, mais l’enveloppe du houppier n’augmente pas. Les nouveaux axes formés apparaissent les uns en retrait des autres et finissent par se courber sous leur propre poids. Ces systèmes d’arcures superposées et affaissées s’observent d’abord au niveau des branches basses, puis gagnent progressivement la cime. L’arbre mature a un contour irrégulier et semble éclater en une multitude de petits houppiers à l’image d’une vaste inflorescence de chou-fleur. L’expression de la sexualité est maximale. Chez les conifères, la réduction de la taille des pousses annuelles et de la ramification se traduit par une forme tabulaire au sommet du tronc. Quatrième et dernier stade du développement d’un arbre, la phase de sénescence commence par la dislocation du houppier et se poursuit par la mort progressive des branches ultimes. Ces pertes sont irréversibles, car la capacité de l’arbre à produire des gourmands, aptitude qui n’a cessé de diminuer au cours du vieillissement, est quasi nulle au moment de la sénescence. Chez les conifères, la sexualité mâle tend à devenir prépondérante et les cônes femelles se raréfient. Les phases mature et sénescente représentent plus de 50 % de la longévité de l’arbre.

Les quatre stades de développement pour les essences feuillues : arbre jeune, adulte, mature et sénescent (de gauche à droite). Dessins : S. Sabatier et C. Drénou.
À l’échelle du peuplement, des structurations du gradient de maturité ont été proposées également ; certaines sont basées sur l’économie sylvicole, d’autres davantage sur l’écologie.
Les sylviculteurs définissent la maturité uniquement comme une mesure de l’âge du peuplement ou la grosseur des arbres. Un arbre, tout comme un peuplement, est considéré comme mature lorsqu’il a atteint son âge ou diamètre d’exploitabilité [88]. Cette définition de la maturité est le fruit d’une vision purement économique. Étant donné que les âges d’exploitabilité utilisés en sylviculture de production se situent en général en deçà du premier tiers de vie du peuplement [3,89], cette conception de la maturité occulte une très grande part du développement biologique des arbres. De plus, cette définition de la maturité n’est pas pertinente d’un point de vue écologique.
Les méthodes d’évaluation de la maturité plus écologiques prennent en compte les différents paramètres témoignant du développement biologique du peuplement. Par exemple, Rossi et al. [90] utilisent l’ensemble du cycle de développement du peuplement, de sa naissance à après sa sénescence. Deux indicateurs servent à approcher la maturité du peuplement vivant (l’âge moyen de la cohorte d’arbres qui structure le peuplement et/ou la densité de TGB et TTGB) et un troisième indicateur se focalise sur la présence de la phase anabolique du peuplement (quantité de bois mort). Dans cette méthode, chacun des trois indicateurs est mesuré et noté.
2.4.4 Réflexions en vue d’une structuration du gradient de maturité
En lien avec ce qui apparaît déjà dans la littérature, nous proposons une structuration du gradient de maturité basée sur quatre paramètres qui évoluent avec le développement biologique des arbres :
- • l’âge moyen de la cohorte d’arbres qui structure le peuplement ;
- • le nombre de très gros bois ;
- • la quantité et la diversité du bois mort et ;
- • l’abondance et la diversité de certains dendro-microhabitats.
Différentes catégorisations de l’âge ont déjà été proposées. Par exemple, Rossi et Vallauri [91] regroupent les essences en quatre catégories suivant leur longévité estimée (les âges seuil des classes sont < 100 ans ; 200 ans ; 300 ans ; > 500 ans). Pour chaque catégorie, la maturité du peuplement est alors évaluée suivant cinq grandes classes d’âge (très jeune, soit a < 1/8 de la l’âge seuil de la classe ; jeune soit 1/8 < a < 1/4 ; adulte soit ¼ < a < 1/2 ; mature soit ½ < a < 3/4 ; âgé soit ¾ < a < 1, et enfin très vieux au-delà).
Pour quelques essences, l’évolution des dendro-microhabitats (diversité, fréquence) a été documentée et montre une différence marquée entre la première et la seconde moitié de la durée de vie de l’arbre. En particulier, les dendro-microhabitats sont significativement plus présents sur hêtres et sapins lorsque les arbres ont dépassé les 2/3 de leur longévité [92]. Leur occurrence est en relation avec la présence de très gros bois (TGB, d > 65 pour les résineux ou > 70 cm pour les feuillus) tels qu’ils sont définis par les bornes commerciales communément utilisées [88] et surtout les très gros bois (TTGB, d > 90 cm pour les feuillus et d > 100 cm pour les résineux), car ces seuils de diamètre sont également pertinents pour la diversité des dendro-microhabitats [20].
Au niveau européen, des seuils de quantité de bois mort ont pu être établis en fonction de la biodiversité associée. Deux valeurs apparaissent fréquemment. La première est 20 m3/ha de bois mort total (au sol et sur pied). C’est au-delà de ce seuil que les espèces de coléoptères saproxyliques de hêtraie sont les plus nombreuses [93]. Dans un contexte boréal de pessière, les espèces de polypores menacées ne sont présentes qu’au-delà de ce seuil [94]. Lorsque les groupes taxonomiques étudiés sont plus nombreux (arthropodes saproxyliques, pics et polypores menacés) et les contextes différents (forêts boréales, tempérées de montagne et de plaines), la valeur seuil varie de 20–50 m3/ha [95] suivant les espèces et les contextes. Le deuxième seuil se situe aux alentours de 50–60 m3/ha. C’est au-delà de cette valeur qu’apparaissent en général les espèces de coléoptères rares, inféodées au bois mort de grande dimension et de stade de décomposition avancé [93]. Notons que ces seuils ont été établis en référence à des données taxonomiques et non pas directement en fonction du développement biologique du peuplement.
Il n’existe aujourd’hui que très peu d’études montrant le lien chiffré entre développement biologique du peuplement et la diversité/abondance des dendro-microhabitats ou le nombre de TGB ou TTGB. Ce manque actuel de références rend prématurée la mise en pratique de la proposition d’une structuration chiffrée du gradient de maturité incluant ces deux aspects de façon précise. Néanmoins, nous pensons que le degré de maturité devrait être estimé par une analyse multicritères qui intègrerait simultanément l’ensemble de ces quatre paramètres (âge, bois mort, TGB et dendro-microhabitats). Pour chacun d’entre eux, le gradient de maturité serait scindé en classes délimitées par des valeurs seuils.
2.4.5 Limites à la pertinence du concept de maturité
L’évaluation de la maturité est en partie basée sur l’âge des arbres structurant le peuplement. Or la longévité des essences est très mal connue dans nos contextes européens où la pression humaine a été très importante depuis plusieurs millénaires. Par exemple, le chêne sessile a une longévité individuelle estimée de « 500 à 1000 ans » [96]. Cette imprécision, qui va du simple au double, vient de la rareté d’arbres âgés de plus de 500 ans et de la variabilité induite par l’impact des conditions stationnelles, des caractéristiques du peuplement et de la compétition, sur la longévité. Le hêtre est quant à lui connu pour avoir une longévité inférieure au chêne, de « 150 à 300 ans » [96]. Pourtant, il existe des peuplements de hêtre bien plus âgés, comme dans le pays basque français, à Iraty où une hêtraie comportant des arbres de plus de 500 ans existe [97].
Les seuils de bois morts cités précédemment sont basés sur l’étude de plusieurs groupes d’espèces, ce qui leur donne un caractère très général. Cependant, pour certaines espèces très exigeantes, le besoin en bois mort peut s’avérer encore plus sélectif, et, par exemple, la conservation du champignon saproxylique Antrodiella citrinella nécessite plus de 140 m3/ha [98].
Les études récentes montrent que le type et la fréquence des dendro-microhabitats [16,99] et le volume de bois mort [95], tout comme la longévité [96], varient fortement en fonction de l’essence considérée, notamment entre feuillus et résineux. Des études complémentaires sur ces paramètres permettront dans les années à venir de structurer de façon précise le concept de maturité.
3 Conclusion et perspectives
La maturité et l’ancienneté sont deux qualités fonctionnelles des milieux forestiers. Différents termes permettent aujourd’hui de caractériser chaque degré d’ancienneté. En pratique, dans nos forêts tempérées, un peuplement à maturité élevée est souvent ancien, ce qui a longtemps provoqué une confusion entre ces deux termes.
Ces deux qualités ont toutes les deux des influences notoires et durables sur la biodiversité et sur les caractéristiques du sol forestier et, de ce fait, sont les déterminants de l’état de conservation de l’écosystème. Les études récentes permettent aujourd’hui de mettre en évidence la complexité de ces qualités. Si les différences écologiques notables entre forêts anciennes et récentes ne sont plus contestables aujourd’hui, il apparaît que ce niveau de précision de l’ancienneté n’est pas suffisant pour tout expliquer. Il est important de remonter plus loin dans le temps et d’étudier l’existence d’autres seuils d’ancienneté.
Les peuplements à maturité élevée suscitent aujourd’hui l’intérêt de plusieurs recherches, mais, dans un contexte européen fortement anthropisé depuis des siècles, nous ne savons que très peu de choses sur les peuplements en fin de longévité, degré ultime de la maturité.
Les questions transversales sur deux qualités telles que la capacité de dispersion/recolonisation des espèces liées à des degrés élevés d’ancienneté et de maturité devraient également être approfondies.
Aujourd’hui, les écosystèmes présentant des degrés élevés d’ancienneté et de maturité sont rares : 29 % de la forêt française est ancienne, 3 % a dépassé l’âge d’exploitabilité. Quant aux forêts subnaturelles, elles sont pratiquement inexistantes (moins de 0,2 % de la surface forestière). Cependant, ces forêts sont rarement protégées par la législation. Les politiques publiques actuelles protègent les écosystèmes forestiers en fonction de la rareté de leur type de végétation et sans disposition explicite pour leur état de conservation. Par exemple, une hêtraie-sapinière montagnarde subnaturelle, comme on en trouve encore quelques-unes dans les Pyrénées, est un écosystème extrêmement rare et pourtant non protégé par la législation, car les hêtraies-sapinières sont communes en France et dans l’ensemble des montagnes européennes (environ 380 000 km2, soit 4 % de l’ensemble des forêts européennes [100]). Pour être plus pertinentes, les politiques de conservation devraient intégrer trois dimensions dans leurs choix, toutes aussi importantes : le type d’habitat naturel (ripisylves, hêtraies, pessières alpines, érablaies sur éboulis, etc.), son histoire (ancienneté) et son état actuel (avancement dans la dynamique et maturité notamment).
Déclaration d’intérêts
Les auteurs déclarent ne pas avoir de conflits d’intérêts en relation avec cet article.
Remerciements
Les auteurs remercient sincèrement Jean-Luc Dupouey pour ses réflexions pertinentes, notamment en ce qui concerne la similitude des processus liés à l’ancienneté et la maturité. Merci également à Christophe Drenou pour ses apports sur l’architecture de l’arbre. Les auteurs remercient vivement les relecteurs de cet article pour leurs remarques pertinentes qui ont permis d’améliorer ce travail. Le lancement de ce travail a bénéficié du soutien du Service du patrimoine naturel (Muséum national d’histoire naturelle).


