1 Introduction
Les hypophosphites des éléments alcalins sont préparés en traitant les solutions chaudes des hydroxydes alcalins par du phosphore blanc :
L'obtention des hypophosphites d'éléments (tels que les éléments d) dont l'hydroxyde n'est pas soluble est réalisée par une autre méthode, plus compliquée et plus coûteuse. À cet effet, l'acide hypophosphoreux est préparé par réaction de l'hypophosphite de baryum avec l'acide sulfurique à 100% [2]; on le fait agir ensuite sur l'oxyde ou sur le carbonate du métal. Par exemple, l'obtention de l'hypophosphite de manganèse peut être représentée par les réactions suivantes :
Nous présentons dans cet article les résultats de l'étude du système quaternaire réciproque Na+,Mn2+/Br–,(H2PO2)–//H2O à 25 oC pour préparer ce sel.
2 Partie expérimentale
L'étude du système quaternaire Na+,Mn2+/Br–,(H2PO2)–//H2O est réalisée de la manière suivante : un mélange correspondant au point de double saturation en sels de chaque ternaire constitutif du système quaternaire étudié est préparé. Ce mélange contient un excès de sels non dissous et le quatrième constituant est alors ajouté jusqu'à saturation et apparition de celui-ci à l'état solide.
Pour réaliser la partie expérimentale de cette étude, on a utilisé les sels NaBr, NaH2PO2, MnBr2 et Mn(H2PO2)2, cristallisés deux fois. Nous avons également mesuré la viscosité et la densité du liquide en équilibre. La viscosité est mesurée par la méthode d'Ostwald et la densité par pycnométrie. La caractérisation des phases solides en équilibre est réalisée par la méthode des restes de Schreinemakers [7].
Les ions constituant le système étudié, parmi lesquels figurent Na+, Mn2+, Br– et H2PO2–, sont dosés par les méthodes analytiques classiques [8–10].
Nous avons étudié les quatre systèmes ternaires NaBr/NaH2PO2/H2O, NaBr/MnBr2/H2O, NaH2PO2/Mn(H2PO2)2/H2O, MnBr2/Mn(H2PO2)2/H2O et la coupe diagonale NaBr/Mn(H2PO2)2/H2O du système quaternaire réciproque Na+,Mn2+/Br–,(H2PO2)–//H2O par la méthode isothermique à la température 25°C.
On constate que, pour le système NaBr/NaH2PO2/H2O, le point invariant ternaire, où se trouvent en équilibre les phases solides NaBr·2 H2O et NaH2PO2·H2O, correspond à la composition suivante (% en masse): NaBr 22,11, NaH2PO2 40,28 et H2O 37,61. En présence de NaH2PO2, la solubilité de NaBr diminue de 49,44 a 22,11% au point invariant ternaire (invariant isotherme–isobare).
Pour le système NaBr/MnBr2/H2O, le point invariant ternaire, où se trouvent en équilibre les phases solides NaBr·2 H2O et MnBr2·4 H2O, correspond à la composition suivante (% en masse): NaBr 13,95, MnBr2 58,42 et H2O 27,63. En présence de MnBr2, la solubilité de NaBr diminue de 49,44 a 13,95% au point invariant ternaire (invariant isotherme–isobare).
La courbe de solubilité mutuelle du système NaH2PO2/Mn(H2PO2)2/H2O renferme deux branches de cristallisation, dont l'intersection correspond au point invariant ternaire, de composition (% en masse) : NaH2PO2 51,25, Mn(H2PO2)2 0,23 et H2O 48,52. En présence de NaH2PO2, la solubilité de Mn(H2PO2)2 diminue de 12,48 à 0,23% au point invariant ternaire (invariant isotherme–isobare). Deux phases solides se trouvent en équilibre en ce point, à savoir: NaH2PO2·H2O et Mn(H2PO2)2·H2O.
Pour le système MnBr2/Mn(H2PO2)2/H2O, le point invariant ternaire, où se trouvent en équilibre les phases solides Mn(H2PO2)2·H2O et MnBr·4 H2O, correspond a la composition suivante (% en masse): Mn(H2PO2)2 1,76, MnBr2 59,74 et H2O 38,50. En présence de MnBr2, la solubilité de Mn(H2PO2)2 diminue de 12,48 à 1,76 % au point invariant ternaire (invariant isotherme–isobare).
Dans la section diagonale NaBr/Mn(H2PO2)2/H2O, les seules phases solides en équilibre avec le liquide sont Mn(H2PO2)2·H2O et NaBr·2H2O. Un point de double saturation en sels est observé, dont les coordonnées sont: NaBr 46,62, Mn(H2PO2)2 3,92 et H2O 49,40 (% massique). En présence de NaBr, la solubilité de Mn(H2PO2)2 diminue de 12,48 à 3,92 % au point invariant ternaire (invariant isotherme–isobare).
Les caractérisations des points invariants (ternaires et quaternaires) déterminés dans le système quaternaire réciproque Na+,Mn2+/Br–,(H2PO2)–//H2O sont présentées dans le Tableau 1 et sur la Fig. 1.
Le système Na+,Mn2+/Br–,(H2PO2)–//H2O à 25 °C
| Phase liquide (% en masse) | d | η | Phase liquide (% mol. de sel) | Phase solide | ||||||
| NaBr | MnBr2 | NaH2PO2 | Mn(H2PO2)2 | (kg m–3) | (10–3 Pa s) | Na2Br2 | MnBr2 | Na2(H2PO2)2 | Mn(H2PO2)2 | (*) |
| 49,44 | 0,00 | 0,00 | 0,00 | 1548 | 2,05 | 100,00 | 0,00 | 0,00 | 0,00 | A |
| 0,00 | 60,90 | 0,00 | 0,00 | 1969 | 13,71 | 0,00 | 100,00 | 0,00 | 0,00 | B |
| 0,00 | 0,00 | 51,96 | 0,00 | 1394 | 17,60 | 0,00 | 0,00 | 100,00 | 0,00 | C |
| 0,00 | 0,00 | 0,00 | 12,48 | 1086 | 1,45 | 0,00 | 0,00 | 0,00 | 100,00 | D |
| 22,11 | 0,00 | 40,28 | 0,00 | 1627 | 26,80 | 31,92 | 0,00 | 68,08 | 0,00 | (A+C)** |
| 13,95 | 58,42 | 0,00 | 0,00 | 2023 | 17,10 | 19,94 | 80,06 | 0,00 | 0,00 | (A+B)** |
| 0,00 | 0,00 | 51,25 | 0,23 | 1393 | 16,84 | 0,00 | 0,00 | 99,60 | 0,40 | (C+D)** |
| 0,00 | 59,74 | 0,00 | 1,76 | 1978 | 16,25 | 0,00 | 96,69 | 0,00 | 3,31 | (B+D)** |
| 46,62 | 0,00 | 0,00 | 3,92 | 1576 | 2,27 | 91,44 | 0,00 | 0,00 | 8,56 | (A+D)** |
| 36,64 | 14,53 | 0,00 | 3,16 | 1709 | 6,69 | 67,73 | 25,75 | 0,00 | 6,52 | A+D |
| 26,08 | 30,98 | 0,00 | 2,32 | 1845 | 11,22 | 44,70 | 50,88 | 0,00 | 4,42 | A+D |
| 17,22 | 49,81 | 0,00 | 1,58 | 1985 | 15,75 | 25,82 | 71,56 | 0,00 | 2,62 | A+D |
| 4,61 | 59,31 | 0,00 | 1,50 | 2001 | 16,78 | 7,27 | 89,92 | 0,00 | 2,81 | B+D |
| 13,72 | 58,36 | 0,00 | 1,28 | 2047 | 17,85 | 19,31 | 78,69 | 0,00 | 2,00 | (A+B+D)*** |
| 36,25 | 0,00 | 16,20 | 1,35 | 1601 | 12,23 | 63,92 | 0,00 | 33,42 | 2,66 | A+D |
| 31,14 | 0,00 | 24,18 | 0,86 | 1613 | 17,28 | 51,46 | 0,00 | 46,96 | 1,58 | A+D |
| 26,42 | 0,00 | 32,76 | 0,58 | 1625 | 22,18 | 40,42 | 0,00 | 58,61 | 0,97 | A+D |
| 7,32 | 0,00 | 47,75 | 0,28 | 1474 | 20,17 | 11,51 | 0,00 | 87,99 | 0,50 | C+D |
| 22,00 | 0,00 | 40,22 | 0,39 | 1635 | 27,15 | 31,65 | 0,00 | 67,72 | 0,63 | (A+C+D)*** |
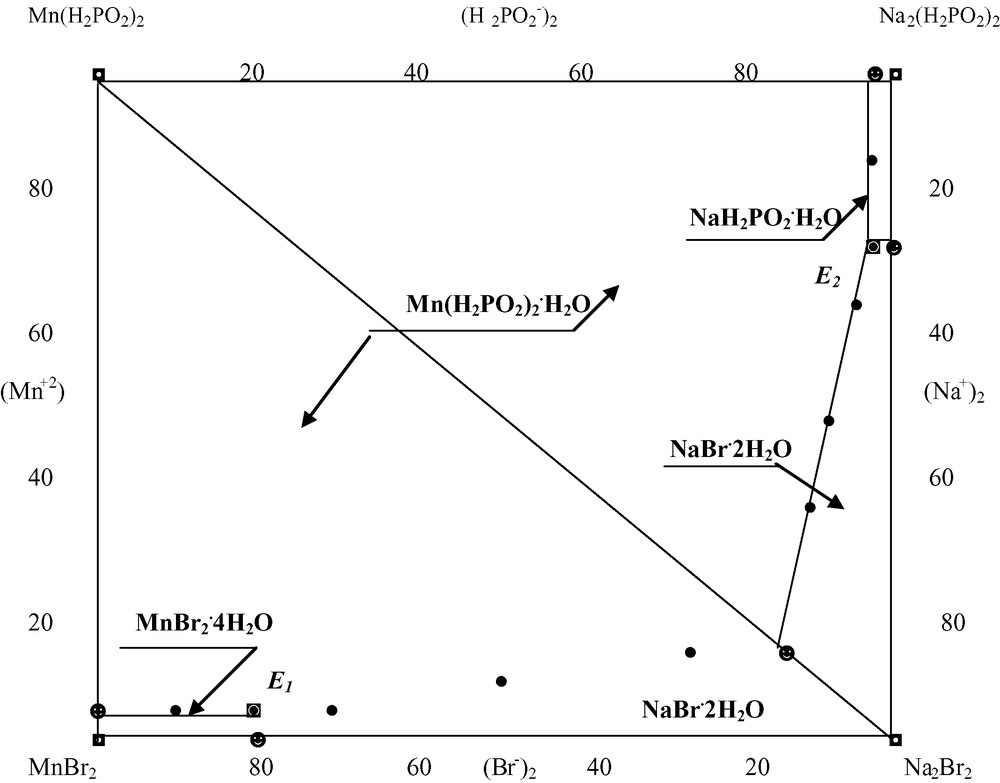
Le domaine de cristallisation des sel NaBr·2 H2O, MnBr2·4 H2O, NaH2PO2·H2O et Mn(H2PO2)2·H2O dans le système Na+,Mn2+/Br–,(H2PO2)–//H2O à 25 °C. Les compositions sont exprimées en pourcentage molaire de mélange salin.
3 Discussion et conclusion
Deux points invariants quaternaires sont déterminés dans le système quaternaire réciproque Na+,Mn2+/Br–,(H2PO2)–//H2O étudié à la température de 25 °C.
La composition du premier point invariant quaternaire E1 (Fig. 1) est la suivante (% en masse): NaBr 13,72, MnBr2 58,36, Mn(H2PO2)2 1,28 et H2O 26,64%. Dans ce point invariant, les trois phases solides suivantes se trouvent en équilibre avec la phase liquide : NaBr·2 H2O, MnBr2·4 H2O et Mn(H2PO2)2·H2O. La viscosité et la masse volumique de la phase liquide en équilibre au point en question sont respectivement de 17,85 × 10–3 Pa s et 2047 kg m–3.
Dans le deuxième point invariant quaternaire E2 (Fig. 1), trois phases solides suivantes se trouvent en équilibre avec la phase liquide: NaBr·2 H2O, NaH2PO2·H2O et Mn(H2PO2)2·H2O. La composition du point invariant considéré est la suivante (% en masse) : NaBr 22,00, NaH2PO2 40,22, Mn(H2PO2)2 0,39 et H2O 37,39. La viscosité et la masse volumique de la phase liquide en équilibre pour le point en question sont respectivement de 27,15 × 10–3 Pa s et 1635 kg m–3.
Se basant sur les résultats obtenus, on peut déduire la conclusion suivante : dans le système quaternaire réciproque Na+,Mn2+/Br–,(H2PO2)–//H2O, étudié à la température de 25 °C, l'hypophosphite de manganèse a la plus faible solubilité de tous les constituants et le domaine de cristallisation de Mn(H2PO2)2·H2O sur le diagramme (Fig. 1) est égal à 92,0% de la surface totale.
Finalement, on peut dire que la préparation de l'hypophosphite de manganèse Mn(H2PO2)2 peut être réalisée en se basant sur la réaction d'échange entre l'hypophosphite de sodium et le bromure de manganèse, car l'équilibre dans le système quaternaire réciproque Na+,Mn2+/Br–,(H2PO2)–//H2O est déplacé dans le sens de formation de l'hypophosphite de manganèse Mn(H2PO2)2


