1 Introduction
Les membranes permettent d'effectuer des séparations entre molécules et/ou ions de taille et de charge différentes. Elles sont généralement caractérisées par le seuil de coupure, qui indique à partir de quelle taille, exprimée en Dalton (1 Dalton = 1 g/mol), les particules sont retenues par le « medium » filtrant. Pourtant, lors du choix d'une membrane pour une application donnée, le seul paramètre de taille, des pores de la membrane ou des particules à séparer, ne suffit pas. Les fabricants de membranes donnent en général trop peu d'informations sur leurs produits, ou bien il est difficile de comparer les données fournies, car elles n'ont pas été établies dans les mêmes conditions opératoires.
Il en résulte que, faute de renseignements suffisants, le choix d'une membrane en vue d'une application donnée est encore aujourd'hui très empirique.
En pratique, chaque utilisateur est confronté au problème du colmatage qui peut parfois modifier considérablement les caractéristiques initiales des membranes [1–4], en limitant les performances des procédés de filtration. En fait, tout se passe au niveau de l'interface membrane–solution à traiter. Cette interface est très complexe et jusqu'ici très difficile à modéliser.
En limitant notre approche aux interactions entre les matériaux de filtration et les solutés présents dans les eaux à potabiliser et susceptibles de colmater les membranes, nous abordons l'opération de filtration avec une meilleure connaissance du matériau de départ grâce aux outils d'autopsies in situ des membranes, comme la mesure de la perméabilité hydraulique et la détermination du potentiel zêta. Ces outils sont complétés par l'étude des propriétés hydrophile–hydrophobe des matériaux grâce à des mesures d'angle de contact et des caractérisations morphologiques et topographiques, par microscopie électronique à balayage (MEB) et par microscopie à force atomique (AFM), respectivement. D'autres outils analytiques, plus récents dans le domaine des membranes, la spectroscopie d'électrons X (XPS ou ESCA), la microscopie confocale [5] et la pyrolyse, ont été mis en œuvre pour obtenir les caractéristiques chimiques des espèces colmatantes. Enfin, des analyses des solutions à filtrer ont été réalisées afin de mieux appréhender les variations de composition. Pour cela, les techniques analytiques comme le COD, l'UV254, la chromatographie d'exclusion de taille à haute pression (HPSEC) [6], l'analyse des acides aminés totaux et des sucres aminés, la dureté et l'alcalinité, ont été mises en œuvre.
Cette approche analytique globale est abordée dans le cas d'une eau réelle (eau brute de la Marne, préfiltrée 1 μm, prélevée au mois de mars 2003) et pour deux solutions synthétiques contenant des molécules colmatantes modèles : acides humiques et résidus d'algues.
Enfin, une étude préliminaire de modèles de colmatage des membranes (de types gâteau et accumulation dans les pores) est proposée dans le but d'évaluer la pertinence du paramètre MFI (Modified Fouling Index) en MF et en UF, pour les différentes solutions traitées par ces deux types de membranes.
Une seconde partie abordera le colmatage interne, en proposant un nouvel indice pour compléter la présente approche, limitée au colmatage de surface.
2 Matériels et méthodes
2.1 Les membranes
Les membranes étudiées sont, soit des membranes de microfiltration (MF), soit des membranes d'ultrafiltration (UF) ; toutes les deux sont constituées du même matériau en polysulfone (PSf) (Fig. 1). Il s'agit d'un carter d'une quinzaine de membranes, sous forme de fibres creuses, collées à leurs extrémités et formant un module de longueur utile 50 cm. Les membranes de MF ont un diamètre moyen de pore de 0,2 μm et celles d'UF de 10 ± 2 nm. Toutes ces membranes sont conservées dans une solution aqueuse constituée de glycérine et de bisulfite de sodium.
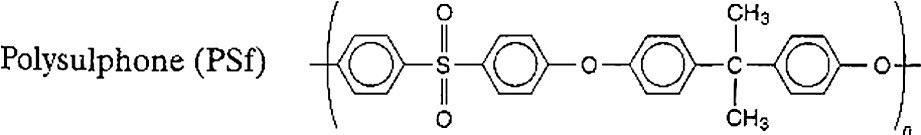
Formule chimique du polysulfone (PSf).
2.1.1 Conditionnement et déconditionnement des membranes
Toute membrane organique est fournie conditionnée pour éviter toute contamination du lieu de fabrication jusqu'à l'utilisateur. Avant toute utilisation, il est donc nécessaire de les déconditionner. Pour cela, un rinçage abondant à l'eau ultrapure est employé, comme préconisé par le fabricant.
2.1.2 Test d'intégrité
Avant toute mise en service des modules, un test d'intégrité est effectué. Cette étape consiste à purger à l'air comprimé, par le circuit perméat, le module immergé dans de l'eau ultrapure (UP). Il s'agit de détecter toute fuite d'air qui puisse provenir, soit d'un mouillage insuffisant, soit d'une casse de fibre ou encore d'un mauvais collage. La pression d'air est progressivement amenée à 1 bar.
2.2 Le pilote
2.2.1 Description des éléments du pilote
Le pilote comprend une unité de préfiltration indépendante. Utilisé pour l'étude des eaux brutes, ce système se compose de trois préfiltres montés en série (société CUNO) :
- ● cartouche de filtration de seuil de coupure 100 μm, Micro-screen en acier inoxydable ;
- ● cartouche de filtration de seuil de coupure 10 μm, Micro-klean III, en acrylique et résine phénolique ;
- ● cartouche de filtration de seuil de coupure 1 μm absolu, Betafine en polypropylène plissé.
La pompe utilisée pour alimenter les préfiltres est une pompe Multi Eco 33.8 KSB (hauteur d'aspiration maximale 8 m et pression de refoulement maximale 6 bar). Le pilote est constitué d'un « circuit perméat » et d'un « circuit alimentation » :
- ● circuit alimentation : une cuve en inox, résistant aux agressions chimiques (acides et oxydants), à doubles parois afin de maintenir l'eau d'alimentation à température constante ; une sonde de température est installée dans le fond de la cuve pour enregistrer la température tout au long des essais de filtration ; une pale d'agitation ; une colonne en PVC dans laquelle est placée le module de filtration ; une pompe centrifuge (KrP 25/4 de chez Heidolph) permettant la recirculation de l'eau d'alimentation entre la cuve et la colonne ; une cuve surélevée en amont, permettant d'alimenter en continu et par écoulement gravitaire la cuve inox ;
- ● circuit perméat : une pompe péristaltique à écrasement de tuyau (modèle PD 5101 de chez Heidolph) ; un capteur de pression (–1) à (+5) bar (modèle PR21R de chez Keller) dont le signal est enregistré ; un débitmètre électromagnétique (modèle Proline promag 50, Endress Hauser) dont le signal est enregistré en continu.
Chacun des circuits est équipé d'une électrode Ag–AgCl, judicieusement placée dans le circuit hydraulique et reliée à un millivoltmètre à haute impédance d'entrée (> 10 MΩ).
Une solution de KCl (2 × 10–4 M pour la MF et 10–3 M pour l'UF) est utilisée lors du déconditionnement des membranes afin d'une part d'assurer le déconditionnement et d'autre part de maintenir une conductivité minimale nécessaire au bon fonctionnement du débitmètre électromagnétique.
Lors de la filtration, le module fibre creuse est placé dans un carter de protection en PVC, ajouré de manière à permettre la circulation de l'eau autour des fibres et éviter le balancement susceptible de les fragiliser. La vitesse de circulation est de 0,018 m/s (Re = 1900).
Le schéma d'ensemble du pilote de filtration est présenté sur la Fig. 2.

Schéma du pilote de filtration.
2.2.2 Protocole expérimental
Le pilote est démarré en début de matinée et il fonctionne toute la journée. Il s'agit d'un mode de filtration frontal, à pression constante. Les prélèvements d'échantillons sont effectués en fin de journée au niveau des circuits de perméat et d'alimentation. Suite à ces prélèvements, le pilote est momentanément arrêté ; tout le système est alors vidangé, puis rincé à l'eau déminéralisée.
Le module de filtration subit ensuite un rétrolavage à l'eau ultrapure (cinq minutes à une pression de 0,7 à 0,8 bar pour la MF et 1 bar pour l'UF). Les eaux collectées lors de ce rétrolavage ont été mélangées pour constituer un échantillon moyen. Par la suite, ces échantillons moyens seront appelés eaux de rétrolavage ou backwash (BW).
Lorsqu'une perte de perméabilité hydraulique de 40% est atteinte, un nettoyage chimique est appliqué dont la procédure est fournie par la société productrice des fibres. Cette étape combine une première phase de nettoyage au chlore (solution à 200 ppm de chlore libre maintenue à 20 °C) à une deuxième phase de nettoyage à l'acide citrique (solution à 20 g/l maintenue à 35 °C). Chacune de ces deux étapes s'applique comme suit :
- ● 15 min de trempage avec recirculation de la solution dans la boucle du circuit d'alimentation ;
- ● 30 min de filtration à 350 mbar pour la membrane MF et à 450 mbar pour la membrane UF ;
- ● 5 min de trempage.
Entre les deux phases de nettoyage, le module membranaire est plongé quelques minutes dans un bain d'eau ultrapure.
2.3 Analyses des eaux étudiées
2.3.1 Les eaux naturelles de surface
Dans le Tableau 1 sont rassemblées les caractéristiques de l'eau réelle employée.
Caractéristiques de l'eau brute (eau brute préfiltrée à 1 μm)
| Paramètres | COD | UV254 nm | SUVA | Calcium | Alcalinité mg/L | Silice |
| (mg C/L) | (m–1) | (l/mg C.m) | mg/l | CaCO3 | (mgSiO2/l) | |
| Alimentation | 1,6–1,9 | 3,2–3,7 | 1,7–2,3 | 85 | 200 | 1,5 |
Il s'agit d'une eau de rivière, la Marne, prise au niveau de la station d'Annêt (région parisienne). Cette eau, peu chargée en matières organiques, est riche en minéraux (calcium et alcalinité élevés) et particulièrement en silice. La valeur du SUVA indique également qu'il s'agit d'une eau faiblement chargée en composés aromatiques, que l'on peut donc qualifier d'allochtone [4].
2.3.2 Les solutions synthétiques
L'étude réalisée sur les eaux naturelles a été complétée par des expériences de colmatage menées sur des solutions synthétiques préparées avec des acides humiques commerciaux d'origine terrestre et d'un extrait de matières organiques sécrétées par des algues. La solution de matière organique sécrétée par les algues provient du SERES (Service d'études et de recherches en environnement et santé publique, Nancy) ; la solution contenant les algues et leurs sécrétions a ensuite été filtrée sur 0,22 μm avant d'être congelée. À partir de ce filtrat, nos solutions synthétiques ont été préparées avec de l'eau osmosée. Cette solution est notée par la suite MO algale. La solution d'acides humiques, d'origine terrestre (Fluka), est préparée à la concentration de 10 ppm avec de l'eau osmosée, qui sera notée AH. Les principales caractéristiques de ces deux solutions sont rassemblées dans le Tableau 2. Il apparaît dans ce tableau que les absorbances UV pour la solution algale sont faibles, valeurs inférieures à 4/m ; en revanche, de très fortes absorbances sont à noter pour les solutions d'acides humiques préparées pour les expériences de colmatage des membranes MF et UF ; elles peuvent atteindre jusqu'à 24,5/m. Par ailleurs, en termes de carbone organique, la solution de résidus d'algues présente une concentration plus élevée par rapport à la solution d'acides humiques.
Caractéristiques générales des solutions synthétiques
| Solution | COD (mgC/l) | UV254 nm (1/m) | SUVA (l/mgC/m) |
| MO algale | 7,2–9,4 | 1,4–3,8 | 0,16–0,45 |
| Acides humiques MF | 3,3–3,5 | 20,2–23,7 | 6,1–6,8 |
| Acides humiques UF | 3,4–3,7 | 21,4–24,5 | 6,1–6,9 |
Il est à souligner que les valeurs de SUVA différent entre les deux solutions :
- ● SUVA inférieur à 1 l/mg C–1 m–1 pour la solution algale ;
- ● SUVA supérieur à 5 l/mg C–1 m–1 pour les solutions d'acides humiques.
En conséquence, la solution d'AH possède un caractère aromatique nettement plus élevé que celui de la solution de MO algale. En outre, si l'on compare les SUVA des solutions synthétiques et de la solution réelle, il apparaît que l'eau réelle possède un caractère aromatique d'environ un tiers par rapport à celui de la solution d'acides humiques. Quant à la solution de MO algale, elle peut être qualifiée d'autochtone.
2.4 Les outils analytiques
2.4.1 Caractérisations des membranes
L'autopsie des membranes est menée selon deux approches, tout à fait complémentaires, et cela après chaque rétrolavage et chaque nettoyage chimique :
- ● la pyrolyse GC/MS des matières colmatantes isolées de la surface des fibres dans un bain à ultrasons (les fibres sont découpées en morceaux de 1–2 cm de long et mise sous ultrasons dans 50 ml d'eau ultrapure ; ensuite, la solution est filtrée sur une membrane en fibre de verre de diamètre de pores 1,2 μm, puis la solution est lyophilisée) ;
- ● l'analyse directe de la surface des fibres par la mise en œuvre des mesures d'angles de contact, d'AFM et FESEM, d'ESCA et de potentiel zêta.
2.4.2 Les méthodes analytiques
Le carbone organique dissous (COD) est mesuré à l'aide d'un appareil Shimadzu TOC 5000A. L'absorbance UV à 254 nm a été déterminée à l'aide d'un spectrophotomètre UV-VIS SAFAS Double Energy System 190(UP). La connaissance des deux paramètres COD et UV254 permet de déterminer le SUVA (absorbance UV spécifique) défini comme le rapport de l'absorbance UV à 254 nm par la teneur en COD de l'échantillon.
La matière colmatante (environ 1 mg pour un échantillon sec déposé dans un tube en quartz d'un volume de 100 μl) est soumise à une pyrolyse flash suivi d'une analyse GC/MS conformément à la méthode décrite par Bruchet et al. [8] en 1990. Les pyrolyses sont effectuées à 650 °C sous courant d'hélium (1 ml/min) dans une unité de pyrolyse Pyroprobe 2000 (Chemical Data Systems, Oxford, Pa), l'unité de pyrolyse est connectée à un chromatographe G1800A (Hewlett Packard) couplé à un détecteur à ionisation d'électrons ; la chambre de pyrolyse est préchauffée à 200 °C et la montée de la température du filament de platine est conduite à raison de 20°C/ms (Pyrolyse flash) jusqu'à 650 °C. Cette température est alors maintenue pendant 20 secondes, les produits de pyrolyse sont séparés sur colonne capillaire AT-WAX (Alltech) dimensions 30 m × 0,25 mm ; diamètre interne 1 μm, en programmation de température de 30 à 220 °C à 3 °C/min. L'identification des pics obtenus se fait grâce aux pyrochromatogrammes obtenus par pyrolyse de composés purs.
Le potentiel zêta des membranes est obtenu par un appareillage de mesure du potentiel d'écoulement, élaboré par nos soins en s'inspirant de la méthode décrite par Pontié et al. [9] en 1997. Une paire d'électrodes Ag–AgCl est judicieusement introduite dans le circuit hydraulique et reliée à un millivoltmètre à haute impédance d'entrée (> 10 MΩ). Un zêtamètre de laboratoire (Zetasizer Nanoseries de chez Malvern Instruments, États-Unis) a permis la détermination quasi simultanée de la répartition de taille et du potentiel zêta des particules présentes dans la solution d'AH.
Les angles de contact sont mesurés par la technique de la goutte posée (goutte d'eau ultrapure) grâce à un appareillage de type KG1 (KRUSS, Deutschland) équipé d'un goniomètre. Les volumes déposés sont de l'ordre de quelque microlitres. Chaque valeur présentée est la moyenne de cinq gouttes ; les valeurs obtenues sont toujours relatives, les écarts sont représentatifs lorsqu'ils sont supérieurs à 10°. Cho et al. [10] en 1998 ont utilisé cette technique pour comparer l'hydrophobie des membranes colmatées par la matière organique naturelle et les membranes nettoyées.
La microscopie à force atomique (AFM) est mise en œuvre sur des échantillons de membranes préalablement séchés. Les échantillons sont fixés à l'aide d'un ruban adhésif et la surface externe des fibres est analysée. L'appareillage est un nanoscope IIIA de chez Digital Instruments (multimode). Tous les échantillons sont analysés en mode tapping et par contraste de phase afin de déterminer la topographie des échantillons et mesurer leur rugosité moyenne de surface (Rms).
Le microscope électronique à balayage à effet de champ (FESEM) est un appareillage de type LEO1501. Avant chaque analyse, les échantillons sont fixés sur un ruban adhésif conducteur, recouvert sur les bords par de la laque à l'argent et enfin recouvert dans son ensemble par deux couches ultraminces de Pt/Pd (2 × 2 nm) réalisées par évaporation sous vide. Les énergies de faisceau varient entre 1 et 3 keV, les images sont analysées, soit en mode rasant (SE2), soit à 90° (In Lens). Cette méthode est utilisée par d'autres auteurs pour caractériser des membranes [11,12].
Les analyses ESCA (ou SPX) permettent d'atteindre une information sur la composition chimique élémentaire des membranes [13,14]. Les analyses ESCA sont menées sur un Scienta 200 (source : Al Kα monochromatic –450 W, de surface analysée 0,5 × 4 mm2, avec un angle de détection de 90° et une profondeur de pénétration de 10 nm). Tous les échantillons sont séchés au préalable. Les résultats présentés sont des moyennes de trois analyses effectuées en tête, au milieu et en queue de fibre.
3 Résultats et discussion
3.1 Caractéristiques des membranes vierges
Dans le Tableau 3, l'ensemble des caractéristiques initiales des membranes est rapporté. Il est intéressant de noter la différence des longueurs des fibres entre MF et UF. Toutefois, compte tenu des différences sur les diamètres internes, les surfaces géométriques exposées sont identiques. En revanche, dans le bas du tableau, des différences nettes apparaissent entre les deux membranes. Tout d'abord, leurs différences de perméabilité hydraulique qui est directement liée à leur différence de diamètre de pore. En ce qui concerne leur caractère hydrophile–hydrophobe, il apparaît, selon les lots, des valeurs très différentes des angles de contact. En effet, avec 0°, la membrane est totalement mouillante, avec 66°, elle est très nettement hydrophobe. L'explication de ces observations provient du procédé de fabrication. En effet, alors que la fabrication des modules industriels est parfaitement réglée et automatisée, celle des petits modules reste « artisanale ». En effet, lors de la préparation des membranes, le polymère est mélangé à des dérivés de la pyrrolidone (composé neutre), utilisés pour rendre le polymère plus hydrophile [15].
Caractéristiques générales des modules de MF et d'UF
| Membranes | MF PS | UF PS |
| Materiau | PS | PS |
| Diamètre interne (μm) | 350 | 380 |
| Diamètre externe (μm) | 720 | 720 |
| Longueur d'une fibre (cm) | 43 | 50 |
| Nombre de fibres | 15 | 15 |
| Surface géométrique (m2) | 0,02 | 0,02 |
| Diamètre de pore moyen en MF (μm)/Seuil de coupure en UF (kDa) | 0,2 μm | 100 kDa |
| (~10 nm) | ||
| Domaine de pH | 1 à 13 | 1 à 13 |
| Sens de la filtration | Extérieur → intérieur | Extérieur → intérieur |
| Perméabilité hydraulique | 250–350 | 90–150 |
| (l/h m2 bar) | ||
| Angle de contact (°) | 65–0a | 66–0a |
| Rms (nm) | (33–70) ± 10 | 10 ± 5 |
| Potentiel zêta (mV) (± 1) | (–8 à –29)a | (–11 à –49)a |
| Densité de pore/μm2 | 17 | 16 |
| Diamètre moyen (nm)b | 400 ± 220 | 46 ± 23 |
a Les valeurs rapportées tiennent compte des fluctuations observées pour les différents modules utilisés (soit au total une dizaine de modules pour chaque type de filtration MF et UF).
b diamètres de pores moyens issus des analyses AFM et FESEM.
Par ailleurs, les analyses AFM et FESEM effectuées sur les différents lots de fibres ont révélé que la répartition des pores présente une hétérogénéité en diamètre et en densité remarquable tout au long de la fibre. Les diamètres de pores obtenus diffèrent beaucoup de ceux donnés par le fabricant. Il faut toutefois moduler ces observations, car les analyses par AFM et FESEM donnent des valeurs de diamètres de pores obtenues seulement en surface. Pour être rigoureux, il faudrait compléter ce type d'analyse par des méthodes de perméation de gaz et de molécules calibrées, ainsi que rapportés récemment par Khayet et Matsuura [16] en 2003. Il est alors possible d'atteindre une caractérisation complète de la structure des pores des membranes fibres creuses, plus proche également des données du fabricant.
Pour les rugosités moyennes de surface, il apparaît également une différence nette entre les membranes de MF et d'UF, la seconde étant moins rugueuse en raison de son plus petit diamètre de pore. Là encore, selon les lots, notamment en MF, les valeurs peuvent être très dispersées (± 50%).
Enfin, pour ce qui concerne l'analyse de la charge de ces membranes, chacune d'elles est négative. L'origine de cette charge n'est pas encore connue ; toutefois, les fluctuations observées, selon les lots, peuvent être rapprochées à la présence de composés dérivés de la pyrrolidone. En fonction du temps de séchage de la fibre, de son rinçage et de son conditionnement, notamment en présence de glycérine, l'ensemble de ces facteurs peut influer à la fois sur la mouillabilité des matériaux mais aussi sur leur état de charge de surface.
3.2 Optimisation de l'étape de déconditionnement
Usuellement, toute étape de filtration sur membrane organique est précédée par un test de filtration à l'eau ultrapure (UP), dont le but est d'éliminer les agents conservateurs utilisés par les fabricants pour maintenir les membranes mouillées et donner une valeur guide de la perméabilité hydraulique initiale. Ce rinçage a pour effet d'éliminer les produits du conditionnement. Pontié et al. [17], en 2005, procèdent différemment pour déconditionner leurs membranes, un nettoyage à l'eau UP étant appliqué jusqu'à ce que la conductivité du perméat soit inférieure à 1 μs/cm. Martinez et al. [18], en 2002, déconditionnent aussi leurs membranes inorganiques avant utilisation ; ils utilisent une solution d'hypochlorite de sodium à 1 g/l en chlore libre, pH ajusté à 11 à l'aide de la soude pendant 30 min, 45 °C, pression transmembranaire de 0,7 bar et une vitesse de recirculation de 2 m/s. À la fin, la membrane est rincée à l'eau distillée pendant 10 min à 45 °C, pression transmembranaire de 0,4 bar et une vitesse de recirculation de 4 m/s.
Un exemple de déconditionnement est rapporté dans le Tableau 4.
Évolution de la perméabilité hydraulique d'une membrane MF lors de l'étape de déconditionnement
| Temps de rinçage (minutes) | (t = 50) | (t = 300) | (t = 500) | (t = 700) | (t = 900) |
| Perméabilité hydraulique (L/(h.m2.bar)) | 280 ± 20 | 285 ± 20 | 275 ± 20 | 270 ± 20 | 270 ± 20 |
On remarque que la valeur de la perméabilité hydraulique se stabilise autour de 270 l/(h m2 bar), et ce après 700 min de rinçage (soit environ 12 h).
3.3 Potentiel colmatant des eaux étudiées
3.3.1 Paramètres généraux de caractérisation du colmatage
3.3.1.1 Suivi de la perméabilité
Le suivi des pertes de perméabilité hydraulique des modules membranaires au cours du temps (ou de la charge organique reçue par la membrane) constitue une première approche de la caractérisation du colmatage des membranes [7,16,19–21,23]. Les Fig. 3 représentent la chute de perméabilité relative (ratio de la perméabilité sur la perméabilité obtenue lors de la première minute de filtration) en fonction de la charge organique reçue par la membrane lors de la filtration de l'eau naturelle étudiée (3a) et la solution d'AH (3b).
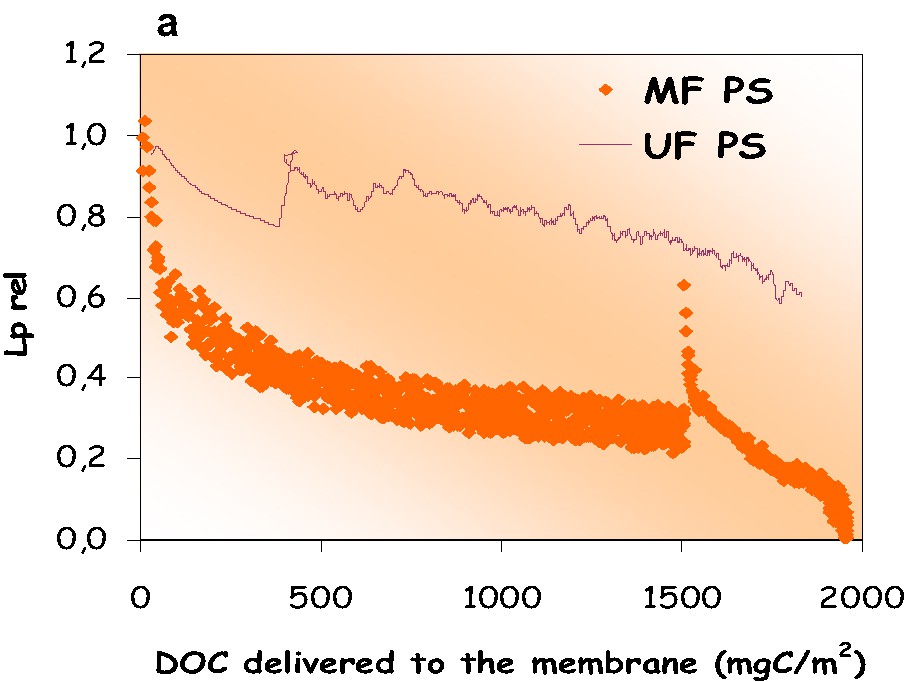

(a) Perméabilité relative en fonction de la quantité de COD vue par les membranes MF et UF lors de la filtration de l'eau de la Marne (préfiltrée sur 1 μm). (b) Perméabilité relative en fonction de la quantité de COD vue par les membranes MF et UF lors de la filtration de la solution d'AH.
Notons que les chutes de perméabilité sont nettement plus importantes pour la MF que pour l'UF. Cette tendance est observée sur l'ensemble des expériences menées. En outre, il apparaît que l'efficacité des rétrolavages est meilleure pour la solution d'acides humiques que l'eau réelle. Par ailleurs, l'impact de cette étape varie en fonction de la membrane considérée. En effet, la membrane MF se colmate plus vite. Dans le cas de l'eau de la Marne, après trois jours de filtration, 80 % de la perméabilité hydraulique initiale a été perdue, malgré les rétrolavages appliqués quotidiennement, ce qui traduit l'existence d'un colmatage sévère.
En revanche, la chute de performance hydraulique de la membrane UF est davantage progressive, puisque seulement 20% de perte sont observées après trois jours de filtration, témoignant également d'un colmatage important. Ce phénomène a été observé pour l'ensemble des tests de filtration menés (eau réelle et solutions synthétiques). Nous ne pouvons attribuer cette différence de comportement à la nature du matériau, qui est la même pour les deux membranes, mais bien plutôt à leurs différences morphologiques et topographiques. En particulier, la membrane MF possède un diamètre de pore moyen plus élevé, d'où une surface totale exposée à la solution colmatante plus importante, et par ailleurs elle possède une rugosité plus élevée, ce qui peut faciliter l'accrochage physique de matières colmatantes. Enfin, le pouvoir colmatant de l'eau de la Marne, de composition complexe : polysaccharides, protéines, humiques, et inorganiques, etc., est plus important que celui de la solution synthétique d'AH, comme nous le présenterons par la suite lors de l'étude consacrée aux indices de colmatage.
3.3.1.2 Caractérisation du colmatage en surface et dans les pores de la membrane
La présence de matières colmatantes à la fois en surface et dans les pores des membranes MF et UF est confirmée par la combinaison d'outils analytiques comme l'angle de contact, l'AFM et le potentiel zêta (Tableaux 5a et 5b). Ainsi, la mesure de la rugosité de surface (par AFM) a-t-elle mis en évidence un accroissement de ce paramètre après filtration de l'eau de la Marne, ce qui traduit la présence d'un dépôt en surface de la membrane. Par ailleurs, des modifications après colmatage des angles de contact sont révélatrices d'un dépôt de matières colmatantes à la surface des membranes. Le changement de coloration (apparition d'une couleur marron clair) est également une preuve de la modification de la surface. Par ailleurs, l'atténuation de la charge négative de la membrane, déduite des mesures de potentiel zêta traduit la présence d'un dépôt colmatant sur les parois des pores, ce qui nous permet d'avancer que les espèces colmatantes sont globalement plutôt neutres ou chargées positivement, comme on l'a rapporté récemment [17].
Évolution de la perméabilité hydraulique, de l'angle de contact, du potentiel zétâ et de la rugosité moyenne de surface (Rms) pour les membranes vierges déconditionnées, colmatées à l'eau de la Marne (après rétrolavage final) et nettoyées chimiquement
| Paramètres | Membranes | Vierges | Colmatées | Après nettoyage chimique |
| Perméabilité hydraulique (l/h m2 bar) | MF PS | 330 | 150 | 200 |
| UF PS | 140 | 65 | n.d. | |
| Angle de contact | MF PS | 0 ± 5 | 0 | 0 |
| (°) | UF PS | 0 ± 5 | 34 | 24 |
| Potentiel zêta | MF PS | –11 | –7 | –11 |
| (mV) (± 1) | UF PS | –2 | n.d. | n.d. |
| Rms (nm) | MF PS | 33 ± 10 | 52 ± 5 | 76 ± 20 |
| (surface analysée : 20 × 20 μm2) | UF PS | 7 ± 5 | 51 ± 8 | 86 ± 43 |
Caractéristiques physicochimiques des membranes colmatées par les AH et la MO algale
| Paramètres | Membranes | Membranes déconditionnées | Colmatées par les AH | Colmatées par les algues | Colmatées par les AH et nettoyées chimiquement | Colmatées par les algues et nettoyées chimiquement |
| Perméabilité à l'eau UP (l/h m2 bar) | UF PS | 150 ± 5 | 115 ± 5 | nd | 152 ± 3 | nd |
| MF PS | 290 ± 5 | 160 ± 5 | nd | 144 ± 5 | ||
| Potentiel zêta (± 1mV) | UF PS | –27 | nd | nd | nd | nd |
| MF PS | –20 | –16 | nd | –43 | ||
| Angle de contact (± 5°) | UF PS | 66 | 40 | 57 | 62 | nd |
| MF PS | 65 | 46 | nd | 66 | ||
| Rugosité moyenne (nm) | UF PS | 76 ± 8 | 46 ± 17 | 77 ± 4 | 33 ± 7 | nd |
| MF PS | 28 | 72 ± 34 | nd | 89 ± 35 |
L'analyse FESEM permet de mettre en évidence le dépôt de matières colmatantes à la surface et dans les pores de la membrane (Fig. 4, à droite).

Images 2D obtenues par analyses FESEM de la MF PS vierge (gauche) et après colmatage (droite).
Après nettoyage chimique, les composés colmatants ne sont que partiellement éliminés, ainsi que l'illustre le Tableau 5a,b. En effet, les résultats reportés dans ces tableaux montrent que les perméabilités hydrauliques ne sont pas retrouvées après nettoyage chimique, pour les deux solutions et les deux types de membranes, à l'exception de l'UF colmatée par les acides humiques, pour laquelle on retrouve la perméabilité initiale, ce qui traduit un colmatage irréversible.
En complément des résultats de perméabilités hydrauliques, les mesures d'angles de contact, de potentiel zêta et de rugosité moyenne de surface confirment l'efficacité partielle du protocole de nettoyage chimique. La même tendance a été observée pour toutes les solutions étudiées.
En conséquence, une optimisation de l'étape du nettoyage chimique apparaît indispensable pour améliorer les performances de ces membranes lors de leur utilisation industrielle.
3.3.2 Identification du matériel colmatant
3.3.2.1 Analyse des solutions d'alimentation, de perméats et de rétrolavage
En ce qui concerne l'analyse des valeurs de COD et d'absorbance UV254nm (Tableaux 2 et 3) et conformément aux résultats des auteurs [22,23], une différence peu significative entre les valeurs des eaux d'alimentation et des perméats a généralement été observée. En conséquence, les espèces organiques à l'origine du colmatage représenteraient une infime part des composés présents dans les eaux, et le colmatage serait la résultante de l'accumulation progressive de ces structures dans les pores et à la surface de la membrane.
Dans le cas des eaux naturelles, des analyses en HPSEC/UV conduites sur les solutions de rétrolavage ont montré [19] qu'en MF, les espèces colmatantes sont majoritairement constituées de structures non humiques de faible poids et haut poids moléculaires, riches en structures azotées. Il est apparu aussi qu'en UF, la teneur des solutions de rétrolavage en composés de type substances humiques est aussi importante que celle des deux précédentes catégories. L'analyse des acides aminés totaux et des sucres aminés totaux a également montré que les solutions de rétrolavage sont enrichies en composés azotés, comparées aux eaux d'alimentation.
3.3.2.2 Autopsie membranaire
Des analyses ESCA ont été menées sur les membranes colmatées (après rétrolavage final) et nettoyées chimiquement. Ces analyses ont montré que la composition de surface des membranes vierges diffère de celle des membranes colmatées et de celle des membranes après nettoyage chimique, mais dans une moindre mesure. La présence d'un dépôt en surface a été mise en évidence par la diminution de l'empreinte du matériau (chute de la teneur en soufre entrant dans la composition élémentaire), comme on l'a rapporté récemment [24]. À l'appui des résultats obtenus, la nature du matériel colmatant est essentiellement organique. En effet, un accroissement de la teneur en oxygène et azote, accompagné, d'une chute de la teneur en carbone, dans des proportions caractéristiques d'un dépôt organique, ont pu être observés à la surface des membranes colmatées. L'ESCA a montré également que les groupements fonctionnels dans lesquels l'azote est impliqué sont de type amine et amide, ce résultat ayant aussi été confirmé par l'analyse structurale du dépôt par pyrolyse CG/SM.
En effet, comme le montre la Fig. 5, des analyses en pyrolyse GC/MS ont été menées sur les matières colmatantes extraites par ultrasons des membranes colmatées après rétrolavage final, mais également après nettoyage chimique. À l'appui des chromatogrammes obtenus, le matériel colmatant analysé (quelle que soit la membrane considérée) serait un mélange de différents biopolymères, dont la principale composante est constituée de polysaccharides, de sucres aminés et de matériels protéinés, substances qui seraient essentiellement d'origine bactérienne ou plus largement microbienne [24]. Les substances humiques entrent également dans la composition du matériel colmatant à des teneurs plus faibles (pics de phénols et de crésol).
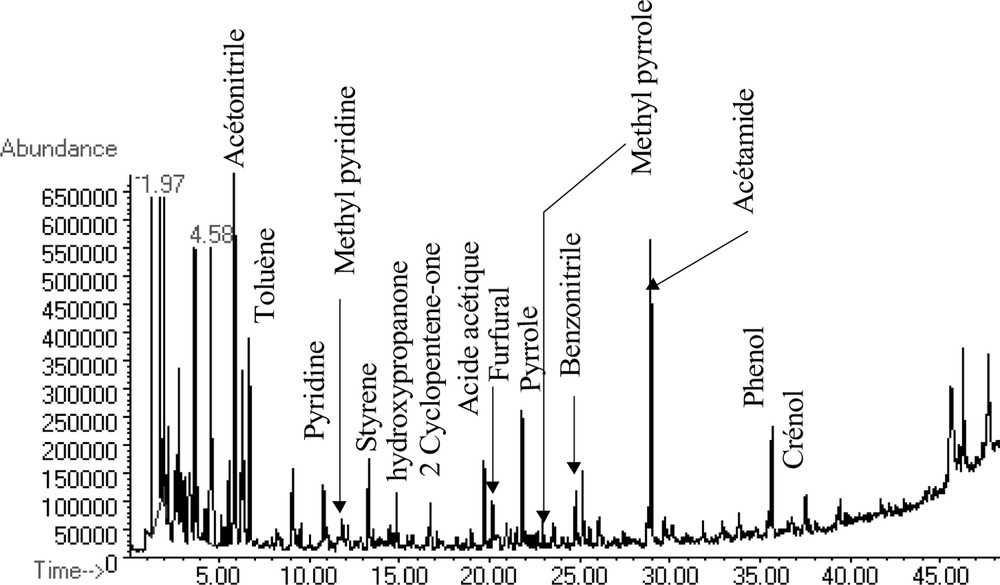
Pyrochromatogramme des matières colmatantes déposées sur la membrane MF après application d'un backflushing (eau de la Marne).
4 Modèles de colmatage (étude préliminaire)
4.1 Détermination des paramètres indice de colmatage modifié–MF et indice de colmatage modifié–UF pour les différentes solutions
Au cours des opérations de MF et d'UF, les membranes subissent des chutes de performances, entraînant une chute de production, en raison de l'apparition du phénomène de colmatage. De nombreux modèles ont été proposés afin de rendre compte de ce phénomène complexe [25]. Pour évaluer le pouvoir colmatant d'une eau, les scientifiques ont recours à des tests de filtration simples débouchant sur la détermination d'indices de colmatage. La représentativité de ces indices et leur fiabilité à prédire les risques de colmatage sur les installations de production d'eau potable restent discutables, les professionnels étant toujours à la recherche d'outils mieux adaptés à leur problématique. La plupart du temps, les scientifiques utilisent des outils qui reposent sur un mode de filtration frontale. Parmi les indices de colmatage les plus utilisés, nous citerons l'indice de colmatage FI (fouling index), l'indice de colmatage modifié MFI (modified fouling index) et l'indice de blocage des pores MPFI (mini-plugged factor index).
Le paramètre choisi dans cette étude est le MFI. Cet indice est basé sur l'exploitation du modèle de colmatage de type gâteau. Il a été proposé par Schippers et al. [26] en 1980, pour les membranes de MF et plus récemment [27] pour les membranes d'UF. Cette partie de nos travaux s'intéresse à la détermination des paramètres MFI–MF [28] et MFI–UF pour l'eau réelle et les solutions synthétiques étudiées précédemment. Cette étude préliminaire des modèles de colmatage devrait nous aider à évaluer l'importance de la présence de matières colmatantes seulement à la surface des membranes MF–UF, alors que les mesures de perméabilité hydraulique donnent un résultat plus global. De plus, le MFI est directement proportionnel à la concentration des particules colmatantes en solution. Sa détermination s'obtient en relevant l'évolution du débit de perméat au cours du temps (t) (ou en fonction du COD), comme illustré Fig. 3. La représentation de l'évolution du rapport t/V en fonction de V, le volume filtré, comme rapporté sur les graphes de la Fig. 6, possède une partie linéarisable, dont la pente permet de déduire le MFI [27].
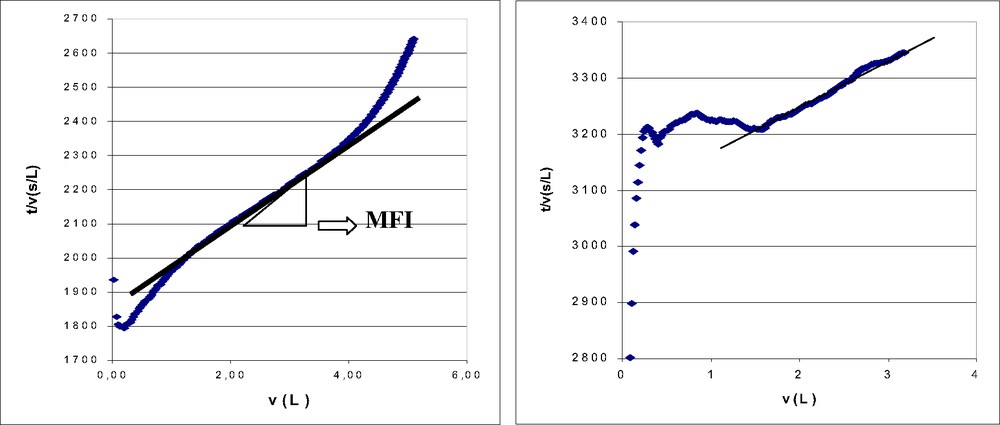
Modèle de colmatage de type gâteau lors de la filtration d'acides humiques, (UF à droite, MF à gauche).
Une analyse comparative des MFI–MF et des MFI–UF est possible à partir des résultats rapportés sur les Figs. 7,8. En première approche, il apparaît que l'eau réelle est la solution qui colmate le plus les deux types de membranes, comme cela a déjà été souligné précédemment lors de l'analyse des mesures de perméabilité hydraulique.
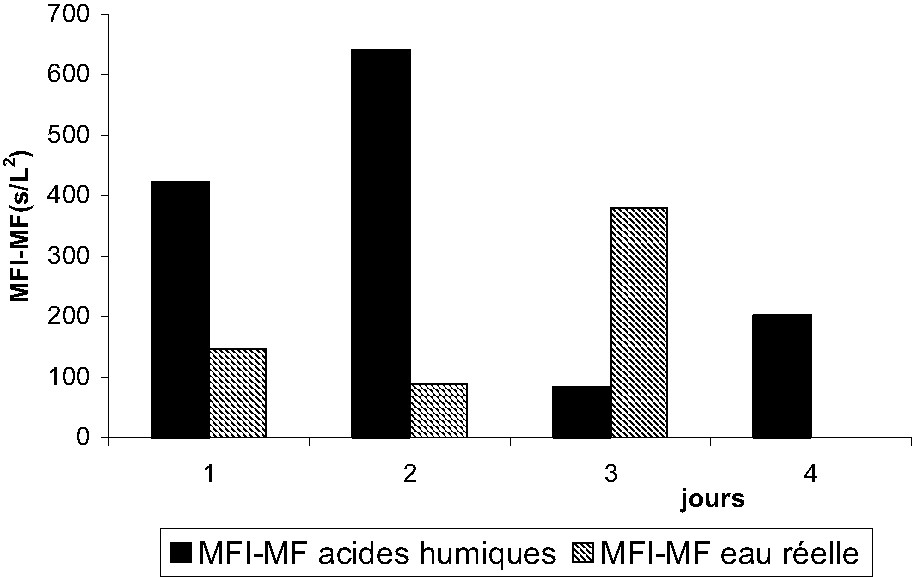
MFI-MF des solutions synthétiques d'acides humiques et de l'eau réelle.

MFI-UF des solutions synthétiques d'acides humiques et de résidus d'algues et l'eau réelle d'Annêt–Marne.
Cette observation a également été rapportée par certains auteurs [4,24,29]. En effet, les auteurs montrent en général que les fractions de matières organiques colmatantes prises séparément colmatent moins que leurs mélanges.
Par ailleurs, l'analyse de la Fig. 7 montre un comportement très différent de celui de l'eau réelle par rapport à la solution d'acides humiques. Si l'on compare maintenant, pour les résultats de la Fig. 8, le cumul des MFI, calculé comme la somme des MFI du premier au dernier jour, nous obtenons environ 1500 s/l2 pour la solution d'AH et 500 s/l2 pour l'eau réelle, soit un rapport d'un tiers. Ce résultat peut être rapproché du rapport un tiers obtenu également entre les valeurs des SUVA de ces deux solutions. Toutefois, dans le cas de l'eau réelle, il est nécessaire de moduler un peu notre propos en raison de l'influence d'interactions Ca–MON ou Si–MON, sur la membrane et en solution, et qui peuvent jouer un rôle non négligeable sur le colmatage. Malheureusement, nous n'avons pas pu obtenir de résultats de MFI–MF pour les algues en raison d'un problème d'intégrité intervenu au cours des expériences.
Si l'on analyse maintenant les résultats de MFI–UF obtenus cette fois pour les trois solutions (Fig. 8), il apparaît une différence très nette entre les acides humiques et les deux autres solutions. En effet, il faut six jours pour abaisser de 40% la perméabilité de la membrane UF avec la solution d'AH, et seulement trois pour les deux autres solutions. Cette différence de comportement est vraisemblablement due à une répulsion importante entre les structures aromatiques de la solution d'AH et le matériau de membrane, plutôt hydrophile. De plus, les mesures de potentiel zêta des membranes laissent apparaître un matériau chargé négativement.
En outre, des analyses simultanées de taille et de charge ont été obtenues pour la solution d'AH ; elles ont montré une répartition de taille globale de 200 nm et un potentiel zêta des particules de –48 mV. Cela montre qu'un phénomène de répulsion électrostatique peut également se combiner à la répulsion chimique. En revanche, avec une répartition de taille de 200 nm, on comprend mieux la raison pour laquelle la membrane MF, de diamètre de pore moyen 0,2 μm, est plus colmatée que celle d'UF.
Si l'on compare maintenant les MFI–UF de l'eau réelle et des résidus d'algues, ils semblent évoluer dans le même sens, pour les deux premiers jours. Lors du troisième jour, la valeur de MFI chute, elle ne peut pas être prise en compte, en raison d'un problème d'intégrité survenu au cours de l'expérience. De plus, la solution de résidus d'algues est celle qui laisse apparaître les plus fortes valeurs de MFI (> 2000 s/l2). Cela montre que cette solution est la plus limitante pour ce type de matériau d'UF. Compte tenu de son caractère autochtone marqué, elle possède davantage de structures solubles, donc hydrophiles et donc davantage susceptibles de colmater ce matériau également hydrophile. Ainsi, pour ce type de solution, les valeurs de MFI deviennent si élevées que le contrôle de la perméabilité et des flux de production associés est difficile, ce qui est effectivement le cas dans l'industrie en période de bloom algal. En effet, il est aujourd'hui connu que ce type de solution génère, au bout d'un certain temps, un gel qui s'avère très limitant pour les perméabilités des membranes.
L'analyse FESEM de la membranes colmatée par ces résidus d'algues, comme rapporté sur la Fig. 9, laisse apparaître des zones d'apparence très visqueuses, preuve de l'apparition de ce phénomène. la Fig. 9 (droite) présente l'évolution du rapport MFI–UF algues/MFI–UF AH. Nous remarquons que ce rapport s'inverse au cours de la filtration des deux solutions synthétiques, et est multiplié d'un facteur 8 à la fin de l'opération.

Image FESEM d'une zone gélifiée sur la membrane d'UF colmatée par les résidus d'algues ; la figure de droite no 10 présente l'évolution du rapport MFI–UF algues/MFI–UF AH au premier jour de filtration (1) et au dernier jour de filtration (2).
Pour résumer les résultats de cette étude préliminaire, le MFI est un outil intéressant pour évaluer les variations de composition des eaux d'alimentation, et sa complémentarité avec les mesures de perméabilité hydraulique apparaît aujourd'hui de plus en plus, et cela pour une conduite optimisée des opérations de filtration à basse pression, MF et UF.
5 Conclusion
Grâce à la combinaison des résultats d'analyse d'eau avec ceux issus des expériences d'autopsies des matériaux de filtration, nous avons proposé une démarche globale du colmatage des membranes MF et UF. Cela nous a permis d'élucider la nature des espèces les plus colmatantes qui sont les polysaccharides, les sucres aminés et les protéines, dont l'origine exacte reste encore à être élucidée. Les travaux entamés avec les solutions synthétiques vont se poursuivre avec d'autres espèces prises séparément et/ou en mélange (protéines, sucres aminés, etc.).
De plus, les résultats préliminaires obtenus sur les valeurs de MFI–UF et de MFI–MF ont montré leur complémentarité avec les mesures de perméabilité hydraulique. Cette étude constitue une nouvelle contribution à la validation de ce type d'outil pour l'évaluation du pouvoir colmatant des eaux naturelles et également pour le suivi de leurs variations saisonnières.
Cette nouvelle approche du colmatage des membranes MF–UF nous permet aujourd'hui d'intervenir plus efficacement sur les différentes étapes de la conduite des procédés à membranes (conditionnement–déconditionnement, nettoyages chimiques) et contribuer ainsi au développement durable de ces technologies en plein essor.
Remerciements
Les auteurs tiennent à remercier J.-L. Pastol (CECM, Paris) pour ses talents au FESEM, F. Sommer (Biophy research) pour les analyses AFM–ESCA et sa gentillesse, D. Olivier (ENSCP) et Hervé Buisson (Veolia Water) pour leur soutien logistique, J.-C. Schrotter (Veolia Water), V. Jacquemet (Veolia Water) et C. Machinal (Veolia Water) pour leur assistance technique.


