1 Introduction
Les baumes sont définis comme des substances naturelles d'origine végétale, souvent sirupeuses lors de l'exsudation ou de la récolte mais qui se solidifient en se desséchant. Caractérisés par une odeur suave, ils ont la particularité d'être partiellement solubles dans l'alcool et de contenir une proportion importante d'acides cinnamique et benzoïque libres [1,2] ou combinés sous forme d'esters [3]. Selon la pharmacopée française, il s'agit d'oléorésines aromatiques dont les plus employées sont les styrax et les benjoins. Les résines (constituées de dérivés terpéniques) peuvent aussi bien provenir de la production normale d'une plante saine (résines physiologiques) que d'un processus de défense consécutif à une blessure ou à l'attaque d'un agent pathogène (résines pathologiques).
Le benjoin est connu depuis l'antiquité et serait originaire de l'Inde. Dans les pays orientaux, sa fumée était censée éloigner les mauvais esprits et les maladies ce qui explique son utilisation lors de cérémonies rituelles. De ce fait, il a d'abord été considéré comme une variété d'encens (ici encens désigne une matière à brûler, l'encens véritable étant l'oliban) ou de myrrhe et comme substance précieuse faisant l'objet d'un commerce régulier dès le XVe siècle. Grâce à son odeur agréable [4], il a été très utilisé par les parfumeurs avant d'être, à la renaissance, introduit en médecine [5] pour lutter contre les inflammations chroniques de l'appareil respiratoire [6]. Dès la seconde moitié du VIIIe siècle, les chinois transportaient du benjoin de l'Asie tropicale vers la Chine. Mais c'est à partir du XIIIe siècle que les arabes en font véritablement le commerce en l'important au Moyen-Orient pour l'utiliser comme encens. Au cours d'une expédition en Orient de 1325 à 1349, Ibn Batouta note qu'à Sumatra, on produit de « l'encens de Java » dont il fait une description. L'encens de Java est appelé en arabe « luban Jawi » puis par déformation « banjawi » pour finalement aboutir à « benjoin ». En 1875, Planchon recense quatre types de benjoin : le benjoin en larmes venant du Siam, le benjoin amygdaloïde d'origine non citée, le benjoin en masse provenant de Calcutta ainsi qu'une variété endémique à l'île de Sumatra, nommée benjoin de Penang.
Au XXe siècle, dans la pharmacopée française, les benjoins sont répertoriés comme des résines exsudées par des arbres du genre Styrax (Styracaceae). Depuis 1937, on distingue deux principales catégories résineuses [7] : le benjoin du Siam (Styrax tonkinensis) et le benjoin de Sumatra (Styrax benzoin et/ou Styrax paralleloneurum).
Le mot storax vient du latin styrax (résine odorante), il existe aussi bien sous forme solide que liquide. Le storax solide également appelé storax-benjoin ou styrax-benjoin [8] est produit par l'aliboufier (Styrax officinalis). Sous le nom de storax liquide, sont nommés trois produits provenant d'arbres appartenant au genre Liquidambar de la famille des Hamamelidaceae : le storax de Turquie ou styrax officinal de Liquidambar orientalis, le storax d'Amérique de Liquidambar styraciflua et le storax de Java de Liquidambar altingiana.
Les résines benjoins sont donc exsudées par des arbres appartenant au genre styrax (Styracaceae) mais certaines résines de ce type comme celles provenant de l'aliboufier sont appelées styrax. La situation se complique d'autant plus par l'utilisation de l'appellation fréquente et mal définie de storax (synonyme incertain de styrax) incluant l'exsudat de plantes appartenant au genre Liquidambar (Hamamelidaceae). L'appellation styrax est souvent employée en égyptologie comme terme générique qualifiant l'ensemble des résines précédemment évoquées [9]. Ce travail pose le problème de la caractérisation de l'origine botanique et géographique des substances naturelles désignées comme styrax, storax, benjoin ou même styrax-benjoin, susceptibles d'avoir été utilisées comme matériaux du patrimoine culturel. Pour cela, une identification de marqueurs a été entreprise grâce à différentes techniques de la chimie analytique : spectroscopie infrarouge à transformée de Fourier (IRTF) et chromatographie liquide à haute performance couplée à une détection UV–Visible (CLHP–UV). Devant la difficulté de disposer de standards botaniquement certifiés, plusieurs échantillons commerciaux d'origine géographique parfaitement connue de benjoins du Siam et de Sumatra, de storax de Turquie et de styrax du Honduras ont été sélectionnés et ont servi de référence pour l'étude d'échantillons d'origine inconnue.
Par ailleurs, cette étude ayant amené à une comparaison avec de la dammar, quatre échantillons commerciaux de cette résine ont également servi de référence.
2 Répartition géographique des espèces végétales, obtention et composition chimique des baumes
2.1 Les benjoins
Les espèces qui produisent du benjoin font partie de la famille des Styracaceae dont la place dans la classification hiérarchique des êtres vivants est variable [10,11]. De manière générale, cette famille fait partie du sous-embranchement des angiospermes. Elle comprend 8 à 12 genres distincts dont six exotiques [12]. Ces derniers contiennent de 120 à 235 espèces environ qui vivent presque uniquement dans les pays intertropicaux et subtropicaux et dont la majorité appartient au genre styrax (entre 60 et 160 espèces). Le genre Styrax se répartit dans les zones chaudes et tempérées [13] du globe à l'exception de l'Afrique subsaharienne et de l'Australie. On distingue généralement trois grandes zones géographiques de répartition (Fig. 1) comportant diverses espèces (Tableau 1). S. tonkinensis est un arbre de 12 à 15 m de hauteur et de 80 à 90 cm de circonférence qui ressemble au bouleau et que l'on rencontre entre 600 et 2000 m d'altitude, sur des collines sablonneuses. Il atteint sa maturité au bout de dix ans. Il pousse spontanément en Extrême-Orient, dans les régions tropicales (Laos, Thaïlande, Viêt Nam). Il est cultivé dans d'autres pays du Sud-Est asiatique, comme la Malaisie [14]. Il fournit un baume appelé « benjoin du Siam » ou « benjoin du Laos ». S. benzoin pousse spontanément en Malaisie ainsi que sur les îles de Sumatra, Java et Bornéo. C'est un arbre buissonnant de 8 à 34 m de hauteur avec un tronc de 10 à 100 cm de diamètre, d'écorce grise à rouge sur 3 à 7 cm d'épaisseur, que l'on rencontre à faible altitude (le plus souvent entre 100 et 700 m). Il atteint 6 m de hauteur en quelques années seulement [15]. S. paralleloneurum se rencontre entre 575 et 1700 m d'altitude dans les forêts mixtes indonésiennes [16]. C'est un arbre dont l'allure générale est extrêmement voisine de celle de S. benzoin. Le tronc est de couleur claire, de 23 à 60 cm de diamètre et de 5 à 25 m de hauteur. S. benzoin et S. paralleloneurum sont à l'origine d'un baume appelé « benjoin de Sumatra ».
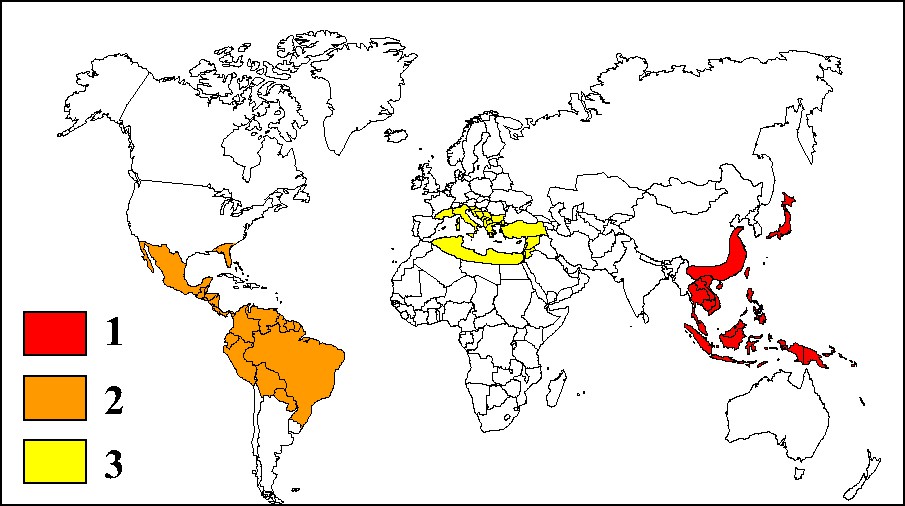
Répartition géographique des espèces botaniques appartenant au genre Styrax. Asie (zone 1), Amériques (zone 2), Bassin méditerranéen (zone 3).
Répartition géographique des espèces botaniques appartenant au genre Styrax
| Zone | Répartition géographique | Espèce botanique |
| 1 | Laos ; Thaïlande ; Viêt-Nam ; Malaisie | Styrax tonkinensis |
| Îles de Sumatra, Java et Bornéo ; Malaisie | Styrax benzoin et Styrax benzoides | |
| Île de Sumatra ; Malaisie | Styrax paralleloneurum et Styrax crotonoides | |
| Malaisie | Styrax ridleyanum | |
| Île de Sumatra | Styrax subpaniculatum et Styrax subdenticola | |
| Chine | Styrax macrothyrsus et Styrax subniveus | |
| Japon | Styrax japonicum | |
| 2 | Californie | Styrax californicus |
| Pérou | Styrax ovatus | |
| Bolivie | Styrax pearcei et Styrax aureus | |
| Amériques | Styrax reticulata et Styrax ferruginea | |
| 3 | Bassin méditerranéen | Styrax officinalis |
Aucune Styracaceae ne dispose d'appareil sécréteur résineux préformé [17]. Il s'avère donc indispensable d'en favoriser la fabrication par gemmage. En effet, les poches lysigènes ne se forment que lorsque la plante subit un traumatisme. La destruction des tissus provoque la formation de tissus ligneux de cicatrisation, riches en poches sécrétrices schizogènes qui s'accroissent par dissociation des cellules périphériques et atteignent de grandes dimensions. Ces poches communiquent avec la fente qui sépare le vieux bois normal de cette formation ligneuse néoplasique et y déversent leur contenu. Les larmes résineuses apparaissent alors à la surface des plaies et la quantité de résine sécrétée est directement proportionnelle à l'importance des traumatismes. Les canaux sécréteurs apparaissent lorsque la production pathologique de résine gagne l'écorce [18]. Ils s'anastomosent entre eux en formant des réseaux qui servent à éliminer l'excès de résine sécrétée [19,20].
Il existe trois qualités vendues de benjoin aussi bien du Siam que de Sumatra. Elles sont obtenues à différentes périodes et selon la profondeur à laquelle on fait le prélèvement sur le tronc. Plus celui-ci est profond, moins la substance est pure et claire.
Ainsi le benjoin du Siam est classé selon la grosseur et la pureté des larmes : la catégorie supérieure, dite benjoin en larmes est constituée de belles larmes isolées de grandes dimensions, d'un blanc jaunâtre à rougeâtre. Leur odeur très fine, rappelle celle de la vanille et s'accentue en vieillissant ; la catégorie moyenne, dite benjoin amygdaloïde, est constituée de blocs enfermant des larmes inégales jaune rougeâtre et d'une masse amorphe ; la catégorie inférieure, dite benjoin en masse, est surtout constituée de la gangue résineuse.
Concernant le benjoin de Sumatra, la catégorie supérieure est constituée par la résine obtenue en détachant la couche la plus externe de la production ; la catégorie moyenne provient du grattage des couches sous-jacentes jusqu'à l'écorce ; la catégorie inférieure provient du dernier raclage énergique effectué 15 jours après la première récolte. Par ailleurs, une quatrième collecte du benjoin de Sumatra conduit à une qualité inférieure appelée benjoin de Palembang.
Selon les données de la littérature, la composition chimique de ces baumes est assez voisine puisque les benjoins du Siam et de Sumatra disposent d'une fraction huile essentielle principalement constituée des acides benzoïque et cinnamique libres ou combinés sous forme d'esters [1–3]. Le benjoin du Siam peut également contenir des traces de vanilline et d'alcool coniférylique (lubanol) alors que le benjoin de Sumatra dispose de traces de benzaldéhyde, de styrène, de cinnamate de phénylpropyle et de cinnamate de cinnamyle (styracine) [12]. La différence majeure de composition se situe au niveau de la fraction terpénique puisque le benjoin du Siam contient de l'acide siarésinolique (acide 19-hydroxyoléanolique) libre ou estérifié tandis que celui de Sumatra est constitué d'acide sumarésinolique (acide 6-hydroxyoléanolique) [12].
2.2 Les styrax (et/ou storax)
Le styrax solide est produit par l'aliboufier (S. officinalis). C'est une plante des régions méditerranéennes [21] que l'on trouve à l'état spontané au Proche-Orient (Liban, Palestine), sur les rives de la méditerranée orientale à Chypre et à Rhodes mais également en Crète, en Grèce continentale et en Italie [22]. Hors de l'Europe, c'est un arbre de 6 à 7 m de hauteur et de 1 m de circonférence. En Europe, c'est un arbrisseau tortueux de 2 à 4 m de hauteur.
Les espèces qui produisent du styrax liquide font partie de la famille des Hamamelidaceae. Elles appartiennent au genre Liquidambar du latin liquidus (liquide) et de l'arabe ambar (ambre), qui signifie ambre liquide par allusion à la sécrétion de l'arbre. On distingue généralement trois principales sources de styrax selon leur répartition géographique (Fig. 2). L. orientalis est un arbre pouvant atteindre 30 m de hauteur [23]. Ressemblant au platane, il forme de vastes forêts au Proche-Orient ainsi que sur la côte sud-ouest de la Turquie [24]. L. styraciflua, du latin styracis (styrax) et fluere (écouler) est un arbre des régions méridionales des États-Unis (états de la zone atlantique de l'Amérique du Nord, Louisiane et Floride) et d'Amérique Centrale (certaines régions du Mexique, du Guatemala et du Honduras). Il ressemble à l'érable et mesure entre 15 à 20 m de hauteur, voire plus. L. altingiana est un très grand arbre de 60 m de hauteur que l'on rencontre en Indonésie (Java), en Chine et jusqu'en Australie. Les arbres du genre Liquidambar possèdent de petits nœuds sécréteurs logés dans l'écorce. Les canaux sécréteurs se trouvent, quant à eux, dans la moelle ainsi que dans les tiges des feuilles. Les traumatismes, comme l'incision du tronc, engendrent des néoformations ligneuses qui donnent naissance à des canaux anastomosés en réseau qui constituent un appareil sécréteur secondaire (poches) fournissant le baume.
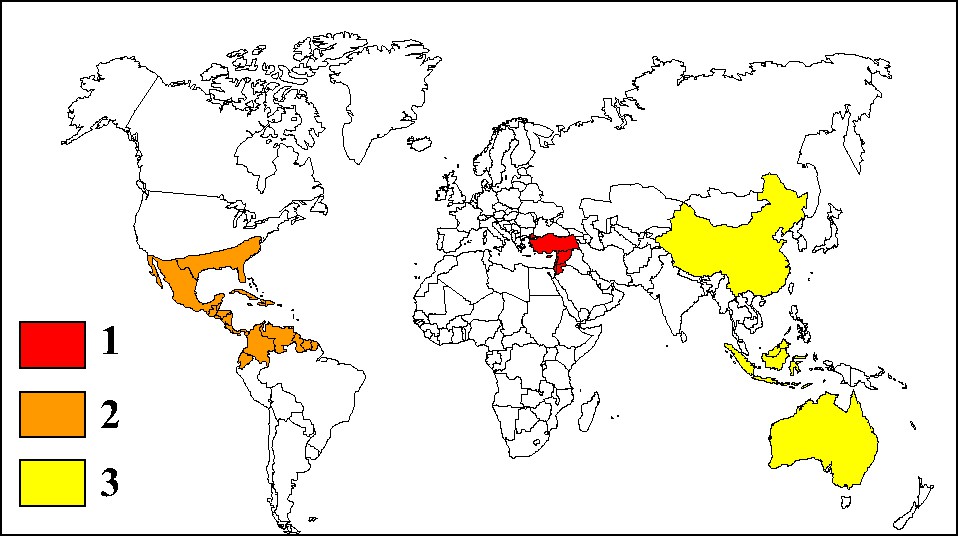
Répartition géographique des espèces botaniques appartenant au genre Liquidambar. L. orientalis (1), L. styraciflua (2), L. altingiana (3).
La meilleure qualité de storax liquide provient de L. orientalis M. C'est une substance semi-liquide ayant la consistance du miel et sa couleur est d'autant plus foncée que l'échantillon est ancien. La seconde qualité de storax provient de L. styraciflua L. et se présente sous deux formes : le storax d'Amérique liquide qui possède la consistance d'une huile épaisse et que l'on recueille directement après incisions de l'écorce de l'arbre ; le storax d'Amérique mou d'apparence opaque et blanchâtre et que l'on récupère en le retirant de l'écorce où il s'est épaissi.
La composition chimique des storax et/ou styrax liquides diffère de celle des benjoins aussi bien au niveau de la fraction volatile que de la fraction triterpénique. D'une part, ils ne contiennent pas (ou très peu) d'acide benzoïque mais essentiellement de l'acide cinnamique libre ou estérifié sous forme de cinnamate d'éthyle, de benzyle et de cinnamyle ainsi que du styrène [12], d'autre part leur fraction terpénique est majoritairement constituée par les acides oléanolique et 3-épi-oléanolique [35]. Certains auteurs évoquent même la présence de diterpènes [25].
3 Méthodologie
3.1 Matériaux résineux et molécules standards
Dans le cadre de ce travail, plusieurs échantillons résineux ont été étudiés : un benjoin du Siam, un storax de Turquie et un styrax du Honduras (les encens du monde, Asie concept, Castelnau-le-Lez, France), un benjoin de Sumatra (Okhra, Roussillon, France) ainsi que diverses résines provenant de marchés orientaux et français : un benjoin d'Indonésie de provenance inconnue, un styrax (marché d'Aubagne, France), un styrax-benjoin (marché de Sanaa, Yémen) ainsi qu'une résine étiquetée « gaoui » (marché de Djibouti).
Les développements de cette étude nous ayant amené à considérer la résine dammar, divers échantillons de cette résine ont été étudiés (Kremer, Aichstetten, Allemagne ; Roeper, Hambourg, Allemagne ; Sennelier, Saint-Brieuc, France ; Alland et Robert, Port Mort, France).
Concernant les molécules de référence (Tableau 2), plusieurs composés aromatiques ont été étudiés : l'acide benzoïque et le cinnamate d'éthyle (Fluka AG, Nuchs, Suisse), l'acide cinnamique et la vanilline (Merck, Darmstadt, Allemagne), le lubanol ou alcool coniférylique (Acros Organics, Fisher Scientific, Edmonton, Alberta, Canada) ainsi que le benzoate de coniféryle (isolé à partir du benjoin du Siam), le cinnamate de p-coumaryle (isolé à partir du benjoin de Sumatra), le benzoate de benzyle et le cinnamate de benzyle (isolés à partir du storax de Turquie). Ces quatre molécules ont été caractérisées par résonance magnétique nucléaire (RMN).
Temps de rétention tR (gradient n° 2) et longueurs d'onde d'absorption λmax des standards aromatiques
| Molécule | tR (min) | λmax (nm) |
| Lubanol | 11,7 | 212, 263, 300 |
| Vanilline | 14,3 | 228, 277, 308 |
| Acide benzoïque | 14,8 | 228, 272 |
| Acide cinnamique | 25,5 | 214, 219, 275 |
| Cinnamate d'éthyle | 43,7 | 215, 220, 276 |
| Cinnamate de p-coumaryle | 45,9 | 206, 273 |
| Benzoate de coniféryle | 46,1 | 223, 267, 305 |
| Benzoate de benzyle | 50,3 | 229, 267 |
| Cinnamate de benzyle | 54,1 | 205, 278 |
Par ailleurs, du fait d'une commercialisation et d'emplois moins répandus ainsi que de nombreux travaux déjà recensés dans la littérature spécialisée [26–30], la résine d'aliboufier ne fait pas partie de cette étude ; elle est composée d'une fraction volatile principalement constituée des acides benzoïque et cinnamique. Par ailleurs, plusieurs études ont mis en évidence la présence de benzofuranes et de saponines dans le S. officinalis L.
3.2 Matériels et méthodes
Cette étude a été réalisée par différentes techniques analytiques : la spectroscopie infrarouge à transformée de Fourier (IRTF) et la chromatographie liquide à haute performance associée à une détection à barrette de photodiodes (CLHP–UV). Ces techniques sont employées depuis plusieurs années par notre équipe pour l'étude de divers matériaux résineux de nature diterpéniques (colophane, sandaraque, etc.) ou triterpénique (oliban, mastic, etc.) [31–33].
Les analyses IR ont été réalisées sur un spectromètre Thermo Nicolet Avatar 360 FT-IR (Thermo Nicolet, Madison, Wisconsin, États-Unis) ESP (résolution : 4 cm−1, accumulations : 64) équipé d'un détecteur DTGS KBr fonctionnant avec le logiciel d'acquisition EZ OMNIC version 6.0. Les échantillons analysés étant des résines végétales naturelles, à la fois dures et élastiques, l'analyse en phase solide a été privilégiée (pastilles de KBr). Les échantillons solides sont broyés de manière homogène dans un mortier en agate avec 20 fois leur poids de bromure de potassium anhydre (Merck, Darmstadt, Allemagne). La poudre est ensuite comprimée sous une pression d'environ 10 t cm–2, avec une presse manuelle, pour former des pastilles très fines d'aspect translucide.
Le matériel chromatographique comporte une pompe à gradient ternaire Spectra-Physics SP 8 800 (Spectra-Physics, San Francisco, Californie, États-Unis), un injecteur manuel rhéodyne (Rohnert Park, Californie, États-Unis) équipé d'une boucle d'injection de 20 μL, une colonne LiChroCART Superspher (5 μm 100 RP-18 250 mm × 4 mm, Merck, Darmstadt, Allemagne) maintenue dans une enceinte thermostatée à 35 °C ainsi qu'un détecteur à barrette de photodiodes Waters 996 (Waters, Milford, Massachusetts, États-Unis). Le système fonctionne avec le logiciel d'acquisition Millennium (Waters) version 3.05.01. Une quantité de 10 à 15 mg d'échantillons résineux finement broyés est solubilisée dans 2 ml de méthanol de grade analytique (Merck, Darmstadt, Allemagne). La solution est ensuite exposée pendant 10 min dans un bain à ultrasons. Après centrifugation, le surnageant est directement injecté. Au cours de cette étude, deux gradients d'élution ont été mis au point.
Le premier (gradient n° 1), établi pour séparer les composés terpéniques, présente un mélange d'élution constitué d'acétonitrile (A) de grade analytique (Merck, Darmstadt, Allemagne) et d'eau (B) distillée millipore acidifiée à 0,01 % (pH = 3) avec de l'acide trifluoroacétique. La séparation débute par un gradient linéaire évoluant d'un mélange 60 % (A)–40 % (B) vers un éluant constitué d'acétonitrile (A) pur en 70 min. Le gradient se termine par une phase isocratique de 30 min, constituée d'acétonitrile (A) pur.
Le second (gradient n° 2), optimisé pour séparer les composés aromatiques de polarité plus importante, débute par un gradient linéaire évoluant d'un mélange 10 % (A)–90 % (B) vers un mélange 60 % (A)–40 % (B) en 50 min. La phase mobile passe ensuite à 100 % en acétonitrile (A) en 10 min avant d'observer une phase isocratique de 20 min constituée d'acétonitrile (A) pur.
4 Résultats et discussion
4.1 Résultats spectroscopiques
La spectroscopie IR associe une fréquence (exprimée en cm−1) à chaque type de vibration de liaison interatomique d'une molécule. Malheureusement, dans le cas de molécules complexes, et a fortiori dans le cas de mélanges, il est difficile d'identifier chaque bande d'absorption. Il est néanmoins toujours possible d'effectuer une comparaison d'empreintes avec une banque de données. La comparaison des spectres révèle un certain nombre de similitudes pour les benjoins du Siam et de Sumatra, ainsi que pour le storax de Turquie et le styrax du Honduras, en particulier dans la zone caractéristique des vibrations des liaisons C=C (1600– 1450 cm−1) et des déformations des liaisons C–H aromatiques (1000–650 cm−1). Cela confirme la composition chimique de ces résines, connues pour leur richesse en dérivés benzoïques et cinnamiques [34].
Les autres échantillons analysés et notamment le benjoin d'Indonésie possèdent des spectres très différents des précédents et manifestement plus proches d'une résine terpénique (Fig. 3). Une recherche comparative avec la banque de données par la méthode de corrélation (logiciel OMNIC 6.0, Thermo Nicolet) a révélé une analogie très importante (Tableau 3) entre cette substance et les autres résines provenant de différents marchés et commercialisées sous les noms de styrax ou de benjoin. Une corrélation tout aussi importante s'est révélée avec divers échantillons de résine dammar, exsudée par des arbres indonésiens appartenant à la famille des Dipterocarpaceae. La spectroscopie IR s'avère donc utile pour effectuer un tri préalable des différents échantillons, permettant de les classer en deux groupes : des baumes à caractère aromatiques et des résines terpéniques structurellement proches de la dammar.

Comparaison des spectres IRTF d'une résine balsamique et d'une résine terpénique. Benjoin du Siam (A), dammar d'Indonésie (B).
Taux de corrélation du spectre IRTF du benjoin d'Indonésie avec les spectres de diverses résines
| Échantillon | Corrélation (%) |
| Styrax (marché d'Aubagne) | 99,68 |
| Styrax-Benjoin (marché de Sanaa) | 99,31 |
| Gaoui (marché de Djibouti) | 98,24 |
| Dammar (Kremer) | 99,18 |
| Dammar (Sennelier) | 99,07 |
| Dammar (Roeper) | 98,77 |
| Dammar (Alland et Robert) | 98,54 |
4.2 Résultats chromatographiques
4.2.1 Étude avec le gradient n° 1
Tous les échantillons ont d'abord été analysés dans les conditions chromatographiques spécifiques des composés terpéniques (gradient n° 1) avec une détection UV à 210 nm, longueur d'onde de choix dans l'étude des résines terpéniques.
Les benjoins du Siam et de Sumatra ainsi que les storax de Turquie et du Honduras ne disposent pas de fraction terpénique décelable mais seulement de composés aromatiques rapidement élués (Fig. 4). Pourtant, les données de la littérature décrivent la présence de triterpènes de type oléanane [12,35] au sein de ces baumes : les acides 6-hydroxyoléanolique (acide sumarésinolique) et 19-hydroxyoléanolique (acide siarésinolique) dans les benjoins de Siam et de Sumatra [12] ainsi que les acides oléanolique et 3-épi-oléanolique dans le storax de Turquie [35]. Il est donc fortement vraisemblable que les échantillons en notre possession ne soient pas les résines brutes mais des produits d'extraction (huiles essentielles, obtenues par des techniques de type entraînement à la vapeur ou par une technique de récolte de la résine incluant un processus de décoction des écorces).
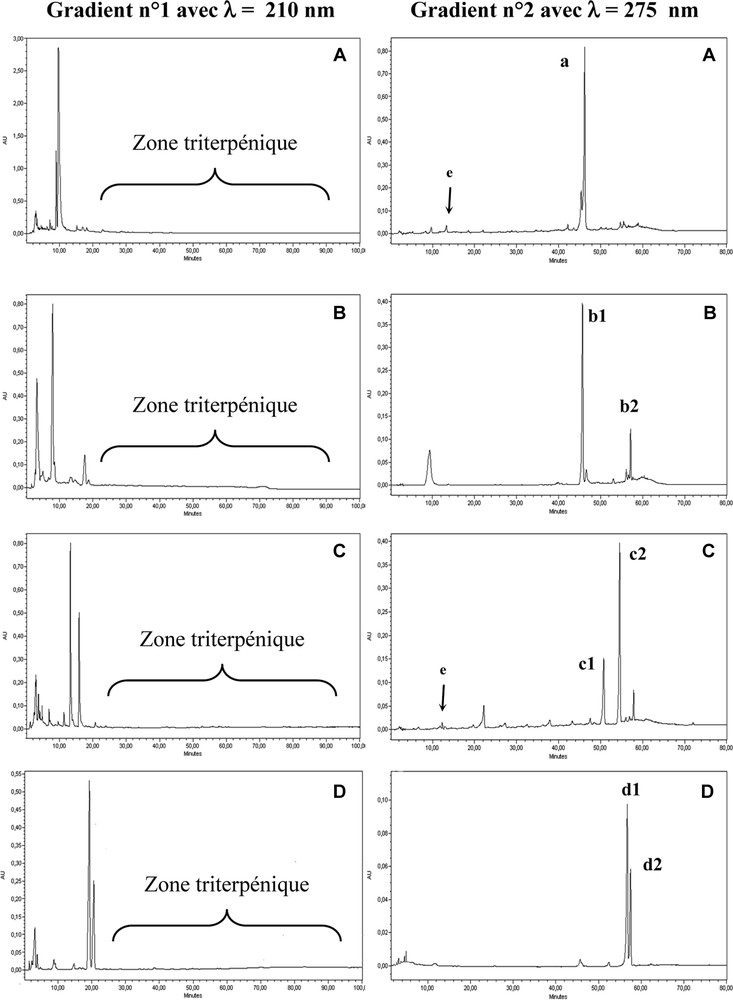
Chromatogrammes CLHP–UV des quatre baumes étudiés. Benjoin du Siam (A), benjoin de Sumatra (B), storax de Turquie (C), styrax du Honduras (D).
En outre, les chromatogrammes des autres échantillons styrax et benjoins ne révèlent pas la présence de composés aromatiques, comme l'a confirmé leur étude avec le gradient n° 2. En revanche, une comparaison d'empreintes chromatographiques avec une banque de données a montré que ces différentes résines, malgré leur dénomination de styrax ou de benjoin, présentent une composition triterpénique très proche de celle des dammars étudiées (Fig. 5), corroborant ainsi les corrélations observées par spectroscopie IR.
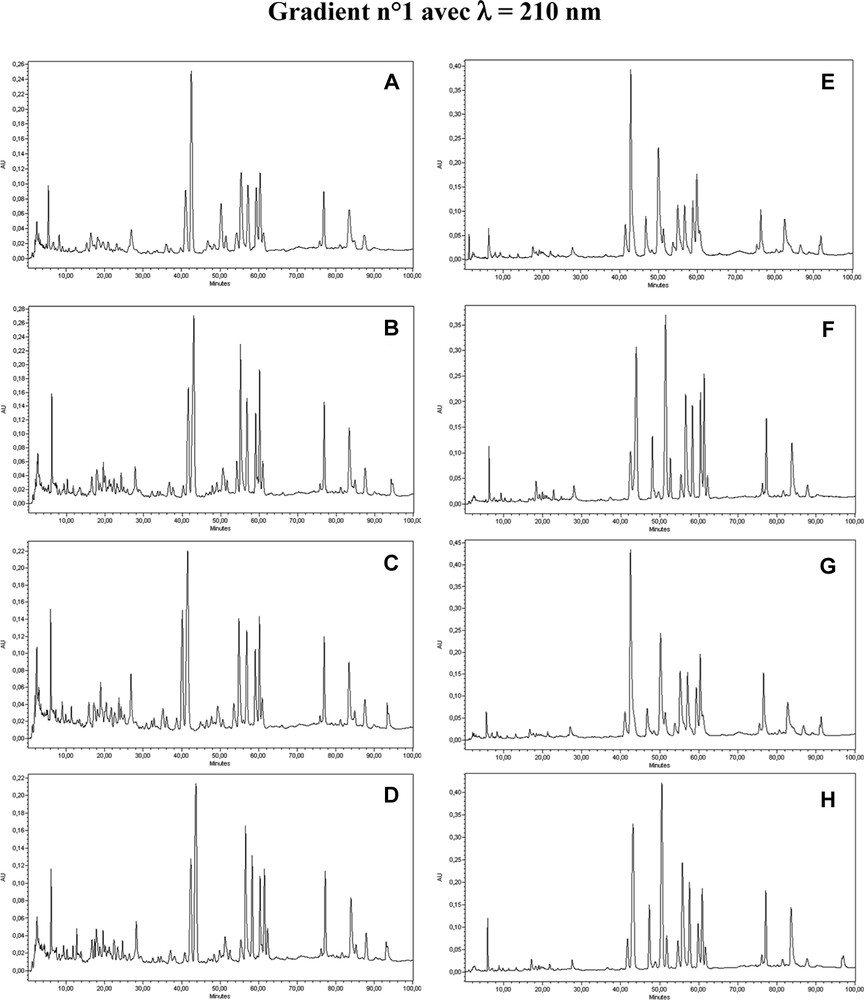
Comparaison des chromatogrammes CLHP–UV des divers échantillons de marchés et des résines dammar. Benjoin d'Indonésie (A), styrax-benjoin (B), styrax (C), gaoui (D).
Dammars : Kremer (E), Roeper (F), Sennelier (G), Alland et Robert (H).
Pourtant, si la dammar est bien une résine triterpénique provenant des mêmes régions du Sud-Est asiatique (Indonésie, Malaisie, Inde, etc.), elle provient d'arbres qui n'appartiennent ni au genre Styrax, ni au genre liquidambar mais aux genres Pterocarpus, Shorea, Hopea et Balanocarpus (famille des Dipterocarpaceae). Par la-même, elle présente une composition chimique complètement différente et largement étudiée. Ses principaux constituants (22-hydroxyhopanone, acide dammarénolique, hydroxydammarénone, dammarènediol, dammaradiénol, dammaradiénone, aldéhyde oléanolique, aldéhyde oléanonique, acide oléanonique, aldéhyde ursolique, aldéhyde ursonique et acide ursonique) ont d'ailleurs été caractérisés [36–39].
4.2.2 Étude avec le gradient n° 2
Les échantillons ne disposant pas de composés terpéniques ont été étudiés (Fig. 4) dans les conditions chromatographiques optimisées pour les composés aromatiques (gradient n° 2) avec une détection UV à 275 nm, principale longueur d'onde permettant la détection dans l'acétonitrile des chromophores cinnamiques et benzoïques.
Parmi les échantillons étudiés, seuls les benjoins du Siam et de Sumatra ainsi que le storax de Turquie et le styrax du Honduras contiennent des composés absorbant à cette longueur d'onde (Fig. 6). Toutefois, les acides cinnamiques et benzoïques libres n'ont pas été détectés.

Spectres UV des principaux dérivés aromatiques.
Le principal constituant du benjoin du Siam est le benzoate de coniféryle (composé a, tR = 46,1 min). Ce résultat est conforme à la majorité des données de la littérature [3,12]. Bien que certains auteurs [40] aient décrit le benzoate de benzyle (composé c1, tR = 50,3 min) comme composé majeur du benjoin du Siam, aucune trace de ce dernier n'a été détectée dans ce travail. Le benjoin de Sumatra présente à un temps de rétention quasi-identique (tR = 45,9 min) à celui du benzoate de coniféryle, un composé isolé et caractérisé par RMN comme étant le cinnamate de p-coumaryle (composé b1) ; ce dernier est décrit comme principal ester aromatique de l'espèce S. paralleloneurum à la différence de S. benzoin qui n'en contient que des traces [3].
Les storax de Turquie et du Honduras possèdent quant à eux des composés aromatiques différents de ceux rencontrés dans les benjoins précédemment évoqués. Le storax de Turquie contient du benzoate de benzyle (composé c1, tR = 50,3 min) et du cinnamate de benzyle (composé c2, tR = 54,1 min) contrairement aux benjoins précédemment cités. Néanmoins, il est intéressant de noter la présence uniquement au sein du storax de Turquie et du benjoin du Siam d'un composé (e) ayant le même spectre UV que la vanilline (Fig. 7) mais un temps de rétention différent de cette dernière (tR = 12 min pour e et tR = 14 min pour la vanilline). Il semble donc que ces échantillons contiennent un dérivé vanillique isomère de celui habituellement décrit dans la littérature. Enfin, nos investigations mettent en évidence un constituant à tR = 57,8 min (composé b2, Fig. 4) au sein du benjoin de Sumatra et un analyte à tR = 58 min (composé d1, Fig. 4) dans le styrax du Honduras dont les spectres UV sont superposables. Il s'agit vraisemblablement d'un même composé, commun à deux baumes exsudés par des espèces botaniques différentes, dont l'existence pourrait, sur le plan chimique, justifier les diverses confusions souvent réalisées.
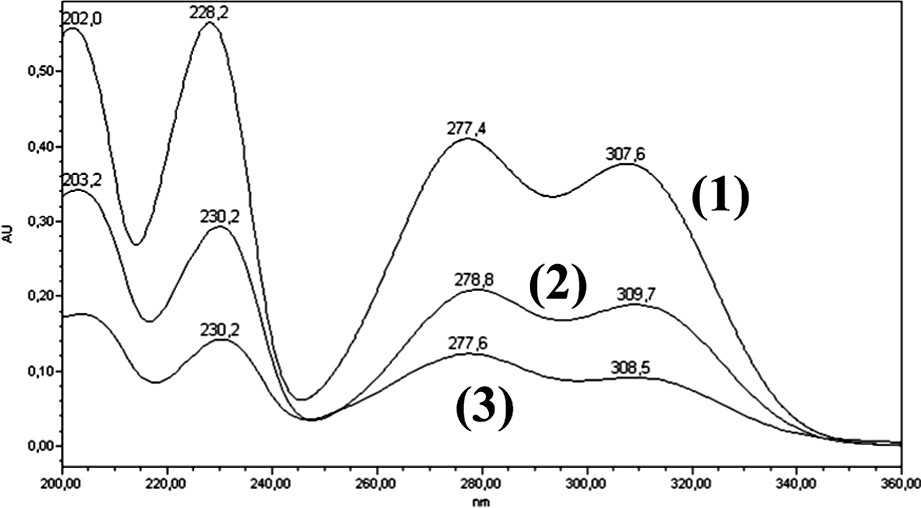
Superposition des spectres UV de la vanilline tR = 14,3 min (1) et des composés à tR = 12,1 min (benjoin du Siam) (2) et à tR = 11,8 min (storax de Turquie) (3).
5 Conclusion
L'étude des différentes résines benjoin, styrax et/ou storax se révèle des plus complexes aussi bien sur le plan de la terminologie que sur le plan chimique.
Contrairement aux données de la littérature, les exsudats commerciaux, constitués de dérivés aromatiques, ne disposent pas de terpènes ou tout du moins n'en contiennent que des traces non détectables en UV. Ces échantillons ne seraient donc pas des baumes stricto sensu, mais il pourrait s'agir de produits d'extraction. L'analyse chromatographique permet de les différencier et d'identifier certains constituants caractéristiques.
Par ailleurs, plusieurs échantillons vendus comme benjoins et/ou styrax, sont en réalité de la dammar. Il ne s'agit pas d'un problème ponctuel puisque cela concerne plusieurs substances vendues sur différents marchés orientaux et français. Il est cependant difficile de préciser s'il s'agit d'adultérations ou de confusions intervenant lors de la récolte.
Bien que parfois employé pour désigner à tort des résines triterpéniques de type dammar, le terme benjoin doit se limiter à des matériaux résineux originaires d'Extrême-Orient, comme ceux du Siam et de Sumatra. L'appellation plus générale de styrax-benjoin peut également convenir à ces deux baumes dans la mesure où les espèces désignées proviennent du genre Styrax. La terminologie storax reste la plus adéquate pour désigner les résines exsudées par des arbres du genre Liquidambar. La dénomination est donc justifiée dans le cas du storax de Turquie mais devient source de confusion pour l'échantillon styrax du Honduras.
L'outil analytique contribue donc à mieux cerner la composition chimique de résines naturelles complexes d'origine végétale. Il renseigne également sur les modes d'obtention ou de transformation de certaines matières premières tout en apportant parfois de précieuses informations sur l'appartenance botanique de certaines substances à l'origine de nombreuses interrogations.
Remerciements
Les auteurs remercient le conseil régional Provence–Alpes–Côte d'Azur et l'atelier de conservation et de restauration d'œuvres d'art Amoroso-Waldeis (Avignon, France) pour le cofinancement de ces travaux de recherche ainsi que le Dr Gérald Culioli, de l'université du Sud, Toulon, Var, pour sa précieuse contribution dans l'identification des structures chimiques par résonance magnétique nucléaire.


