1 Introduction
En 1998, Sornette en collaboration avec Johansen et Bouchaud [1,2] a rendu compte par des lois log-périodiques de l’évolution des indices économiques S et P 500 et avec Johansen [3] de celle des indices Nikkei et Dow Jones. Ces lois trouvent leurs origines du « groupe de renormalisation », d’où « des lois puissance » présentant des corrections log-périodiques. Ces résultats sont présentés et analysés théoriquement dans le livre de Sornette [4]. De son côté, en 1998, Nottale, publiait La théorie de la relativité d’échelles [5], théorie fort complexe qui se veut une généralisation moderne des théories de la relativité. Dans le cadre de sa théorie, il propose de ne pas accepter la differenciabilité systématique de l’espace–temps continu, mais que celui-ci soit fractal. En conséquence, les lois de la physique sont valables à toutes les échelles ce qui conduit à l’unification des lois quantiques et classiques. Il a montré, toujours dans le même cadre théorique, que les arbres des évolutions ont donc une structure fractale log-périodique. Par la suite, dans une série d’articles, il précisait sa théorie et analysait avec Chaline et al. et Grou et al. [6] les évolutions log-périodiques de diverses espèces (hominidés, équidés, rongeurs…), ainsi que la chronologie des crises économiques depuis 10 000 ans dans le monde Occidental et l’Amérique Centrale. Précédemment, pour notre part, dans le but plus modeste d’apporter de nouvelles confirmations des propositions de Nottale dans des domaines fort différents de ceux explorés, nous avons mis en évidence trois autres log-périodicités : celle de la musique Jazz ainsi que celle des Ordres religieux et monastiques [7] et, en collaboration avec Baron [8], celle de l’évolution des accélérateurs de particules de haute énergie utilisés en physique nucléaire et corpusculaire. Suivant la même idée, nous nous proposons ici de vérifier si la chronologie, au cours des siècles, des découvertes des éléments chimiques suit également une loi log-périodique. En conséquence nous allons établir cette chronologie après avoir donné les principales équations qui structurent cette loi.
2 Loi log-périodique
La log-périodicité permet de comprendre des systèmes critiques dont l’évolution est régulière, mais avec un rythme coupé par des accélérations notables. Celles-ci sont à l’origine de bifurcations vers des évolutions secondaires si on fait l’analogie avec le point de départ des branches pour les arbres végétaux. Le formalisme et les justifications d’une telle loi sont bien détaillés par Nottale, Chaline et Grou (nommés plus loin NCG) dans les différents articles [6].
Les embranchements au cours d’une évolution se succèdent à des instants Tn tels que
À l’aide des valeurs Tc et g on calcule la valeur de l’instant Tn + 1 de rang n + 1 connaissant l’instant Tn de rang n :
Une conclusion notable de ce simple modèle est, s’il est vérifié, d’affirmer qu’il est possible de prédire approximativement les dates des étapes d’une chronologie dont on connaît les ingrédients g et Tc, mais seulement les dates et non leurs causes et leurs conséquences. Cette prédiction est possible à partir de la quatrième date, mais la connaissance de trois dates et donc de deux intervalles permet une première estimation de g et de Tc. La principale question posée est de comprendre l’origine d’une telle loi d’arborescence fractale.
3 Historique de la découverte des éléments chimiques
La Fig. 1 donne le nombre cumulé des éléments chimiques découverts depuis 1750 à nos jours. Comme nous l’avons déjà montré en collaboration avec Bernas [9], la courbe représentant ce nombre croît régulièrement, mais avec des ressauts dus à l’accélération du rythme des découvertes. L’amorce de chacune de ces accélérations correspond à l’arrivée d’une ou de plusieurs nouvelles techniques qui relancent la recherche de nouveaux éléments. Cette recherche s’effectue avec la ou les techniques innovantes, mais aussi à l’aide des techniques « classiques » qui souvent ont été très largement perfectionnées entre temps. Par analogie avec les arbres végétaux, on peut considérer ces accélérations comme des embranchements marquant le démarrage d’une nouvelle voie de recherche. Mais, après chaque accélération, le rythme des découvertes se ralentit jusqu’à une pause que viennent interrompre les innovations suivantes. Ces pauses confirment un certain épuisement de la créativité : par exemple, entre 1830 et 1860 seulement quatre éléments sont découverts, alors qu’entre 1860 et 1890 il y en a 15 ! Ce comportement de l’évolution des découvertes des éléments est à rapprocher du modèle des « équilibres ponctués » qu’ont proposé Gould et Eldredge pour expliquer l’évolution des espèces [10].
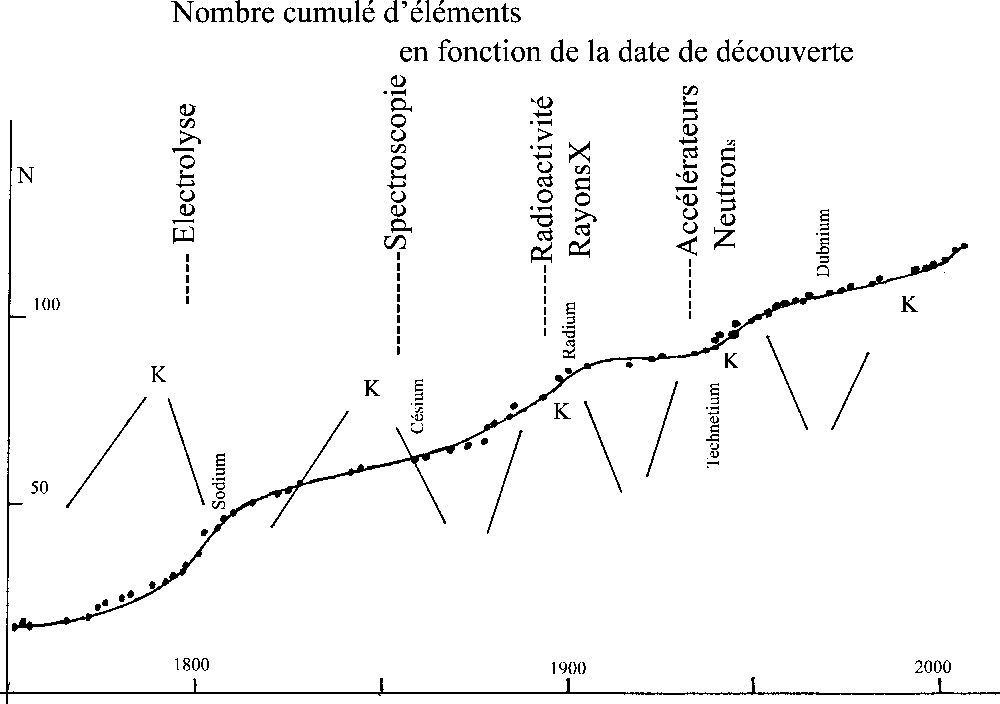
Nombre cumulé d’éléments chimiques connus en fonction de la date de leur découverte. Les cycles de Kondratiev sont superposés avec leurs maxima K. Le premier élément de chaque cycle est indiqué ainsi que les innovations à l’origine d’un cycle.
Sur la même figure, nous avons tracé schématiquement les cycles économiques de Kondratiev. Il est remarquable de constater que les techniques novatrices apparaissent aux environs des périodes de récession confirmant dans notre cas particulier l’affirmation de Schumpeter sur le rôle des innovations[11] qui relancent les activités économiques et sociales. En outre, on peut décomposer la courbe de la figure en une somme de courbes « logistiques » montrant qu’il y a eu diffusion des techniques innovantes au cours des siècles.
Au cours de l’Antiquité, seuls neuf éléments chimiques furent connus (carbone, or, argent, cuivre, soufre, étain, plomb, mercure, fer). Puis l’arsenic, l’antimoine, et le zinc et le phosphore sont identifiés, respectivement, aux xiiie, xve, xviie siècles, soit, au total, 13 éléments seulement. Évidement les notions d’atomes, de molécules et d’éléments sont alors ignorées. On confond corps composés et éléments simples. Aucune recherche sérieuse n’apparaît à cette époque où l’alchimie, la magie dominent en Occident jusqu’au xviie siècle.
Au siècle suivant, celui des « Lumières », tout change comme changent les sociétés, et cela très rapidement. Stahl en 1719 avance la notion de phlogistique, une idée fausse, mais qui, en revanche, stimula durant 50 ans la réflexion des chercheurs et orienta les études vers l’expérimentation, principalement l’oxydoréduction. Ces études vont mener à la découverte d’un grand nombre d’éléments (20) au cours de ce siècle. Le premier est le cobalt (Brand en 1737). Dans le conflit qui l’oppose aux tenants de la phlogistique, ces résultats vont favoriser la victoire de Lavoisier et de ses idées. Dès lors, il est généralement admis que c’est ce dernier qui a fait de la chimie une vraie Science.
Au départ du cycle suivant, en 1800, Volta invente la pile électrique. Grâce aux générateurs de courants continus qui en découlent, c’est la naissance de l’électrochimie et en particulier celle de l’électrolyse. Aussi, dès 1806, grâce à celle-ci, Davy découvre le sodium puis le potassium avant le calcium et le baryum… En 1860, nouvelle technique : la spectroscopie optique ; elle est utilisée par Bunsen et Kirchoff pour détecter de nouveaux éléments : le césium et le rubidium, le thallium… Pour ces investigations, une aide précieuse fut apportée en 1869 par Mendeleïev qui publia le tableau portant son nom et qui, à l’époque, ne contenait que 63 éléments connus. Les cases vides et les informations déduites de ce tableau ont permis par la suite de guider les chimistes dans leurs recherches.
La fin du xixe siècle marque l’éclosion de la physique moderne : parmi des découvertes fondamentales, la radioactivité est mise en évidence par Becquerel (1896). Cette propriété est un outil (comme la spectroscopie) pour déterminer la présence d’éléments inconnus que l’on sépare par les techniques traditionnelles ou innovantes d’entraînement par affinités chimiques. Rapidement, le radium et le polonium sont annoncés par M. et P. Curie en 1898. Bien d’autres éléments radioactifs seront connus ultérieurement. Peu auparavant, en 1895, Roentgen avait mis en évidence les rayons X dont les fréquences purent être reliées aux numéros atomiques, c’est-à-dire à l’identification de l’atome (Moseley). En 1929, un nouvel instrument destiné à la physique nucléaire, le cyclotron, est imaginé à Berkeley par Lawrence avant que par la suite Chadwick (Grande-Bretagne) ne montre l’existence des neutrons dont les propriétés sont aussitôt étudiées et exploitées. Dès lors les neutrons et les cyclotrons deviennent les outils obligatoires pour obtenir de nouveaux éléments à l’aide de réactions nucléaires. En cherchant à réaliser une capture neutronique par des atomes, suivie d’une désintégration bêta (émission d’un électron qui change le nombre atomique), E. Fermi tente de réaliser à partir de 1934 la synthèse de noyaux. Mais, c’est le technétium qui est le premier élément fabriqué artificiellement à la suite de l’interaction d’un faisceau de deutons avec une cible de molybdène (Perrier et Segré en 1937). Par la suite, plusieurs éléments sont produits par réactions neutroniques dans des réacteurs nucléaires (premiers éléments transuraniens) et, même, dans des explosions thermonucléaires (einsteinium et fermium).
À partir des années 1950, les découvertes sont surtout faites à l’aide d’accélérateurs de plus en plus sophistiqués, améliorées dans le cadre de la concurrence sans merci entre un petit nombre de grands laboratoires russe, américain et, plus récemment, allemand (principalement JIRN-Doubna, LBL-Berkeley et GSI-Darmstadt qui se partagent les découvertes). Après les réactions nucléaires induites par particules légères, des ions plus lourds (C, N, O, Na…) sont utilisés. À partir de 1981, Doubna et Darmstadt misent sur la technique de « fusion froide ». Enfin, au cours des années 2000, Doubna revient à la « fusion chaude » mais avec des procédés différents : des projectiles très lourds et riches en neutrons, les Ca48, sur des cibles d’isotopes, riches en neutrons, du plutonium, américium, curium et californium. Avec ce mode opératoire, la collaboration entre Doubna et le laboratoire Lawrence de Livermore aux États-Unis, a débouché sur l’obtention des propriétés de nouveaux éléments de numéro atomique allant jusqu’à Z = 118 (en attente de confirmation par les autorités scientifiques internationales). Ces données historiques ont été extraites de différents sites Internet, des références [12,13]. Des communications privées m’ont été très utiles.
4 Discussion et conclusion
À partir de la Fig. 1 on peut proposer dans la Fig. 2 un arbre généalogique décrivant le déroulement historique de la découverte des éléments avant 1929. L’application des équations de la log-périodicité à cet arbre généalogique (en se limitant, donc, aux innovations bien datées et antérieures à 1929) conduit par optimisation aux quantités suivantes :
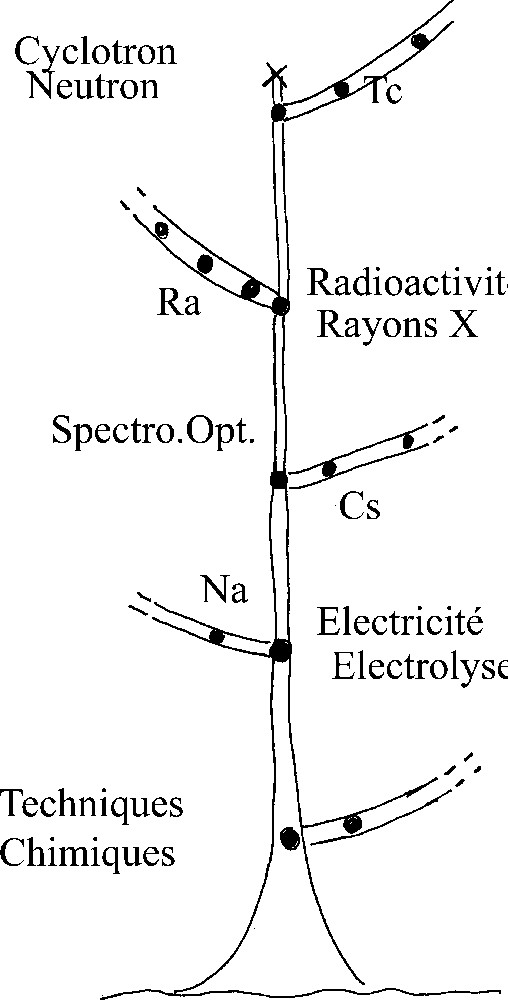
Arbre généalogique de la découverte des éléments chimiques. Le premier élément de chaque branche a été porté.
Toujours à l’aide de l’équation (I), il est aisé de calculer les dates des innovations qui ont dû suivre, soit : 1959 ± 3, 1982 ± 4, 2000 ± 5. Au regard de l’historique précédent on constate que ces moments correspondent respectivement à :
- • la technique innovante qu’est l’utilisation des accélérateurs à ions lourds (nouveaux outils à l’époque) ; jusqu’alors seuls les ions légers protons, deutons, alphas servaient de projectiles. Le nobélium et le lawrencium sont connus ainsi ;
- • la « fusion froide » adoptée à Doubna et à Darmstadt (bohrium…) ;
- • la « fusion chaude », choisie, toujours à Doubna, pour atteindre les noyaux jusqu’au numéro atomique Z = 118.
Ainsi, l’accord est très satisfaisant pour ces trois dates non introduites dans le calcul de g et Tc et doit être souligné comme une preuve supplémentaire de la validité de la loi log-périodique appliquée à la découverte des éléments chimiques.
Dans l’avenir, au moyen de l’équation (I) on peut prévoir l’arrivée de nouvelles innovations vers 2014 ± 5, sans prévoir leur nature et leurs impacts ! C’est une date très proche et nous pourrons, alors, vérifier la validité des hypothèses et des ingrédients utilisés. Dès maintenant des projets existent pour concevoir de nouvelles techniques (en particulier des systèmes d’identification des produits de réactions…).
Autre argument : nous avons signalé plus haut que l’apparition des innovations scientifiques, qui relancent les cycles de découverte de nouveaux éléments, coïncide avec les cycles économiques dits de Kondratiev. Or, Grou, Chaline et Nottale [6] ont montré que la chronologie des crises économiques sur des siècles, incluant les crises de ces cycles, suit une loi log-périodique dont les paramètres caractéristiques sont Tc = 2080 ± 30 et g = 1,32 ± 0,02. Il y a donc un très bon accord entre ces résultats et les nôtres qui ont été obtenus à partir de données totalement différentes (Tc = 2055 ± 25). Cet accord peut être considéré comme une nouvelle validation de la théorie de Nottale.
NCG [6] ont proposé que l’accélération dans un processus d’évolution pouvait être expliquée par un effet de mémoire. La connaissance du passé permet au processus de gagner du temps à chaque étape de l’évolution, gain qui est mesuré par le paramètre d’autosimilarité g. Donc si l’effet mémoire est important, la valeur de g est grande. Effectivement, nous avons observé dans l’évolution log-périodique des ordres religieux [14] un paramètre g voisin de 2. Or, cette évolution s’effectue toujours dans le cadre défini par les textes sacrés dont la Bible. On peut admettre que les innovations qui marquent les étapes de ce processus sont certes importantes mais moins fondamentales, moins bouleversantes que, par exemple, les innovations qui jalonnent l’évolution économique des sociétés (voir NCG) ou l’évolution des techniques chimiques où tout est remis en question.
Tous les éléments découverts depuis l’uranium jusqu’à l’élément de numéro atomique Z = 118 sont instables (radioactifs) et n’existent pas dans la nature. Ils ont des durées de vie courtes, d’autant plus courtes (parfois des millisecondes ou des fractions de millisecondes) que les nombres atomiques de ces éléments augmentent. Cependant, les dernières données obtenues pour les éléments de Z = 110 à 118 sont en faveur d’un « îlot de stabilité des noyaux super lourds » prévu par les théoriciens et recherché depuis des décennies [15]. En conséquence, ces résultats permettent d’espérer que la recherche des noyaux super lourds va se poursuivre avec succès. L’existence de l’îlot des super lourds étant confirmée, un nouveau domaine scientifique s’ouvre pour déterminer les propriétés de ces noyaux.
Il faut souligner l’augmentation considérable de la complexité (au sens spécifique de la physique) dans les méthodes expérimentales adoptées depuis l’époque de Lavoisier jusqu’à aujourd’hui : au début, une simple réaction chimique d’oxydoréduction était réalisée sur une table banale avec de simples récipients et du feu. L’électrolyse a nécessité d’avoir du courant continu ; la spectroscopie a exigé des instruments d’optiques très travaillés et maintenant, il faut des accélérateurs puissants, dédiés à ces recherches, des détecteurs sophistiqués et un personnel scientifiques très nombreux, sans oublier des moyens financiers considérables.
En considérant l’histoire de ces découvertes, il est possible de dire que l’emploi de techniques de plus en plus poussées a permis des « gains de productivité » dans ce domaine comme on en obtient en économie. De tels gains ont été nécessaires pour aboutir aux performances actuelles : détecter la présence de quelques noyaux radioactifs d’une vie inférieure à la microseconde. Que l’on songe qu’un siècle auparavant, le hasard seul a fait découvrir la radioactivité !
Au cours des siècles concernés, les lieux de découvertes se sont déplacés. Au début, il s’agissait de pays européens, assez nombreux : France, Grande-Bretagne, Allemagne, Scandinavie. Au fur et à mesure le nombre de centres de recherche s’est réduit pour se limiter actuellement à trois (peut-être un seul ?), mais avec des collaborations internationales. Là aussi un effet d’échelles est visible. Toutes ces remarques concernant le présent sujet ont déjà été notées par NCG et plaident pour un système log-périodique qu’elles caractérisent.
Pour se relier encore plus aux travaux de NCG, notons qu’apparaissent toujours dans nos analyses l’action du hasard (exemple typique : la découverte de la radioactivité par Becquerel) et la contingence (exemple typique : la pile de Volta est arrivé au moment où la classe bourgeoise prend le pouvoir en France et que Napoléon adapte en conséquence l’économie dans ce pays et en Europe). Ce sont les effets du « hasard contraint » [16] qui façonnent la chronologie des découvertes.
À partir de tous les arguments précédents, on ne peut que conclure que la chronologie étudiée ici suit un parcours très voisin des chemins empruntés par toutes les évolutions analysées précédemment par NCG ou nous-mêmes avec cette succession de sauts majeurs, de mutations mineures et de stagnations. Cette universalité (dite du troisième type) suggère dans beaucoup de domaines un mécanisme sous-jacent mais imparfaitement compris comme celui qu’évoque Sapoval [17] dans l’exemple de « l’agrégation limitée par la diffusion » où le hasard contraint aboutit non au désordre mais à l’ordre. Terminons en rappelant la définition donnée par ce chercheur :
« L’universalité est la manifestation d’une structure mathématique sous-jacente commune à des phénomènes ou à des situations physiques apparemment différents ».
Remerciements
Je tiens à remercier mes deux collègues de l’université Paris-Sud, Monique Bernas qui a longtemps séjourné à Darmstadt et Michel Hussonnois qui, fort amicalement, m’a transmis de nombreuses précisions sur les recherches des noyaux super lourds auxquelles il a participé à Doubna durant de nombreuses années. Je suis fort reconnaissant à Robert Guillaumont (Académie des Sciences) pour sa disponibilité, ses commentaires et, surtout, ses critiques fort constructives.


