Pourquoi Louis Pasteur (1822–1895) est-il passé de ses études initiales de cristallographie, mesurant la rotation du plan de polarisation de la lumière après la traversée de cristaux ou de solutions, aux explorations des fermentations, qui l’ont ensuite conduit aux études de microbiologie ? Dans un article précédent [1], les travaux de Pasteur sur le dédoublement des acides tartriques et des tartrates ont été analysés à partir de tous ses articles scientifiques (initiaux, et comparés aux rééditions ultérieures, notamment dans des recueils de ses œuvres) : il a été montré comment Pasteur était l’héritier scientifique direct de Jean-Baptiste Biot (1774–1862) et d’Auguste Laurent (1807–1853), et comment il avait bénéficié des idées fondatrices de ce dernier, qui était son « tuteur » dans le laboratoire d’Antoine-Jérôme Balard (1802–1876).
Dans le présent texte, le projet est différent, et double : toutes les publications et notes de Pasteur, de 1848 à 1880, sont utilisées en vue d’une meilleure compréhension de la transition entre ses travaux de cristallographie et ses études des fermentations, qui marquent la fin de la période considérée dans ce texte ; toutes ne sont cependant pas citées, car une telle étude a été faite par Flack [2].
Est analysée ici l’évolution d’une pensée scientifique, pour un homme qui a inspiré des hagiographes tout autant que des détracteurs, certains d’entre eux oubliant que les hypothèses, idées et théories que les scientifiques utilisent opérationnellement évoluent lentement, parfois contradictoirement, à mesure que les résultats d’expérience s’ajoutent. L’histoire de cette évolution et celle des progrès de la théorie atomique sont mises en correspondance, afin de comprendre comment Pasteur a « réussi à tracer un chemin de certitudes au travers de grandes incertitudes », ce qui, pour Debru, « est la définition même de la science expérimentale moderne » [3]. Des citations (en italiques) sont données, dans la mesure où elles montrent les idées de Pasteur plus fidèlement que des commentaires de ses textes. De nombreux termes utilisés par Pasteur et ses contemporains, quand ils sont cités ici, sont placés entre guillemets, afin que ne leur soit pas attribuée une acception moderne, qui serait anachronique ou indue. Enfin une synthèse est faite entre des hypothèses concurrentes, à propos de l’évolution des recherches de Pasteur, de la cristallographie vers la biochimie et la microbiologie.
Ajoutons que, pour ces analyses, ne sont donnés ici que des extraits des publications les plus saillantes, car Pasteur se répète beaucoup. Sauf exception, les publications sont évoquées dans un ordre chronologique, afin de bien séparer les faits — établis à partir des publications essentiellement à l’Académie des sciences — et les idées données dans des textes publiés postérieurement (par Pasteur ou par ses historiens) et qui faussent évidemment l’appréciation de la pensée de Pasteur au moment où il fait ses travaux. A propos des notions d’atomes et de molécules, des anachronismes ont été évités, la discussion détaillée de l’évolution des idées de Pasteur à ce propos étant effectuée dans [1] ; toutefois des observations relatives à ces notions continueront de s’imposer quand elles permettront de mieux comprendre la pensée de Pasteur à l’époque où il fait ses travaux et de mieux percevoir les raisons de son changement d’orientation scientifique.
1. Les acides tartriques et les composés organiques
L’étude dont les résultats sont donnés ici commence avec la publication du 22 mai 1848 [4], qui correspondait à l’annonce, à l’Académie des sciences, de la découverte à laquelle Pasteur se référera souvent : l’ « acide racémique », découvert par l’industriel alsacien Charles Kestner (1803–1870), était un mélange de deux énantiomères (c’est la terminologie moderne pour désigner des composés dont les molécules sont images l’une de l’autre dans un miroir) de l’ « acide tartrique » (ou acide 2,3-dihydroxybutanedioïque) ; ces composés sont aujourd’hui désignés par (2R, 3R), ou (+), et par (2S, 3S), ou (−) [1].
Pasteur était sorti de l’École normale supérieure deux ans plus tôt, et Balard l’avait accueilli dans son laboratoire, où travaillait Laurent, qui s’était mis en disponibilité de son poste de professeur de chimie de l’Université de Bordeaux [5, 6]. Les contributions de Laurent aux travaux initiaux de Pasteur — et notamment au résultat de 1848 — furent essentielles : Laurent enseigna à Pasteur à utiliser conjointement la cristallographie et la mesure de l’activité optique (c’est-à-dire la mesure de la rotation du plan de polarisation de la lumière, quand cette dernière traverse des cristaux ou des solutions). Mieux encore, Laurent fournit à Pasteur les cristaux que ce dernier analysa [1]. Pourtant Laurent ne fut pas cité dans l’article décrivant le dédoublement des tartrates, ce qui le conduisit à adresser aux Comptes rendus de l’Académie des sciences, quelques semaines après la publication de la découverte des deux acides tartriques (+) et (−), un article où il signalait ses apports [7] (dans les évocations ultérieures des travaux ayant conduit au dédoublement des tartrates, Pasteur ne cita que rarement Laurent, et il y a lieu de s’en étonner).
Les principaux scientifiques qui avaient préparé la découverte annoncée le 22 mai 1848 étaient René Just Haüy (1743–1822), Louis-Joseph Gay-Lussac (1778–1850), Carl Scheele (1742–1786), Kestner, François Arago (1786–1853), Eilhard Mitscherlich (1794–1863), Biot et Laurent [1]. L’acide tartrique (+) avait été étudié depuis 1769, et la découverte par Kestner de ce qui fut nommé « acide paratartrique », ou encore « acide thannique » (il avait été découvert à Thann, en Alsace), en 1822, fut évidemment cruciale pour l’identification de deux des trois isomères de l’acide tartrique (voir la Figure 1) : plus précisément, pour son étude, Pasteur fit usage de techniques d’étude de l’orientation des faces des cristaux par des techniques initialement mises au point par William Hyde Wollaston (1766–1828) et par Biot, ainsi que de mesures de la rotation du plan de polarisation de la lumière, mises au point par Biot, sur la base de découvertes d’Étienne-Louis Malus (1775–1812) et d’Arago.
Les deux isomères optiquement actifs (2R-3R) et (2S-3S) de l’acide tartrique, ou acide 2,3-dihydroxybutanedioïque. Ici comme dans les autres figures, les représentations sont modernes, car, dans les années 1850 et 1860, quand Pasteur étudia ces composés, les chimistes n’avaient généralement pas d’idée géométrique ou stéréochimique de la forme des « molécules », entités qui étaient alors souvent confondues avec des « atomes » ; ces entités ne correspondaient pas aux objets que nous désignons sous ce nom [2]. Pasteur [8] et ses contemporains, après la découverte de la « dissymétrie moléculaire » de ces deux acides tartriques (sur trois isomères de l’ « acide tartrique »), nommaient ces derniers « acide lévoracémique » et « acide dextroracémique ».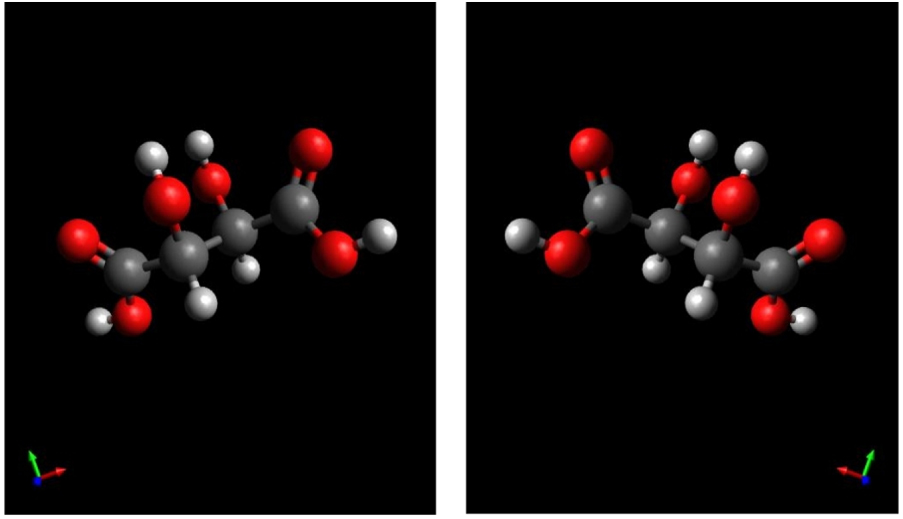
Après Biot, Pasteur répéta que les composés organiques étaient plus fréquemment actifs optiquement que les composés minéraux [9] : « Chacun sait, en effet, depuis les belles et nombreuses recherches de M. Biot, que beaucoup de substances organiques jouissent de la propriété singulière de dévier à l’état de dissolution le plan de polarisation des rayons lumineux ». Il organisa ses études autour de cette idée.
Cette époque était antérieure de plus de dix ans au premier congrès international des chimistes, que Friedrich August Kekulé (1829–1896), Charles Adolphe Würtz (1817–1884) et Karl Weltzien (1813–1870) organisèrent à Karlsruhe et où Stanislao Cannizzaro (1826–1910), reprenant des idées d’Amadeo Avogadro, fit circuler un mémoire qui proposait une définition claire des notions d’atomes et de molécules. En revanche, en 1848, ces notions étaient très indistinctes, au point d’être interchangeables dans les paroles, les écrits et les pensées scientifiques, et le terme de « dissymétrie moléculaire », employé par Pasteur et d’autres à côté de « dissymétrie optique », dans les années 1850 — et même dans les décennies suivantes —, ne peut pas être interprété avec le sens de « molécule » que nous avons aujourd’hui ; c’est une des raisons pour laquelle nous proposons de ne pas lui substituer les expressions « chiralité moléculaire » ou « chiralité », au contraire des termes « hémiédrie » ou « activité rotatoire », qui ont conservé leur sens exact, parce qu’expérimental [10, 11]. Dans [1], il est montré que Pasteur utilisait le mot « molécule » avec une acception proche de celle qu’avait donnée Haüy [12], quand il proposait que les cristaux étaient des empilements de « molécules intégrantes », ayant généralisé l’observation selon laquelle un petit cristal rhomboédrique qui s’était cassé avait fait apparaître un cristal rhomboédrique plus petit.
C’est ce que l’on détecte notamment dans [13], quand Pasteur écrit que Haüy « admettait très-bien que deux substances de même composition chimique [il s’agit ici de composition chimique élémentaire, c’est nous qui précisons] pouvaient avoir des formes cristallines différentes. Ce qu’il n’admettait pas, et ce qui lui semblait inconcevable, c’est que des substances ayant la même composition chimique, et dont l’arrangement moléculaire des atomes élémentaires était le même [ici, c’est Pasteur qui souligne], eussent la même forme cristalline. » La fin de cette citation montre nettement combien il serait erroné de croire que Pasteur put — comme ses contemporains — avoir une idée claire de la notion d’atome ou de molécule à l’époque que nous considérons ici. Cela se retrouve dans « On peut donc très-bien, selon moi, jusqu’à preuve du contraire, admettre que cette variété de baryto-calcite n’est qu’une variété de baryte carbonatée unie par accident atome par atome au carbonate de chaux » [13, 14] : le mot « atome » ne peut désigner qu’une partie élémentaire. De même pour le passage suivant : « Je pense dès lors qu’il est impossible de douter qu’un certain groupe moléculaire reste constant dans tous ces sels ; que l’eau de cristallisation, que les bases, reléguées aux extrémités de ce groupe, le modifient à ces extrémités seulement, ne touchant qu’à peine, et dans la mesure de la différence des angles observés entre les facettes, à l’arrangement moléculaire central. Assurément je ne fais que confirmer ici cette opinion que tous les chimistes énonceraient, savoir qu’entre tous les sels d’un même acide, il y a quelque chose de commun. Ces faits, cependant, nous montrent, en outre, l’étroite relation qui existe entre la forme cristalline et la constitution moléculaire, et le jour que l’on peut jeter, par les études cristallographiques, sur l’arrangement des atomes » [15, 16]. Cette citation pose la question de savoir comment Pasteur et ses contemporains imaginaient les organisations à très petite échelle [10, 17, 18, 19, 20, 21] : dans une recherche sur les évolutions intellectuelles de Pasteur, cette question s’impose évidemment, notamment parce que les chimistes français, dont Pasteur [22], étaient férus des écrits d’Antoine Laurent de Lavoisier, lequel, reprenant Condillac, avait insisté sur l’importance de la nomenclature en chimie [23].
Profitons de cette dernière citation pour observer que, si l’on utilise la terminologie moderne, alors il est exact que la cristallographie donne des informations sur l’arrangement des atomes ; en revanche, il serait anachronique de voir dans la fin de la phrase de Pasteur la préfiguration des travaux de William Henry Bragg (1862–1942) et de William Lawrence Bragg (1890–1971) en 1915, puisque les rayons X ne furent découverts qu’en 1895 par Wilhelm Konrad Röntgen (1845–1923) [24].
Certains ont considéré comme « remarquable que, sans l’idée claire d’atomes et de molécules, on ait pu imaginer que la chiralité moléculaire [Pasteur parle, lui, de « dissymétrie optique » ou de « dissymétrie moléculaire »] ait été le résultat d’arrangements hélicoïdaux d’objets dans les cristaux », et ils évoquent des textes — postérieurs au dédoublement des tartrates — où Pasteur discute une organisation tétraédrique [25, 26], mais il est anachronique de penser que Pasteur avait correctement compris que certains groupes chimiques (au sens moderne) formaient des motifs tétraédriques, car cette idée ne fut introduite que plus tard, par Joseph Achille Le Bel (1847–1930) et Jacobus Henricus van’t Hoff (1852–1911), et cette fois avec une idée moderne d’atomes et de molécules [10]. En outre, la « dissymétrie moléculaire » n’est pas le résultat d’arrangements « hélicoïdaux » des atomes, ni avec l’acception pastorienne, ni avec l’acception moderne du mot « atome » [1].
Dans les idées que Pasteur devait considérer pour ses interprétations, il y avait cette différence entre les composés organiques et les composés minéraux, identifiée par Biot [4, 9], mais aussi cet étonnement que le quartz fasse tourner le plan de polarisation, d’une part, tandis que l’« acide paratartrique » (ou acide racémique) et ses sels ne le fassent pas. Pasteur écrivit ainsi, en 1850 [14] : « La cause qui produit l’hémiédrie peut avoir deux origines distinctes. Elle peut résider dans la molécule chimique elle-même, et se transporter à toutes les combinaisons de cette molécule. C’est ce qui a lieu pour l’acide tartrique et l’acide lévoracémique. La dissymétrie de la forme [du cristal] peut, d’autre part, n’être qu’une conséquence du mode d’agrégation des molécules dans le cristal, ce qui a lieu probablement dans le quartz. Or, dans ce dernier cas, la structure cristalline une fois détruite, il n’y a plus de dissymétrie, il n’y a plus de phénomène de polarisation rotatoire possible, et la substance, à l’état de dissolution ne peut dévier le plan de polarisation de la lumière. Elle le déviera à l’état cristallisé. Dans le cas même où la dissymétrie existerait dans la molécule chimique, par suite d’un arrangement spécial des atomes dans cette molécule, il pourrait arriver que la substance ne la déviât pas à l’état de dissolution. »
Dans cet extrait, la « molécule chimique » semble être la « molécule intégrante » de Haüy, une petite entité conjecturée et mal comprise à l’époque, comme on l’a signalé précédemment et dans [1]. Quant à l’arrangement des « atomes », il ne peut donc s’agir non plus de la notion actuelle, malgré l’apparence de sens que prend la phrase a posteriori. Relue sans anachronisme, cette phrase contient des termes trop flous pour être considérée comme « presciente » [2, 27, 28].
Finalement le principal mérite de Pasteur, de ses années de thèse à la publication du dédoublement des tartrates, est son activité scientifique particulièrement soutenue, même s’il se répète largement, de publication en publication [1]. Sa capacité de synthèse doit également être observée, ce que montre notamment son article du 20 mars 1848 [13], où sont cités les travaux de Laurent et d’autres, tels Gabriel Delafosse (1796–1878), qui fut élève de Biot et professeur de Pasteur : dans ce texte, sont analysées les formes cristallines de « toutes les substances dimorphes » alors connues de lui et de Delafosse, à savoir soufre, carbonate de calcium (aragonite), « baryto-calcite », « nitrate de potasse », « nitrate de soude », « sesquioxyde de fer », sulfure de cuivre, sulfure d’argent, « sulfate de potasse », iodure de mercure, « mésotypes », micas, « sulfotricarbonate de plomb », sulfate de nickel, séléniate de zinc, grenat, idocrase, chlorure de naphtaline, « chlorure de naphtaline monochlorée », pyrite, acide arsénieux, « acide titanique ».
Dans le mémoire du 22 mai 1848 [4], ce sont les « tartrates » et les « paratartrates » qui sont essentiellement considérés, mais le jeune scientifique cherche des généralisations fécondes : « On dira, et avec juste raison : Toutes les substances organiques qui dévient le plan de polarisation lorsqu’elles sont dissoutes jouiront donc de l’hémiédrie. J’aurais beaucoup désiré ne présenter ce travail à l’Académie qu’après avoir examiné les bases organiques, le camphre et d’autres substances. Mais ici on rencontre de grandes difficultés pour la recherche de l’hémiédrie. La beauté des cristaux des tartrates, leur grosseur, m’a servi considérablement. Cependant j’ai pu facilement étudier le sucre candi, et je puis annoncer, d’après mes propres recherches, que cette substance est hémiédrique, et jouit à un haut degré de la pyro-électricité polaire. C’est même par l’étude de cette dernière propriété que j’ai été assuré de l’hémiédrie, dont je me suis rendu compte ensuite par l’observation attentive de la forme cristalline. Postérieurement, j’ai trouvé que cette détermination avait été déjà faite il y a longtemps par le Dr Hankel. »
A ce stade, Pasteur était passé de l’étude morphologique des cristaux, à l’étude des rotations éventuelles du plan de polarisation qu’ils induisaient, ce qui l’avait conduit mieux caractériser l’hémiédrie des tartrates. C’était une voie qui était apparue féconde, et qu’on le voit suivre dans ses travaux ultérieurs.
2. L’après 1848
En avril 1849, alors qu’il poursuit ses études des tartrates, Pasteur annonce avoir découvert qu’un sel de l’acide formique est hémiédrique [13, 29] : « En terminant, j’annoncerai à l’Académie un résultat qui semble offrir beaucoup d’intérêt. J’ai trouvé le double caractère hémiédrique dans un autre sel organique, le formiate de strontiane. Ce sel cristallise en prismes droits à base rhombe, portant des facettes hémiédriques sur les arêtes de base, et qui conduisent à deux tétraèdres identiques, mais inverses [souligné par Pasteur]. » Puis, à la fin de cette même année, Biot informa Pasteur que l’« alcool amylique », produit lors de la fermentation de la fécule de pomme de terre, déviait le plan de polarisation de la lumière [30]. Pasteur signale des difficultés à caractériser physiquement le « composé », au-delà des déterminations de la composition élémentaire, et cela se comprend aujourd’hui, car il existe 12 composés isomères ayant la formule générale C 5 H 11 OH (voir la Figure 2) [31].
Les principaux alcools amyliques explorés par Pasteur : le (-)-(S)-2-méthylbutan-1-ol, optiquement actif, et le 3-méthylbutan-1-ol, optiquement inactif [28, 31].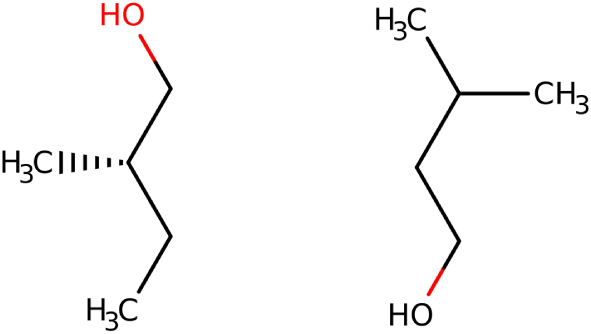
Si la fermentation apparaît ainsi dans le champ d’études scientifiques de Pasteur, il n’est pas certain que cela ait changé immédiatement le cours de ses travaux expérimentaux, car ses publications de 1849 restent consacrées aux acides tartriques et aux tartrates ; d’ailleurs, pendant longtemps, Pasteur resta attaché à sa réussite de 1848 et en chercha des prolongements directs [30, 32].
Cette observation est historiquement importante, car certains ont vu dans les études des alcools amyliques des raisons pour lesquelles, quelques années plus tard, Pasteur quitta progressivement la physico-chimie des cristaux pour les études de la fermentation, puis de la microbiologie, tandis que d’autres proposaient que la transition soit plutôt due à l’intérêt de Pasteur pour des problèmes industriels, quand il fut nommé à Lille en 1854 [26]. Nous prendrons parti plus loin à ce propos.
En 1850, Pasteur continue donc de s’intéresser aux acides tartriques et aux tartrates de « chaux » (le terme de Pasteur est ici conservé, alors que, ici par exemple, on dirait aujourd’hui « calcium », tout comme on dirait potassium, sodium, ammonium, etc. dans ce qui suit), de « potasse », de « soude », d’« ammoniaque », « émétique de potasse », « émétique d’ammoniaque » [33], mais il étend ses travaux à d’autres composés organiques, et cela est précisément une piste féconde, puisque le vivant est source de chiralité, à défaut d’avoir l’apanage de faire tourner le plan de polarisation de la lumière [34] : « Les faits que j’ai recueillis cette année se rapportent à l’asparagine, à l’acide aspartique, à la combinaison du glucose avec le sel marin, et au formiate de strontiane. […] En examinant la forme cristalline de l’asparagine, j’ai reconnu d’une manière indubitable que tous les cristaux de cette substance sont hémiédriques. L’hémiédrie est, en outre, non superposable. Il était donc probable que cette substance devait jouir de la propriété rotatoire, et c’est en effet ce que l’expérience a confirmé. […] Les relations qui unissent l’asparagine à l’acide aspartique, indiquaient l’existence probable de la propriété rotatoire dans l’acide aspartique. En effet, l’acide aspartique dévie le plan de polarisation des rayons lumineux, et son pouvoir rotatoire a de grandes analogies avec celui de l’asparagine. […] Enfin, les recherches récentes des chimistes tendant à faire admettre que l’asparagine est l’amide de l’acide malique, j’étais conduit à rechercher le pouvoir rotatoire dans l’acide malique et les malates. L’expérience a encore répondu à mon attente. L’acide malique, et les sels qui en dérivent, ont la propriété de dévier le plan de polarisation des rayons lumineux ; et j’ai retrouvé l’hémiédrie non superposable dans plusieurs malates. Mais il est un fait sur lequel je veux surtout insister à propos de l’acide malique. Cet acide offre, dans les particularités de son pouvoir rotatoire, des analogies très grandes avec les acides tartriques droit et gauche ; et ces analogies conduisent naturellement à penser qu’il existe d’intimes relations d’arrangements moléculaires dissymétriques, entre l’acide malique et l’un ou l’autre des deux acides tartriques. Il est très vraisemblable qu’il doit exister, entre l’acide malique et l’un des deux acides tartriques, droit ou gauche, un groupement moléculaire commun, avec la modification que peut apporter, dans ce groupement, la différence de composition de ces acides [c’est l’auteur qui souligne]. »
Commentons ce passage en observant que l’asparagine n’est pas l’amide de l’acide malique (l’atome d’azote ne remplace pas l’atome de carbone stéréogénique) (voir la Figure 3), mais, surtout, que l’hypothèse de « groupement moléculaire commun » entre les acides tartriques et les acides maliques n’est pas la cause de la communauté de propriétés optiques ; c’est plutôt la tétravalence du carbone, et l’organisation tétraédrique de ses substituants, laquelle conduit à la chiralité. Évidemment, le signalement de ces erreurs ne peut être une critique de Pasteur, car les idées sur la notion de radical étaient encore très discutées ; elles avaient été révisées par Laurent vers 1844, à partir de la théorie du dualisme électrochimique de Dumas [35], et c’est seulement en 1860 — c’est-à-dire l’année du colloque des chimistes de Karslruhe — qu’Auguste Cahours (1813–1891) s’autorisa à écrire [36, 37] : « On donne le nom de radicaux à des êtres particuliers dont la nature complexe peut être mise en évidence à l’aide de forces physiques ou par l’intervention des réactifs, mais qui, bien que formés de plusieurs éléments, présentent les caractères des corps simples et remplissent des fonctions exactement semblables. Ce sont, en un mot, des composés qui possèdent la propriété de former avec les corps simples des combinaisons entièrement analogues à celles que produisent ces derniers par leur union mutuelle. » À cette époque, Cahours observait que certains radicaux avaient été isolés : le cyanogène, le cacodyle, etc., tandis que d’autres « n’ont à cette heure qu’une existence purement hypothétique » : le méthyle, l’éthyle, l’acétyle, le benzoïle, l’ammonium, etc.
L’acide malique, l’acide aspartique et l’asparagine (ne sont représentées ici que les formes L).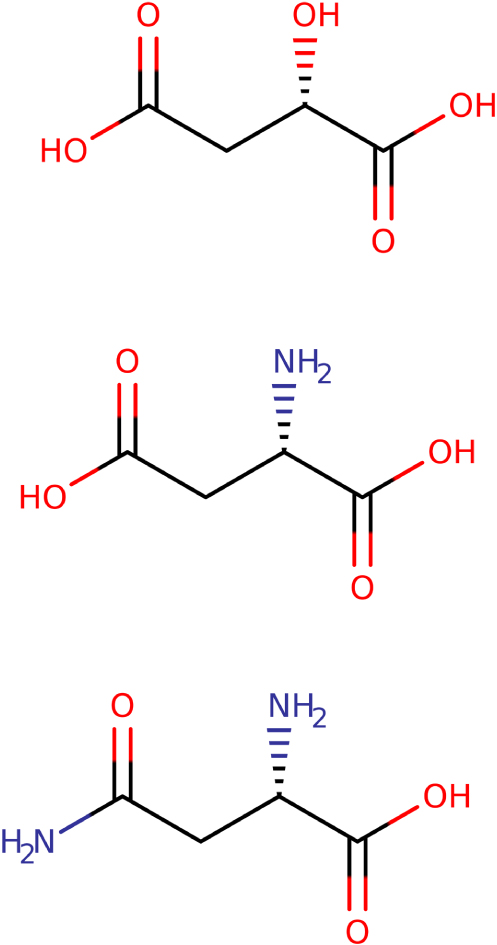
Sur sa lancée, Pasteur publie le 30 septembre 1850 ses résultats d’étude du formiate de strontiane, de l’acide aspartique et d’aspartates, de l’asparagine, de l’acide malique, des malates, de l’acide fumarique et des fumarates, de l’acide maléique, du « glucosate de sel marin » [38]. Comme pour d’autres articles antérieurs, il publie des paragraphes quasi identiques dans plusieurs articles successifs, conservant les termes « atomes » ou « molécules » pour des acceptions de son temps :
« Pendant très longtemps on ignora complètement quelle pouvait être la cause de cette dissymétrie de la forme cristalline. Il n’existe qu’un seul travail, celui de M. Delafosse, où, pour la première fois, on ait essayé d’établir que ce phénomène de l’hémiédrie tenait à la constitution intime du cristal. Pour rendre compte du phénomène, M. Delafosse s’arrête à la structure interne, à la disposition des molécules physiques, sans aller jusqu’au mode d’arrangement des atomes dans la molécule chimique. » Pasteur était trop précis pour ne pas être conscient du rapprochement, dans la fin de cet extrait, entre les deux expressions « molécules physiques » et « molécule chimique », mais il n’y a pas, à notre connaissance, de discussion de sa part de cette différence. On en est réduit à rapprocher le premier terme des textes de Haüy (les « molécules intégrantes »), et à associer le second aux explorations des chimistes, sans que la relation entre les deux termes puisse être explicitée, à cette époque.
Les conclusions du texte de 1851 sont quasiment mot à mot celles de 1850 : « Les faits précédents conduisent à supposer que l’hémiédrie du formiate de strontiane ne tient pas à l’arrangement des atomes dans la molécule chimique, mais à l’arrangement des molécules physiques dans le cristal total. » Cette observation conforte l’hypothèse que nous venons de faire.
Évidemment la question de l’activité optique des corps est loin d’être résolue, ce qui motive que Pasteur continue ses études [39] : « Or on n’a jamais, jusqu’à ce jour, donné naissance, par les procédés des laboratoires, à une substance ayant une action sur le plan de polarisation en partant de composés qui ne possédaient pas eux même cette faculté. » Ici, on trouve un écho de ses idées sur l’activité optique des composés du vivant.
Cette même année, Pasteur approche à nouveau la question des fermentations : partant de cristaux produits par Victor Dessaignes (1800–1885), un receveur de Vendôme qui faisait de la chimie dans un laboratoire personnel [40], il ne retrouve pas l’activité optique des cristaux « naturels ». Or ces cristaux avaient été obtenus par fermentation du fumarate d’ammonium en acide aspartique [41]. Pis, l’activité optique de l’ « acide aspartique » dépendait du pH : dextrarotatoire à pH élevé, lévorotatoire à faible pH.
Pour autant, Pasteur poursuivit ses études de divers composés organiques, convaincu de l’importance de la découverte qu’il aurait faite avec les acides tartriques et les tartrates : « Aujourd’hui nous voyons que les combinaisons actives sur la lumière polarisée peuvent être assez peu altérées dans leur groupement moléculaire constitutif pour conserver, sans exception, toutes leurs propriétés chimiques, en perdant seulement, dans leurs molécules constituantes, cette dissymétrie spéciale qui produit le caractère droit ou gauche. […] L’ensemble de ces quatre particularités, qui forment autant d’exceptions aux lois ordinaires du phénomène rotatoire, ne s’est présenté encore dans aucune substance. Or l’acide malique actif m’a offert ces mêmes particularités d’une manière plus saillante même que l’acide tartrique. »
A l’époque, il n’a pas trouvé l’acide mésotartrique, puisqu’il en conjecture l’existence [1] : « Il y a aussi de fortes raisons de croire qu’il peut exister un acide tartrique correspondant à l’acide malique inactif. Cet acide serait neutre sur la lumière polarisée comme l’acide racémique, mais différerait de ce dernier par sa constitution moléculaire, et ne pourrait être dédoublé en deux acides tartriques, droit et gauche. »
3. 1852 : Nommé à Strasbourg
Quand Pasteur est nommé à l’université de Strasbourg, en 1852, il continue de publier rapidement, et toujours avec sa manière fleurie, classique à l’époque [1], mais surtout de façon très redondante, d’article en article : dans une communication de 1852 [42], on retrouve les mêmes phrases que dans les textes précédents.
C’est l’époque où Mitscherlich lui signale la présence, en Saxe, d’une usine qui aurait produit industriellement le mélange racémique d’acides tartriques [43]. Désireux de gagner le prix de la Société de pharmacie de Paris, Pasteur part pour la Saxe, mais, une fois sur place, il constate que la fabrication ne forme plus le mélange racémique depuis que l’usine a changé de fournisseur de tartre (du tartre du vin, à ne pas confondre avec le carbonate de calcium [1]). Il visite les carrières et conclut que le problème résulte du raffinage : le racémique est éliminé [43].
Cette même année, il continue ses études de la quinine, de la cinchonine et de la quinidine, observe que la quinine est faite de deux isomères, comme la cinchonine, mais il ne comprend pas que la quinidine n’est que l’isomère dextrogyre de la quinine. Il observe que, au soleil, les solutions de ces composés changent de couleur, de sorte qu’il en vient à chauffer volontairement divers composés, à la recherche d’un effet sur l’activité optique (voir la Figure 4). Il nomme « quinicine » la quinine chauffée et espère avoir trouvé un nouveau médicament, mais les tests cliniques, à l’Hôpital de la charité, à Paris, sont un échec [44].
La quinine ((R)-[(2S,4S,5R)-5-éthényl-1-azabicyclo[2.2.2]octan-2-yl]-(6-méthoxyquinolin-4-yl)méthanol) et la quinidine ((S)-[(2R,4S,5R)-5-éthényl-1- azabicyclo[2.2.2]octan-2-yl]-(6-méthoxyquinolin-4-yl)méthanol).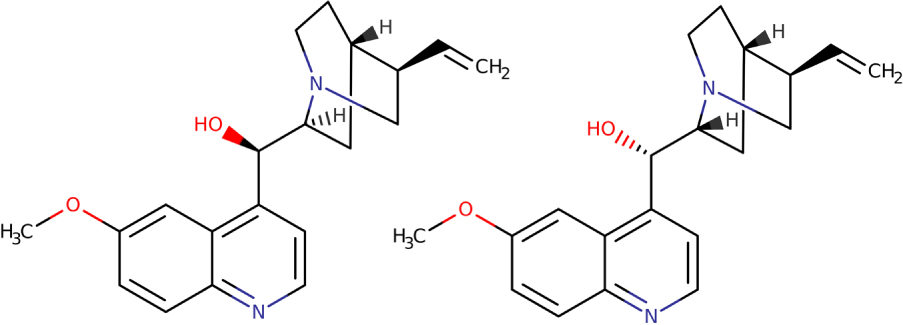
Surtout, à Strasbourg, il poursuit ses études de l’activité optique, explorant tous les échantillons des collections de la Faculté, et se convainc que les minéraux et les substances chimiques produites artificiellement en laboratoire seraient dominés par la symétrie, et que les seuls corps qui dévient le plan de polarisation de la lumière proviendraient de végétaux et d’animaux : le pouvoir rotatoire différencierait l’animé de l’inanimé, la vie de ce qui n’en est pas [42].
A l’époque, et notamment grâce à Biot, de nombreux composés organiques optiquement actifs avaient été identifiés [45], tels que l’amygdaline, divers sucres, des huiles essentielles, l’acide mandélique (nommé alors « amygdalique »), le camphre, la morphine, la strychnine, la brucine, la cinchonine, la quinine, l’albumine, etc. Les composés actifs connus étaient donc majoritairement organiques, à l’exception notoire du quartz, mais ce dernier perdait son activité optique à l’état fondu. Et Pasteur d’émettre une hypothèse « universelle » qu’il conservera longtemps [44] : « Au moment de leur regroupement, les atomes élémentaires [l’expression seule suffit à montrer, à nouveau, combien la notion d’atome était différente de la nôtre] sont soumis à une influence dissymétrique et, comme toutes les molécules organiques qui ont pris naissance dans des circonstances analogues sont identiques, quelles que soient leur origine et le lieu de leur production, cette influence doit être universelle. Elle embrasserait le globe terrestre tout entier. A elle serait due la dissymétrie moléculaire des produits organiques naturels des végétaux, produits que nous retrouvons chez les animaux à peu près sans altération, et où elle joue un rôle mystérieux duquel nous n’avons encore aucune idée. L’univers est un ensemble dissymétrique, et je suis persuadé que la vie, telle qu’elle se manifeste à nous, est fonction de la dissymétrie de l’univers ou des conséquences qu’elle entraîne ».
Dans son texte où il présente en détail ses investigations sur les acides tartriques, Pasteur fait état des pratiques qui conduisent au racémique sans les comprendre, signalant d’ailleurs plusieurs fois que les eaux-mères ont attendu plusieurs années. Puis, tandis qu’il publie des notes sur la quinidine, la strychnine, la quinine, la quinoïdine, le mystère du mélange racémique continue de le préoccuper [46, 47] : « D’ailleurs, on doit regarder l’ensemble des faces hémiédriques d’un cristal comme l’une des nombreuses formes secondaires que peut toujours revêtir une substance quelle qu’elle soit. C’est que cette identité absolue pour tout ce qui n’est pas hémiédrie et sens du phénomène rotatoire [des tartrates] n’existe qu’autant que les deux acides tartriques sont unis à des combinaisons inactives sur la lumière polarisée. Mais les place-t-on, eux ou leurs dérivés, en présence de produits qui ont une action moléculaire quelconque sur le plan de polarisation, alors toute identité cesse d’avoir lieu. »
4. Le basculement à Lille
Le passage aux études des fermentations intervient à Lille, après que Pasteur a été nommé doyen de la nouvelle faculté des sciences, en 1854. Certains ont dit que Pasteur aurait été conduit à étudier les fermentations en raison des activités industrielles de la région lilloise (fabrication d’alcool ou brasserie) ; d’autres ont supposé que Pasteur aurait été conduit aux études des fermentations par ses études de l’ « alcool amylique » [48, 49, 50]. Nous pensons qu’il n’y a pas lieu de choisir entre ces deux explications, car elles ne s’excluent pas : l’activité scientifique se fonde sur un ensemble de conditions, matérielles et intellectuelles ; et la lecture des publications de Pasteur fait penser, en outre, qu’il avait déjà tant défriché le terrain de la chiralité qu’il avait pu juger de bonne stratégie scientifique d’envisager des questions nouvelles, afin de résoudre ou d’abandonner un problème qui résistait aux explorations.
Certes, autour de Lille, les industries agricoles et alimentaires étaient essentielles, avec notamment des fermentations alcooliques à partir de betteraves, mais aussi les brasseries [50, 51, 52]. Lors de la nomination de Pasteur, le ministre de l’instruction publique avait insisté sur les applications des sciences, en soutien aux industries de la région : « Je n’ai pas besoin, Monsieur, de vous rappeler toute l’importance qui s’attache au succès de cette nouvelle Faculté des sciences placée dans une ville qui est le centre le plus riche de l’activité industrielle dans le nord de la France » [53]. En conséquence, Pasteur fit des efforts pour que les étudiants n’aient pas seulement une formation théorique, mais également des connaissances technologiques et techniques : il organisa des visites d’usines [48, 54] et traita dans ses cours des phénomènes qui avaient lieu lors de la fermentation du jus de betterave [55]. C’est là le versant de ce que je nomme l’ « hypothèse lilloise » de son évolution scientifique. Toutefois ce changement de lieu de travail, qui conduisit à l’étude de composés organiques, rejoint aussi l’ « hypothèse universelle ». Il n’y a pas lieu d’opposer ces possibilités ; au contraire, il y avait pour Pasteur une sorte de double évidence à évoluer vers les études des fermentations.
Ce qui est certain, c’est que peu après le début des cours de l’année universitaire 1856–1857, à l’automne, le père d’un des étudiants, M. Bigo, fabriquant d’alcool à partir de jus de betteraves, soumit à Pasteur des difficultés de production : l’alcool obtenu à partir des betteraves était acide, de mauvaise qualité, et les cuves de fermentation avaient une odeur « fétide » [43]. Pasteur accepta d’étudier le problème, et se trouva directement confronté à la question des fermentations [26, 51, 56]. Des indications factuelles de cet épisode figurent dans ses cahiers de laboratoire : on y trouve le nom de Bigo et le nom de la rue où se trouvait l’usine de ce dernier (à savoir la rue d’Esquermes, et non d’Esquermay comme cela a été écrit) [26, 50]. En outre, on sait que, en décembre 1856, Marie Pasteur, l’épouse de Pasteur, écrivit à son beau-père : « Louis continue à travailler avec ardeur. Il est plongé maintenant dans le jus de betterave jusqu’au cou. Il passe ses journées dans une fabrique d’alcool » [57].
Pasteur identifia l’acide lactique comme un des produits qui nuisaient à la qualité des préparations de Bigo, et c’est ainsi qu’il fut conduit aux études de la fermentation lactique, ce dont il fit des parties de son cours [51] : le 2 février 1857, les trois premières lignes sont « Suite de l’étude de la fermentation. Le phénomène nous est connu dans ses conditions principales. Son importance exige plus de détails » [26]. C’est là non plus une hypothèse « amylique » ni « universelle », mais une hypothèse « lactique », qui n’est que secondairement « lilloise ».
Ce qui est certain, aussi, c’est que c’est de cette époque lilloise (1855–1857) que datent deux articles sur l’alcool amylique [14]. Le premier, déjà évoqué [30], est un petit résumé des travaux présentés à l’Académie des sciences en 1855 : Pasteur y décrit la composition et la purification d’échantillons commerciaux d’ « alcool amylique », indiquant dans le résumé que l’alcool amylique commercial est un mélange de deux isomères très semblables, voire indiscernables chimiquement ou physiquement. À la fin de son article, Pasteur écrit que son intérêt pour ces composés est né de considérations cristallographiques : les deux alcools sont liquides dans les conditions ordinaires, mais il avait préparé une série de dérivés qui cristallisaient et trouvé que les dérivés de l’alcool optiquement actif violaient ses lois [28, 57, 58]. Découvrant une réfutation des théories qu’il avait lui-même proposées, Pasteur a dû être ébranlé, et il n’est pas certain que, avec les résultats expérimentaux dont il disposait alors, il ait pu imaginer comment il pouvait réconcilier des faits contradictoires.
Ce qui n’est guère évoqué par les historiens qui se sont intéressés à la fermentation dans l’œuvre de Pasteur [26, 50], c’est que Pasteur s’intéressa aussi au lactose, cette même année 1856 [58] : « Lorsque Kirchhoff, membre de l’Académie de Saint-Pétersbourg, eut publié la découverte si remarquable de la transformation de l’amidon en matière sucrée, Vogel essaya l’expérience de Kirchhoff sur le sucre de lait. Il fit bouillir 100 grammes de sucre de lait avec 400 grammes d’eau et 2 grammes d’acide sulfurique, pendant quelques heures, en ajoutant de temps en temps un peu d’eau pour remplacer celle qui s’évaporait par l’ébullition. La liqueur, saturée par la craie, évaporée à l’étuve, donna un sirop brun, épais, qui se prit en masse cristalline au bout de quelques jours ». Et il ajoute : « Cette matière, analogue à la cassonade, a une saveur bien plus sucrée que n’est une dissolution aqueuse la plus concentrée de sucre de lait. Ce goût excessivement sucré a fait soupçonner qu’il s’était formé du véritable sucre, propre à donner naissance à la fermentation alcoolique. En effet, à peine avait-on introduit ce produit, sous des circonstances favorables, avec la levure de bière, que la fermentation alcoolique s’est établie de la manière la plus vive, tandis que le sucre de lait ne fermente jamais. […] Tel est le sucre qui, avec de grandes apparences de raison sans doute a été pris pour du sucre de fécule ; et, à toutes les époques, les idées physiologiques émises sur le sucre de lait ont eu pour base la prétendue transformation de ce sucre en sucre de fécule. Mais, en réalité, le sucre de lait modifié par les acides est tout autre que le glucose. Je propose de le nommer lactose. On réserverait le nom de sucre de lait ou de lactine pour le sucre cristallisable du lait. »
Ici, la confusion du lactose avec le galactose ne doit pas conduire à ne pas repérer qu’apparaissent à nouveau des questions de fermentation.
Cela précède le second mémoire, consacré aux alcools amyliques, où Pasteur examine la question cristallographique ainsi posée, et où il écrit ne pas parvenir à induire l’hémiédrie cristalline. Il conclut que l’hémiédrie cristalline n’est pas une manifestation nécessaire de la « dissymétrie moléculaire » [30, 59]. Notons pour terminer que ce dernier article évoque « l’arrangement atomique des molécules », ce qui nous donne une indication supplémentaire pour analyser les conceptions structurales de Pasteur à cette époque.
En 1857 et 1858, Pasteur s’explique sur la question des fermentations, nouveau champ qu’il substitue partiellement au premier [60, 61, 62] : « Je crois devoir indiquer en quelques mots comment j’ai été conduit à m’occuper de recherches sur les fermentations. […] On s’étonnera peut-être de me voir aborder un sujet de chimie physiologique bien éloigné en apparence de mes premiers travaux. Il s’y rattache néanmoins très directement. Dans l’une de mes dernières communications à l’Académie, j’ai établi que l’alcool amylique, contrairement à ce que l’on avait cru jusqu’alors, était une matière complexe formée de deux alcools distincts, isomères, l’un déviant à gauche le plan de polarisation, l’autre dépourvu de toute action. […] Je résolus dès lors de faire une étude approfondie des deux alcools amyliques, de déterminer, s’il était possible, les causes de leur production simultanée et leur véritable origine, sur laquelle certaines idées préconçues me portaient à partager l’opinion commune. […] Si [l’alcool amylique], lorsqu’il est actif, avait le sucre pour origine, comme tous les chimistes l’admettent, son action optique serait empruntée à celle du sucre. C’est ce que je répugne à croire dans l’état actuel de nos connaissances. […] Le groupe moléculaire de l’alcool amylique est trop distant de celui du sucre pour que, s’il en dérive, il en retienne une dissymétrie d’arrangement de ses atomes. Je le répète, ce sont là des idées préconçues. Elles suffisaient cependant pour me déterminer à étudier quelle pouvait être l’influence du ferment dans la production des deux alcools amyliques. Car on voit toujours ces alcools prendre naissance dans l’opération de la fermentation, et c’était là une invitation de plus à persévérer dans la solution de ces questions. »
Il ajoute également : « J’ai été conduit à m’occuper de la fermentation à la suite de mes recherches sur les propriétés des alcools amyliques et sur les particularités cristallographiques fort remarquables de leurs dérivés. […] Je me propose d’établir dans la première partie de ce travail que, de même qu’il existe un ferment alcoolique, la levure de bière, que l’on trouve partout où il y a du sucre qui se dédouble [un mot important pour l’histoire de l’atomisme, puisque c’est le même que celui qui était utilisé pour la séparation des acides tartriques du racémique, mais qui a ici un sens différent, en langage moderne] en alcool et en acide carbonique, de même il y a un ferment particulier, une levure lactique toujours présente quand du sucre devient acide lactique, et que, si toute matière plastique azotée peut transformer le sucre en cet acide, c’est qu’elle est pour le développement de ce ferment un aliment convenable. […] Voyons maintenant les caractères de cette substance dont la production est corrélative des phénomènes compris sous la dénomination de fermentation lactique. […] Au microscope, elle est formée de petits globules ou de petits articles très-courts, isolés ou en amas, constituant des flocons irréguliers ».
On ne discutera pas ici de la controverse sur la nature des fermentations, et le rôle des micro-organismes ou de ferments inanimés, mais on soulignera que, dans ce débat scientifique, Pasteur fondait ses points de vue sur son hypothèse « universelle » du vivant, comme l’indique la suite du texte : « Tels ont été pour moi l’occasion et le motif d’expériences nouvelles sur les fermentations. Mais, comme il arrive souvent en pareille circonstance, mon travail s’est agrandi peu à peu et a dévié de sa première direction ; de telle sorte que les résultats que je publie aujourd’hui paraissent étrangers à mes études antérieures. La liaison se montrera plus évidente dans ceux qui suivront. J’espère pouvoir ultérieurement mettre en rapport les phénomènes de la fermentation et le caractère de dissymétrie moléculaire propre aux substances organiques ».
Autrement dit, il y a une continuité entre ses expériences sur les cristaux et ses études des levures, et le fil conducteur est la dissymétrie [60]. D’ailleurs, au lieu d’adopter une interprétation historique qui risquerait d’être fausse parce qu’excessivement tranchée, comment ne pas rappeler prudemment [63] que les textes où Pasteur évoque la « dissymétrie moléculaire » se sont progressivement éloignés des comptes rendus expérimentaux et pour devenir des mises en ordre de travaux ? Cela a conduit Geison à des positions tranchées, quand il a détecté des différences entre notes, cahiers et publications de Pasteur [50].
En tout cas, Pasteur commence par obtenir l’acide tartrique gauche à partir du racémique, preuve que ses préoccupations de chiralité ne sont — évidemment — pas éloignées. Puis, en 1858 [64], il montre que l’acide succinique est « un produit normal, nécessaire, de la fermentation alcoolique » [65] : « Après quelques jours de fermentation, le liquide primitivement inactif [du racémique] possède un pouvoir rotatoire à gauche sensible, et ce pouvoir augmente progressivement à mesure que la fermentation se continue, de manière à atteindre un maximum. La fermentation est alors suspendue, Il n’y a plus trace d’acide droit dans la liqueur, qui, évaporée et mêlée à son volume d’alcool, donne immédiatement une abondante cristallisation de tartrate gauche d’ammoniaque. Voilà sans doute un excellent moyen de préparer l’acide tartrique gauche ».
La lecture des mémoires de cette époque révèle que ce sont les capacités de chimiste de Pasteur qui permettent ses études innovantes des fermentations : Pasteur part, certes, d’études de la fermentation de l’acide lactique (lait aigri), parce que les travaux sur ce thème sont rares, contrairement à ceux de la fermentation alcoolique et qu’aucune levure lactique n’a été découverte, mais il faut souligner que l’acide lactique est un sous-produit de l’alcool amylique optiquement actif. Et son hypothèse sur la chiralité de la vie continue de le mouvoir : « Si l’on venait à me dire que, dans ces conclusions, je vais au-delà des faits, je répondrais que cela est vrai, en ce sens que je me place franchement dans un ordre d’idées qui […] ne peuvent être irrémédiablement démontrées. […] Il m’est avis, au point où je me trouve de mes connaissances sur le sujet, que quiconque jugera avec impartialité les résultats de ce travail et ceux que je publierai prochainement reconnaîtra avec moi que la fermentation s’y montre corrélative de la vie, de l’organisation de globules, non de la mort ou de la putréfaction de ces globules, pas plus qu’elle n’y apparaît comme un phénomène de contact, où la transformation du sucre s’accomplirait en présence du ferment sans rien lui donner, sans rien lui prendre. » Ici, on observera qu’il y avait des considérations sur le vivant, dans les études des activités optiques, et des considérations sur le vivant avec la fermentation : c’est un pont qui doit manifestement retenir l’attention, pour comprendre la transition de la cristallographie à la biochimie.
Pasteur est alors lancé dans les études de la fermentation, maintenant la fermentation alcoolique, qu’il aurait initialement évitée tant elle avait été préalablement étudiée [66] : « Je vous prie de vouloir bien annoncer à l’Académie un résultat curieux et très-inattendu. C’est la présence constante de la glycérine parmi les produits de la fermentation alcoolique ». Il découvre d’abord [67] qu’il n’y a pas d’acide lactique dans la fermentation alcoolique ; puis il s’attaque nommément à Justus von Liebig, en faisant observer que, contrairement à ce que dernier avait publié, il n’y a pas d’ammoniac dans la fermentation alcoolique [68].
5. Après 1860
En 1860, Pasteur est lancé dans les expériences sur les causes de la fermentation [69, 70] quand il fait ses leçons à la Société chimique de Paris (aujourd’hui la Société chimique de France) [71] : il y insiste sur les questions de chiralité en relation avec les fermentations, comme dans les fermentations des acides tartriques. Il ne mentionne l’ « alcool amylique » que pour dire qu’il avait découvert un tel alcool inactif, ce qui est le départ d’une série de composés. Nous proposons de voir, dans cette insistance sur la fermentation des acides tartriques, et pas sur l’alcool amylique, moins une volonté de reconstruire l’histoire qu’une manifestation d’un intérêt scientifique nouveau. D’ailleurs, dans une conférence qu’il fit à la Société centrale de médecine vétérinaire en 1880 [70], alors qu’il retraçait l’évolution de sa carrière, Pasteur ne dit rien de l’ « alcool amylique » et il indique clairement que c’est l’observation du métabolisme énantiosélectif des acides tartriques par des micro-organismes qui l’avait dirigé vers les fermentations. Cette observation est intéressante, car elle montre le choix de Pasteur, parmi des causes multiples.
Parallèlement à l’exploration de la transition vers l’étude des fermentations, nous avons suivi jusqu’ici l’évolution du sens qu’avaient, pour Pasteur, les mots « atomes » et « molécules », mais qu’en pensait-il en 1860 ? Considérons trois extraits [71] :
- « Rappelez-vous la définition de l’espèce chimique que j’indiquais tout à l’heure : c’est la collection de tous les individus identiques par la nature, la proportion et l’arrangement des éléments. […] Dans les corps isomères, la nature et la proportion sont les mêmes. L’arrangement seul diffère. Le grand intérêt de l’isomérie a été d’introduire dans la science ce principe que les corps peuvent être et sont essentiellement différents par cela seul que l’arrangement des atomes n’est pas le même dans leurs molécules chimiques. »
- « Les atomes de l’acide [tartrique] droit sont-ils groupés suivant les spires d’une hélice dextrorsum, ou placés aux sommets d’un tétraèdre irrégulier, ou disposés suivant tel ou tel assemblage dissymétrique déterminé ? Nous ne saurions répondre à ces questions. »
- « Permettez-moi de représenter grossièrement, quoique au fond avec justesse, la structure du quartz et celles des produits organiques naturels. Imaginez un escalier tournant dont les marches seraient des cubes, ou tout autre objet à image superposable. Détruisez l’escalier, et la dissymétrie aura disparu. La dissymétrie de l’escalier n’était que le résultat du mode d’assemblage de ses marches élémentaires. Tel est le quartz. […] Imaginez, au contraire, le même escalier tournant formé de tétraèdres irréguliers pour marches. Détruisez l’escalier, et la dissymétrie existera encore. »
Les deux leçons datent du 20 janvier et du 3 février, tandis que le congrès de Karlsruhe eut lieu du 3 au 5 septembre : Pasteur, n’ayant pas exploré la question particulière des théories atomiques, n’avait pas de raison de changer de point de vue. D’ailleurs, ses termes restent mal fixés en 1863 [43] : « Or les groupements atomiques qui composent les molécules de toutes les espèces chimiques sont des objets et des assemblages que nous trouvons autour de nous. A priori, donc, on peut croire qu’eux également doivent se partager en nos deux catégories : les groupements d’atomes qui ont un plan de symétrie et une image qui leur est superposable, et les groupements d’atomes qui n’ont pas de plan de symétrie et une image qui ne leur est pas superposable. En d’autres termes, il doit y avoir des groupes d’atomes symétriques et d’autres dissymétriques, c’est-à-dire des groupes droits et gauches, des groupes inverses les uns des autres. Ceux-ci, nous les connaissons : c’est, par exemple, le groupe tartrique droit et le groupe tartrique gauche. Il existe une foule de groupes d’atomes dissymétriques qui attendent encore la production artificielle ou naturelle de leurs inverses. Nous avons le sucre droit : nous ignorons l’existence du sucre gauche. Nous avons l’albumine gauche, nous ignorons l’albumine droite. »
Ici Pasteur parle de « groupements d’atomes » ou de « groupes d’atomes », et non plus de « molécules », et il n’est pas clair de savoir quelle relation il fait entre entités. En 1874, dans une lettre adressée à Michel Eugène Chevreul (1786–1889), Pasteur évoque une « définition de l’espèce » (chimique) [72], mais les analyses présentées dans [1] indiquent que, même dans les années 1910, les idées restaient mal fixées à ce propos.
En tout cas, les idées initiales sur la « dissymétrie moléculaire » ne l’ont pas quitté, après son changement de champ de recherche, et elles motivent que, en 1871, soit 15 ans après avoir arrêté ses travaux sur la chiralité, il ait encore pu croire à une base universelle de la chiralité, et repris des expériences pour l’établir [73]. Il soutint cette idée en 1875 : « Transformer un corps inactif en un autre corps inactif, qui a la faculté de se résoudre simultanément en un corps droit et son symétrique, n’est en rien comparable à la possibilité de transformation d’un corps inactif en un corps actif simple. C’est là ce qu’on n’a jamais fait ; c’est là, au contraire, ce que la nature vivante fait sans cesse sous nos yeux » [74].
En 1883, Pasteur continue de promouvoir son idée « universelle », physique, de l’origine de la chiralité [75] : « Que faut-il faire pour imiter la nature ? Il faut rompre avec vos méthodes, qui sont, à ce point de vue, surannées et impuissantes. Il faut chercher à faire agir des forces dissymétriques, recourir à des actions de solénoïde, de magnétique, de mouvement dissymétrique lumineux, à des actions de substances elles-mêmes dissymétriques. Lorsque, entraîné, enchaîné devrais-je dire, par une logique presque inflexible de mes études, j’ai passé des recherches de cristallographie et de chimie moléculaire à l’étude des ferments, j’étais tout entier à la pensée d’introduire la dissymétrique dans les phénomènes chimiques. »
Ou encore : « Ces expériences accusent la ligne de démarcation profonde entre le règne minéral et le règne organique, puisque pour imiter ce que fait la nature, c’est-à-dire préparer un corps droit ou un corps gauche, nous sommes contraints de faire intervenir des actions toutes particulières, des actions de dissymétrie. La ligne de démarcation dont nous parlons n’est pas une question de chimie pure et d’obtention de produits tels ou tels, c’est une question de forces ; la vie est dominée par des actions dissymétriques dont nous pressentons l’existence enveloppante et cosmique. Je pressens même que toutes les espèces vivantes sont primordialement, dans leur structure, dans leurs formes extérieures, des fonctions de la dissymétrie cosmique. La vie, c’est le germe et le germe, c’est la vie. Or qui pourrait dire ce que seraient les devenir des germes, si l’on pouvait remplacer dans ces germes les principes immédiats, albumine, cellulose, etc., etc., par leurs principes dissymétriques inverses ? La solution consisterait d’une part, dans la découverte de la génération spontanée […] oui, il y a une séparation profonde entre le règne organique et le règne minéral. Cette ligne de démarcation a deux expressions : d’une part on n’a jamais fait un produit de synthèse, minéral ou organique […] d’autre part, la dissymétrie préside aux actions chimiques qui donnent lieu aux principes immédiats essentiels de la vie végétale ».
Les tentatives de Pasteur de produire de la chiralité moléculaire par l’action de forces physiques n’aboutirent pas [51, 73]. Pourtant il n’abandonna pas sa croyance dans le rôle de telles forces universelles dans la genèse de la chiralité moléculaire, et, même plus tard, il entreprit des expériences pour produire des composés optiquement actifs en utilisant des champs magnétiques, mais aucun facteur biologique [73]. Entre-temps, les études des fermentations l’avaient conduit à l’étude des micro-organismes, et à toutes les réalisations pour lesquelles il est justement célèbre : fermentation acétique, maladie du ver à soie, maladie du charbon, rage, etc.
Finalement l’examen des textes réunis ici montre comment des hypothèses fausses, fondées sur des théories insuffisantes, ont pu permettre à un scientifique remarquablement actif de progresser, d’accumuler des données expérimentales, qui, longtemps après qu’il s’était réorienté, ont été éclairées par des travaux d’autres scientifiques : les tétraèdres de Joseph Achille Le Bel (1947–1930) et de Jacobus Henricus Van’t Hoff (1852–1911) n’avaient rien à voir avec ceux de Pasteur, mais ils donnèrent la possibilité de comprendre la « dissymétrie moléculaire », et de faire advenir les idées de « chiralité » [1]. En quelque sorte, Pasteur se justifie par anticipation à cet égard quand il réunit, en 1878, d’anciens travaux sur la « dissymétrie moléculaire » pour les publier sous le titre : « Études de chimie moléculaire ou recherches sur la dissymétrie dans les produits organiques naturels » (le livre ne fut pas achevé) [75]. Il y écrit : « Mais, comme le dit quelque part Lavoisier, c’est le sort de tous ceux qui travaillent d’apercevoir un nouveau pas à faire sitôt qu’ils en ont fait un premier, et ils ne donneraient jamais rien au public, s’ils attendaient qu’ils eussent atteint le bout de la carrière qui se présente successivement à eux et qui paraît s’étendre à mesure qu’ils avancent pour la parcourir. » C’est bien ce qu’il a fait.
Conflit d’intérêt
L’auteur n’a aucun conflit d’intérêt à déclarer.




 CC-BY 4.0
CC-BY 4.0