1 Introduction
Les zéolites sont des tecto-aluminosilicates qui répondent à la formule générale Mn+x/n[(AlO2)x(SiO2)y]x–·z H2O, où M est un cation échangeable de valence n et z le nombre de molécules d'eau d'hydratation. La structure cristalline des zéolites est caractérisée par des unités primaires de construction formées de tétraèdres SiO4 et AlO4–, reliés entre eux par leurs sommets. L'arrangement final conduit à des espaces internes vacants en forme de pores, de cages et de canaux. À chaque atome d'aluminium trivalent correspond une charge négative dans le réseau. Le réseau zéolitique covalent est donc anionique, et les cations Mn+ assurent l'électroneutralité du solide : ils sont appelés cations de compensation [1,2].
On dénombre plus de 40 zéolites naturelles et plus de 150 nouvelles structures synthétiques [3]. Les zéolites naturelles les plus connues sont l'analcime, la clinoptilolite, la chabasite, l'érionite, la mordénite et la philipsite. Les zéolites naturelles et synthétiques sont largement utilisées à cause de leurs propriétés exceptionnelles [3]. En effet, grâce à leur structure particulière, les zéolites sont utilisées comme échangeurs d'ions, tamis moléculaires, desséchants, catalyseurs. Il faut mentionner aussi leur récente application dans la protection de l'environnement (épuration des eaux usées par élimination des métaux lourds, adsorption de gaz polluants), dans l'agriculture comme support d'engrais et de produits phytosanitaires, ou pour l'amendement des sols [3–7].
L'analcime, de formule structurale (Na(AlSi2)O6·H2O), a un volume de pores estimé à 18%, un diamètre des canaux de 2,6 Å, une capacité d'échange ionique de 4,54 mequiv g−1 et présente une grande stabilité hydrothermique. C'est une zéolite de choix pour le stockage de résidus radioactifs, car les ions et les molécules d'eau n'ont qu'une faible mobilité dans ses pores [8,9].
Il s'agit pour nous de caractériser des échantillons d'analcimolites du bassin de Tim Mersoï (Nord du Niger) par utilisation de la diffraction des rayons X (DRX), la microscopie électronique à balayage (MEB) et la microscopie de transmission à haute résolution (TEM).
2 Matériaux et techniques expérimentales
Au Niger, la zéolite naturelle analcime a été mise en évidence dans les dépôts d'âge Permien à Jurassique (290 à 150 millions d'années) de la bordure occidentale de l'Aïr (Fig. S-1). Le terme d'analcimolite a ensuite été proposé pour désigner ces dépôts à analcime [10,11]. Les analcimolites comprennent : le groupe permien d'Izégouandane, la formation triasique d'Aguélal, les groupes jurassiques de Goufat et de Wagadi (Fig. S-2a).
Les échantillons, finement broyés, ont servi pour la caractérisation par diffraction des rayons X (DRX) sur poudre. Le diffractomètre utilisé est de type Siemens D5000, équipé d'une anticathode de cuivre (radiation Cu Kα, λ = 1,5406 Å), fonctionnant sous 40 kV et 30 mA. Tous les diffractogrammes ont été enregistrés à température ambiante. Les résultats obtenus par DRX sont complétés par microscopie électronique à balayage avec un appareil Hitachi S-350, fonctionnant à 20 kV, couplé avec une sonde EDAX pour effectuer une microanalyse (Link ISIS) permettant de lier in situ la composition chimique des particules observées. La DRX est utilisée pour identifier les différentes phases cristallines contenues dans les échantillons, tandis que la MEB/EDAX permet une caractérisation morphologique et élémentaire des échantillons.
Des images ont été aussi obtenues en utilisant un microscope électronique de transmission à haute résolution (TEM), JEOL 3010, sous une tension d'accélération de 300 kV.
3 Résultats
3.1 Caractères pétrographiques
Notre étude porte sur une coupe (Fig. S-2b) levée dans une carrière à ciel ouvert de la formation Abinky (Fig. S-1), située à l'ouest de la flexure-faille d'In Azaoua-Arlit. La distinction des faciès intègre des données sédimentaires (surface de ravinement ou d'érosion), lithologiques (changement de faciès) et granulométriques.
D'une épaisseur d'environ 25 m, cette coupe présente six couches distinctes, au niveau desquelles ont été réalisés des échantillonnages (Fig. S-2b). Du sommet vers la base, on distingue les faciès ci-après, dans lesquels les prélèvements ont été effectués.
3.1.1 Faciès 1 (échantillons CA.1, CA.2, CA.3 et CA.4)
Il s'agit d'un niveau à analcimolite gréseuse massive, de couleur jaune à ocre, à taches brun chocolat. L'analcimolite se présente sous forme de glomérules associés à un mélange d'oxyde de fer et de quartz.
3.1.2 Faciès 2 (échantillons CA.5, CA.6, CA.7 et CA.8)
Ce faciès est représenté par un niveau à analcimolites gréseuses, en couches lenticulaires de couleur jaune ocre à verdâtre, avec des poches à recristallisations blanchâtres, mal cimentées par une matrice d'oxyde de fer noirâtre.
3.1.3 Faciès 3 (échantillons CA.9 et CA.10)
Il est représenté par des grès très grossiers à lentilles d'analcimolite blanchâtres, ocres et verdâtres, organisés en couches à litage discontinu ondulant.
3.1.4 Faciès 4 (échantillons CA.11, CA.12, CA.13 et CA.14)
C'est un niveau épais, de plus de 5 m de puissance, à analcimolite brun rougeâtre, organisé en couches plus ou moins massives. La roche à cassure conchoïdale présente des fentes de retrait courbes, discontinues et des surfaces de glissement (microfailles) à oxydes de fer, avec, plus ou moins, une recristallisation de quartz. On note également la présence d'un lit d'analcimolite ondulant discontinu blanc jaunâtre, avec d'abondantes recristallisations de quartz.
3.1.5 Faciès 5 (échantillons CA.15 et CA.16)
Ce faciès présente des niveaux gréseux plus grossiers, à matériel peu roulé et très altéré, dans une gangue gréso-argileuse pulvérulente de couleur rouille. On observe de rares intercalations de plages lenticulaires d'analcimolite chocolatée à cassure esquilleuse. Les recristallisations de silice sont abondantes dans les cavités.
3.1.6 Faciès 6 (échantillons CA.17 et CA.18)
La roche correspond à des grès fins, mal cimentés. Les phases amorphes de silice et d'analcime sont bien représentées. Le faciès correspond à un ensemble massif, clair avec des rares taches rougeâtres, avec un liseré jaune clair, plus ou moins ondulant vers la base.
3.2 Caractérisation physico-chimique
Les Fis. S-3.a, S-3.b et S-3.c rapportent les diffractogrammes relatifs aux différents échantillons. Ces diagrammes montrent la présence d'analcime et de quartz dans tous les échantillons. On retrouve les pics caractéristiques de l'analcime (en trait plein) et du quartz (en pointillés). Les valeurs de la distance inter réticulaire d sont reportées dans le Tableau 1 et sont comparées à celles de l'analcime de référence et à celles obtenues sur des analcimolites de la même région [10,12]. Rappelons que, dans le cas de l'analcime, les principaux pics sont situés à d = 2,93, 3,43 et 5,60 Å. Dans le cas du quartz, les pics sont à 3,34 et 4,27 Å. Les Fig. S-3a et b concernent les échantillons constitués essentiellement d'analcime et de quartz, alors que la Fig. S-3c représente les diffractogrammes d'échantillons présentant, en outre, d'autres phases cristallines en teneur notable. Le diffractogramme indexé de l'échantillon CA.14 est reporté sur toutes ces figures. Pour l'ensemble des échantillons, les pics observés sont bien fins, preuve de la bonne cristallinité des différents constituants des échantillons.
Comparaison des distances inter-réticulaires (d) avec les valeurs de référence [12] et celles obtenues par Pacquet [10]
| Ce travail | Pacquet [10] | Flinders [12] | Ce travail | Pacquet [10] | Flinders [12] | ||||||
| d (Å) | I | d (Å) | I | d (Å) | I/I1 | d (Å) | I | d (Å) | I | d (Å) | I/I1 |
| 6,87 | tf | 6,87 | 5 | 1,713 | f | 1,715 | f | 1,716 | 60 | ||
| 5,59 | F | 5,61 | F | 5,61 | 80 | 1,687 | f | 1,688 | f | 1,689 | 40 |
| 4,844 | m | 4,86 | m | 4,86 | 40 | 1,661 | tf | 1,664 | tf | 1,664 | 10 |
| 3,681 | f | 3,67 | f | 3,67 | 20 | 1,615 | tf | 1,618 | tf | 1,618 | 20 |
| 3,425 | TF | 3,43 | TF | 3,43 | 100 | 1,593 | f | 1,595 | f | 1,596 | 30 |
| 3,24 | tf | 1,495 | tf | 1,498 | tf | 1,498 | 20 | ||||
| 2,921 | F | 2,925 | F | 2,925 | 80 | 1,478 | tf | 1,479 | tf | 1,480 | 20 |
| 2,797 | f | 2,802 | f | 2,801 | 20 | 1,462 | tf | 1,463 | ttf | 1,463 | 10 |
| 2,687 | m | 2,69 | m | 2,693 | 50 | 1,444 | tf | 1,446 | tf | 1,447 | 10 |
| 2,501 | m | 2,508 | m | 2,505 | 50 | 1,414 | f | 1,413 | f | 1,415 | 40 |
| 2,423 | f | 2,429 | f | 2,426 | 30 | 1,386 | f | 1,386 | 5 | ||
| 2,222 | m | 2,225 | f | 2,226 | 40 | 1,371 | tf | 1,37 | f | 1,372 | 10 |
| 2,172 | tf | 2,168 | 5 | 1,357 | f | 1,358 | f | 1,359 | 40 | ||
| 2,115 | tf | 2,115 | 5 | 1,308 | tf | 1,308 | 10 | ||||
| 2,020 | tf | 2,025 | tf | 2,022 | 10 | 1,285 | tf | 1,285 | 20 | ||
| 1,938 | tf | 1,938 | tf | 1,94 | 5 | 1,262 | tf | 1,263 | 20 | ||
| 1,901 | f | 1,904 | m | 1,903 | 50 | 1,222 | tf | 1,220 | 30 | ||
| 1,865 | f | 1,867 | f | 1,867 | 40 | 1,185 | tf | 1,185 | 10 | ||
| 1,835 | tf | 1,833 | 5 | 1,167 | tf | 1,168 | 10 | ||||
| 1,740 | m | 1,742 | m | 1,743 | 60 | 1,119 | tf | 1,120 | 10 |
Les résultats de la microanalyse à la sonde EDAX sont reportés dans le Tableau 2, qui donne le pourcentage massique des différents oxydes dans les échantillons analysés. La présence de silicium et d'aluminium comme éléments majoritaires confirme la forte présence des phases analcime et quartz.
| Échantillon | % Massique en oxyde | Total % | PFa% | |||||||||
| Na2O | MgO | Al2O3 | SiO2 | K2O | CaO | TiO2 | MnO2 | Fe2O3 | CuO | |||
| CA.1 | 7,20 | 14,24 | 68,33 | 0,90 | 1,15 | 1,17 | 0,21 | 93,2 | 6,8 | |||
| CA.2 | 6,34 | 13,49 | 66,91 | 0,97 | 1,59 | 2,98 | 0,22 | 92,5 | 7,5 | |||
| CA.3 | 7,09 | 12,82 | 66,07 | 0,37 | 0,31 | 1,17 | 5,07 | 92,9 | 7,1 | |||
| CA.4 | 6,25 | 11,38 | 69,37 | 0,29 | 1,94 | 5,22 | 94,4 | 5,6 | ||||
| CA.5 | 4,66 | 9,18 | 36,11 | 38,23 | 0,81 | 1,03 | 4,01 | 0,27 | 94,3 | 5,7 | ||
| CA.6 | 4,83 | 0,53 | 15,04 | 60,37 | < 0,1 | 1,12 | 1,34 | 8,12 | 91,4 | 8,6 | ||
| CA.7 | 7,95 | 14,27 | 54,78 | 0,50 | 1,34 | 12,44 | 0,22 | 91,5 | 8,5 | |||
| CA.8 | 7,55 | 13,42 | 52,80 | 0,57 | 1,58 | 15,11 | 0,17 | 91,2 | 8,8 | |||
| CA.9 | 4,11 | 8,75 | 44,83 | 0,43 | 0,78 | 1,52 | 32,06 | 0,32 | 92,8 | 7,2 | ||
| CA.10 | 8 | 15,76 | 59,75 | 0,27 | 1,53 | 1,82 | 4,92 | 0,17 | 92,2 | 7,8 | ||
| CA.12 | 6,18 | 10,92 | 61,51 | 1,61 | 12,84 | 0,35 | 93,4 | 6,6 | ||||
| CA.14 | 6,28 | 12,96 | 64,16 | 0,21 | 1,51 | 1,12 | 6,73 | 0,22 | 93,2 | 6,8 | ||
| CA.15 | 2,1 | 0,24 | 6,24 | 77,88 | 4,92 | 0,41 | 0,56 | 5,34 | 97,7 | 2,3 | ||
| CA.16 | 4,58 | 1,18 | 16,32 | 57,95 | 2,96 | 1,39 | 2,21 | 7,15 | 0,18 | 93,9 | 6,1 | |
| CA.17 | 1,3 | 11,2 | 76,2 | 0,5 | 1,2 | 0,8 | 4,6 | 0,2 | 96 | 4,0 |
a PF = perte au feu à 500 °C.
Des observations en microscopie électronique ont été réalisées sur les échantillons. À titre d'exemple, la Fig. 1 représente des images obtenues sur l'échantillon CA.1 ; la Fig. 2 présente une image haute résolution d'un cristal d'analcime du même échantillon CA.1.

Images MEB de l'échantillon CA.1.

Image TEM de l'analcime dans CA.1.
4 Discussion
L'analyse des diffractogrammes a été faite en utilisant la base de données PDF-1 de l'ICDD (International Center of Diffraction Data) ; elle montre que les échantillons sont formés essentiellement d'analcime et de quartz. Aucune trace d'une autre zéolite n'a été mise en évidence.
Toutefois, on observe sur les diffractogrammes des pics, généralement de très faible intensité, qui ne sont attribués, ni au quartz, ni à l'analcime, ni à aucun autre silicate ; ce qui met en évidence la présence d'autres phases cristallines, en quantités plus ou moins faibles. Ces pics sont parfois importants, indiquant une présence appréciable de la phase correspondante, comme le montre la Fig. S-3c. Ainsi, on observe sur le diffractogramme de l'échantillon CA.5 un pic intense à d = 3,06 Å, attribué à la présence de calcite CaCO3 et, sur celui de l'échantillon CA15, un pic moyen à d = 3,24 Å, qui est associé au feldspath potassique KAlSi3O8, sous sa forme microcline.
Les résultats de la microanalyse EDAX sont en accord avec les différentes phases identifiées à partir des différents diffractogrammes. Ainsi, la présence de calcite dans l'échantillon CA.5 est confirmée par la teneur élevée en calcium (atteignant 38%). La calcite est identifiée à partir de ses principaux pics, à d = 2,10, 3,04 et 3,86 Å (comme indiqué sur la Fig. S-3c). La présence de calcite est également vérifiée par analyse thermogravimétrique (ATG). Les courbes ATG et DTG (dérivée de la courbe ATG) obtenues sur cet échantillon sont représentées sur la Fig. 3. Sur le diagramme, on distingue deux domaines bien distincts : un domaine entre 100 et 400 °C, correspondant à la déshydratation de l'analcime [9], et un autre, entre 580 et 800 °C, dans lequel la calcite se décompose en oxyde de calcium. En utilisant la perte de masse associée à la décomposition de la calcite [13,14], on estime la teneur de ce minéral dans l'échantillon à environ 36%. Le taux de potassium corrobore la présence de K-feldspath, mise en évidence par DRX dans l'échantillon CA.15.
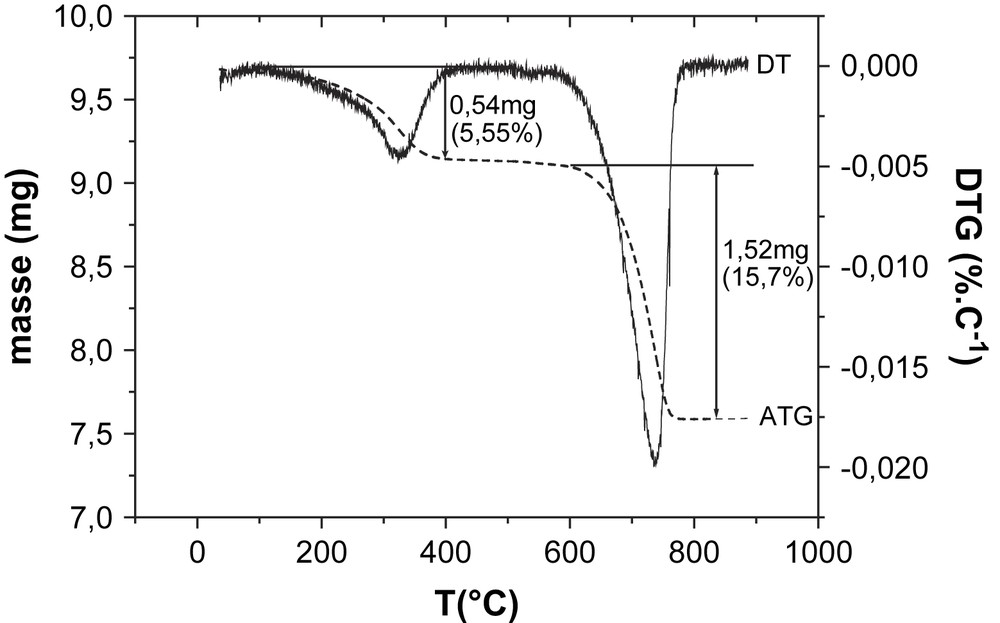
Courbes ATG et DTG de l'échantillon CA.5.
Sur les diffractogrammes de tous les échantillons, nous avons observé un pic faible à d = 3,52 Å, attribué à l'oxyde de titane TiO2 sous sa forme anatase. Ceci est en accord avec la présence de titane en faibles quantités dans les échantillons, comme le montre le Tableau 2.
L'analyse chimique semi-quantitative à la sonde EDAX révèle la présence de fer dans tous les échantillons. La teneur en fer est particulièrement élevée dans les échantillons CA.8 et CA.9. Le fer se trouve essentiellement sous forme de gœthite FeO(OH), identifiée à partir de ses principaux pics à d = 2,45, 2,69 et 4,18 Å (Fig. S-3c). La faible intensité des pics peut s'expliquer par le fait que le fer se trouve aussi sous forme de nontronite A Na0,3Fe2Si4O10(OH)2·xH2O.
Le cuivre, observé en très faible teneur dans tous les échantillons, est attribué à la présence de la ferrite de cuivre CuFe2O4.
L'analyse des diffractogrammes et des résultats de microanalyse des différents échantillons sont en accord avec les descriptions géologiques. Elle confirme et précise que la teneur en quartz dans les échantillons augmente vers la base de la coupe : les échantillons prélevés au sommet de la coupe contiennent de faibles proportions de quartz, tandis que ces pics deviennent plus importants dans les échantillons de la base de la coupe (CA.18, Fig. S-3b). Ceci s'explique par des phénomènes de lessivage, tandis que l'abondance du fer, observée dans les échantillons CA.8 et CA.9, peut être mise en relation avec les fluctuations de la nappe phréatique. L'échantillon CA.5 présente un comportement particulier, avec une forte teneur en calcium, et ne contient presque pas de quartz.
Sur les images de microscopie MEB, représentées sur la Fig. 1, on reconnaît des cristaux de haute qualité morphologique. Les particules observées montrent bien l'habitus cristallin typique de l'analcime, le trapézoèdre isométrique, tandis que diverses combinaisons d'inter-croissance ont donné naissance à une large variété de formes simples et complexes. Leurs tailles et leurs morphologies se révèlent assez hétérogènes. La Fig. 1a montre aussi la formation d'autres phases cristallines à la surface des cristaux d'analcime. Les résultats de l'analyse EDAX sur ces zones et les spectres DRX indiquent qu'il s'agirait de cristaux de quartz ou de silice. Toutefois, la multitude des cristaux d'analcime observée sur la Fig. 1b montre l'abondance de cette zéolite dans l'échantillon CA.1.
La Fig. 2 présente une image de haute résolution d'un cristal d'analcime. On peut noter que la structure de l'analcime est très ordonnée et libre de défauts, ce qui s'accorde avec la qualité des diffractogrammes de rayons X obtenus.
5 Conclusion
Il ressort des différentes analyses effectuées que l'analcime constitue la phase cristalline majeure des échantillons prélevés, même si du quartz est également présent, en proportions très variables selon les échantillons. Aucune trace d'une autre variété de zéolite n'a été décelée. Les échantillons situés au sommet de la coupe sont plus riches en analcime, alors que la proportion de quartz augmente dans les échantillons à la base de la coupe. Ces résultats nous paraissent de nature à promouvoir des investigations visant à une valorisation des ressources zéolitiques du bassin de Tim Mersoï.


